原发性肝癌为威胁国民健康的重大疾病之一,是中国癌症第2大死因,2020年全球有83万人死于肝癌,我国约占1/2[1-2]。原发性肝癌分为肝细胞癌(HCC)及肝内胆管癌,HCC占80%~90%[3],其起病隐匿,许多患者确诊时错失手术机会,而晚期HCC全身治疗效果有限,预后较差[4-5]。以索拉非尼为代表的酪氨酸激酶*制剂抑**(TKI)可一定程度延长部分患者生存期,但全身治疗仍面临诸多挑战[6]。
随着程序性死亡受体1(PD-1)和细胞毒性T淋巴细胞相关蛋白4(CTLA4)*制剂抑**临床研究结果揭晓,免疫检查点*制剂抑**(ICI)为主的免疫治疗在多癌种中表现出令人鼓舞的疗效。作为人体关键的免疫器官,肝脏在维持机体免疫耐受中发挥重要作用[7]。早期HCC免疫治疗的临床效果欠佳,但随着研究不断深入和更新,新的ICI和联合用药给患者带来生存获益,为HCC的系统治疗带来新的可能。
本文综合近5年文献及2022年美国临床肿瘤学会(ASCO)年会研究报告[8],就HCC免疫治疗最新进展及治疗策略进行综述,以期为临床研究与决策提供参考。
1 ICI单药治疗进展
HCC具有高度异质性,免疫微环境复杂,ICI单药通常效果不佳,多为中晚期HCC的2线治疗方案,以PD-1/PD-L1及CTLA-4为靶点[9-10]。美国食品药品监督管理局(FDA)和国家药品监督管理局(NMPA)批准的主要免疫治疗药物名称及适应症整理于表1。
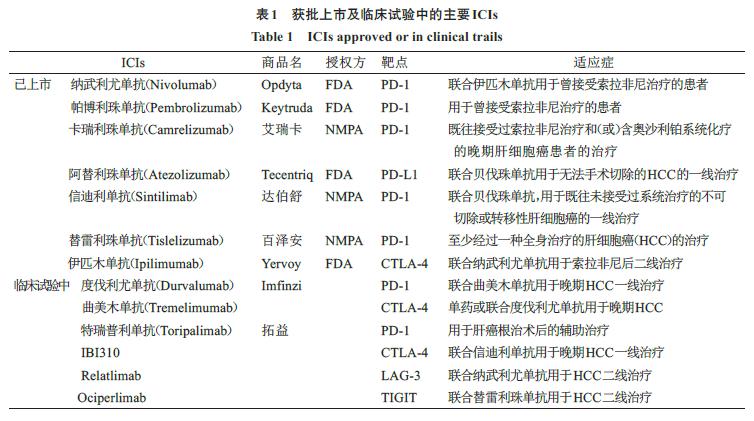
目前,中国临床肿瘤学会(CSCO)免疫检查点*制剂抑**临床应用指南(2022版)[11]、原发性肝癌诊疗指南(2022年版)[12]及肝细胞癌免疫治疗中国专家共识(2021版)[13]推荐帕博利珠单抗、卡瑞利珠单抗和替雷利珠单抗为二线方案。
在所有ICI单药中,帕博利珠单抗对于晚期未进行过治疗的HCC患者Ⅱ期临床获得了同类药物最高的18.3%的客观缓解率(ORR)[14-15]和17个月中位生存期(mOS)[16](表2)。但该药之前作为二线用药的Ⅲ期临床未达到预期的结局指标[36](表3)。为便于比较,将I/Ⅱ期及Ⅲ期临床研究结果的ORR、mOS、治疗相关不良事件(TRAE)、严重不良事件(SAE)、风险比(HR)等数据分别整理于表2[14-35]、3[36-41]。

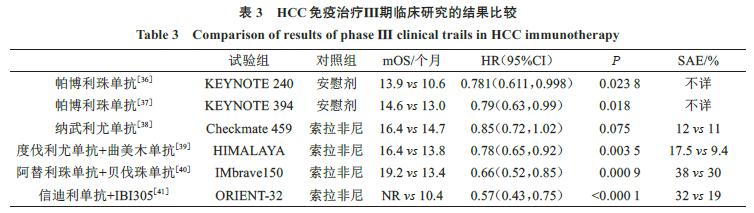
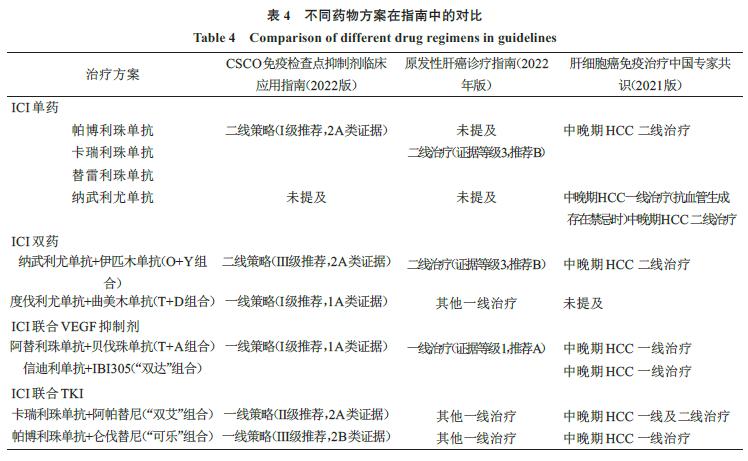
后续研究显示帕博利珠单抗对亚洲人群疗效更优(ORR为20.6%、mOS为13.8个月)[37,42],据此被推荐为晚期HCC二线治疗(表4)。CSCO诊疗指南证据类别与推荐等级分I级推荐、Ⅱ级推荐、Ⅲ级推荐、1A类证据、2A类证据、2B类证据、2B类证据。I级推荐:适应症明确、可及性好、肿瘤治疗价值稳定,纳入医保的诊治措施;Ⅱ级推荐:具有高级别证据,但可及性差或效价比不高;Ⅲ级推荐:循证证据不足,但专家组认为可以接受。1A类证据:大型随机对照研究;2A类证据:小型随机对照研究、病例对照研究,专家一致共识;2B类证据:小型随机对照研究、病例对照研究,专家基本一致共识。原发性肝癌诊疗指南证据类别与推荐等级:A为绝大多数目标用户均应采纳该推荐意见;B为多数目标用户会采纳该推荐意见,执行过程中应注意考虑医患共同决策[11]。
卡瑞利珠单抗在Ⅱ期临床中对进展后继续用药的患者疗效尚佳(mOS为16.9个月)[17-18],尽管反应性皮肤毛细血管内皮增生发生率较高(66.8%),但这可能与良好预后相关[43]。替雷利珠单抗与卡瑞利珠单抗疗效相近[19],不良事件的发生率更低[20](表2),现正开展挑战一线适应症的临床研究[44]。纳武利尤单抗Ⅱ期临床结果尚可[21,45],包括在亚裔人群中[46],但Ⅲ期临床失败,导致其HCC适应症被撤回[38](表2、3)。对不同的药物在CSCO免疫检查点*制剂抑**临床应用指南(2022版)[11]、原发性肝癌诊疗指南(2022年版)[12]、肝细胞癌免疫治疗中国专家共识(2021版)[13]中的证据等级对比见表4。
2 ICIs联合治疗进展
2.1 ICIs双药联合方案
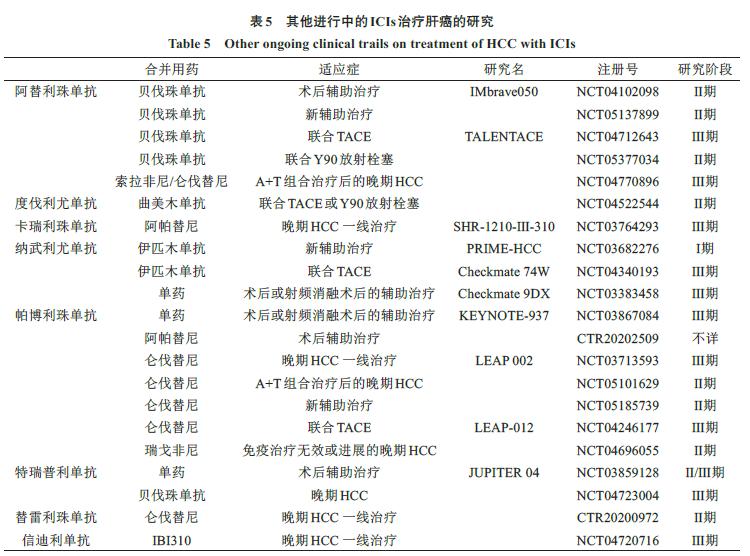
目前主要的双药组合为PD-1联合CTLA-4*制剂抑**,也有研究聚焦于LAG-3、TIGIT等。纳武利尤单抗联合伊匹木单抗(O+Y组合)是目前唯一获批的ICI双药联合,Ⅱ期研究取得较好结果(ORR为32%、OS为22.8个月)[21],尤其对于甲胎蛋白(AFP)<400 ng·mL-1的患者,mOS可达46.1个月[23]。度伐利尤单抗联合曲美木单抗[22](T+D组合),具有比O+Y组合更好的耐受性[24],Ⅲ期临床证实,T+D组合能够改善患者生存期(表3)[39],提高生活质量[47],且安全性良好[48]。国产双免组合信迪利单抗联合IBI310已进入Ⅲ期临床[25],其他值得期待的临床研究均总结于表5,可关注后续结果。
2.2 联合血管内皮生长因子*制剂抑**
抗血管生成是肝癌治疗的重要靶点[49-50]。阿替利珠单抗联合贝伐珠单抗(T+A组合)在Ⅰ期临床取得36%的ORR[26-27],且Ⅲ期临床疗效明显优于索拉非尼[40],长期随访的mOS达到19.2个月,中国亚组疗效更佳(mOS为24.0个月)[51]。信迪利单抗(达伯舒)联合贝伐珠单抗类似物IBI305(达攸同)又称“双达”组合,Ⅰ期结果与T+A组合相近,但耐受更好[28],Ⅱ/Ⅲ期临床试验结果同样优于索拉非尼[41]。目前,T+A组合和双达组合已被推荐为中晚期HCC的一线治疗。此外,国产PD-1单抗特瑞普利单抗联合贝伐珠单抗的Ⅲ期临床试验也已启动值得关注。
2.3 联合酪氨酸激酶*制剂抑**
仑伐替尼是一款多靶点TKI,临床前研究显示,仑伐替尼能够降低肿瘤PD-L1水平,提高抗PD-1疗效[52-53]。在I期临床中,帕博利珠单抗(可瑞达)联合仑伐替尼(乐卫玛)的“可乐”组合表现出较好疗效(ORR为36%、mOS为22个月,见表2)[29]。目前,评价“可乐”组合作为一线治疗的Ⅲ期临床正在开展[54-55],有望进一步扩大适应症。卡瑞利珠单抗(艾瑞卡)联合阿帕替尼(艾坦)的“双艾”组合在I期临床中获得了50%的ORR[30];Ⅱ期临床显示其作为一、二线治疗均有较好疗效[31-32](表2)。目前,该组合的Ⅲ期临床已达研究终点,结果尚未披露。此外,纳武利尤单抗联合仑伐替尼[56]及其他不同组合的多项研究正在进行中。
2.4 联合局部治疗
除中晚期HCC的系统性治疗外,免疫治疗也逐渐应用于HCC早中期。对可手术的患者可作为辅助或新辅助治疗,以减少复发。NIVOLVE研究证实,纳武利尤单抗作为术后或射频消融术后的辅助治疗可使1年无复发生存率提高至78.6%,且耐受性较好[57-58]。目前,纳武利尤单抗[59]、帕博利珠单抗[60]、特瑞普利单抗等单药方案作为辅助或新辅助治疗的研究均已进入Ⅲ期临床(表5)。此外,T+A组合[61]、O+Y组合[62]在辅助或新辅助治疗中的探索也已开展。
对中期HCC,以TACE为主的介入治疗通常是第一选择[63-64],而免疫治疗同样能起到协同增效的作用。纳武利尤单抗联合TACE在Ⅱ期临床中取得较好疗效(ORR为71.4%、mOS为7.2个月)[33];而O+Y组合[65]、T+A组合[66]和“可乐”组合[67]联合TACE的研究均进入Ⅲ期临床。除传统的TACE术式外,钇-90(Y90)放射栓塞也是中期HCC的可选治疗[68]。纳武利尤单抗、帕博利珠单抗与Y90联合治疗的可行性均已在Ⅱ期临床试验中得到验证[34-35]。
3 免疫细胞治疗进展
免疫细胞治疗,又称过继性免疫细胞治疗,是免疫治疗的重要领域之一,主要包括嵌合抗原受体T细胞(CAR-T)、T细胞受体(TCR)、工程T细胞(TCR-T)、肿瘤浸润淋巴细胞(TILs)等。但其应用在实体瘤治疗中尚处早期[69]。其中CAR-T和TCR-T前景较好[70-71]。
3.1 CAR-T治疗
CAR-T的原理是通过细胞工程在T细胞表面表达可识别肿瘤抗原并激活T细胞的嵌合抗原受体,使T细胞发挥识别并*伤杀**肿瘤细胞的作用。目前,多项基础研究已证实CAR-T对肝癌的作用[72-73]。相关的临床研究已在晚期、经治的HCC患者中开展,mOS为9~12个月[74-75]。然而,肝癌的异质性使得能作为CAR-T靶标的肿瘤抗原较少。其次,肿瘤内部的抑制性免疫微环境可能阻碍CAR-T功能[76],肝脏的免疫耐受性则使情况尤为复杂,通过基因编辑敲除CAR-T中的PD1或CTLA-4[77-78]有望突破这一瓶颈,然而CAR-T的安全和耐受性仍是其应用于临床最需解决的问题。
3.2 TCR-T
不同于CAR-T细胞,TCR-T识别的是MHC的抗原肽,这使得TCR-T在乙型肝炎病毒(HBV)感染相关的HCC中更有优势[79]。由于HBV的基因片段在慢性感染期间整合进入肝细胞的染色体中[80],因此工程化的TCR能够靶向HCC细胞中的HBV抗原已得到基础研究的证实[81-82]。临床研究显示TCR-T能够缩小人HCC的肺转移灶[83]。另1项研究显示,HCC肝移植患者的免疫抑制治疗不影响TCR-T的活性[84],这意味着TCR-T有可能在HCC治疗中发挥更大作用。
3.3 TILs治疗
TILs是肿瘤中浸润的多种淋巴细胞的统称,其中部分细胞亚群具有抗肿瘤活性,但在体内受调节性T细胞(Treg)等抑制[85]。TILs治疗通常是从肿瘤样本中分离TILs,在体外进行激活和扩增,最后回输体内进行治疗。临床前研究显示寡克隆TILs具有较高的抗肿瘤活性,且与Treg比例呈负相关[86];1项Ⅰ期临床研究提示,活化和扩增的自体TILs在HCC患者中可能取得不错的治疗效果[87]。总体上来说,TILs治疗在HCC中研究较少,这可能与肝癌较低的免疫原性和抑制性免疫微环境相关。
3.4 其他免疫细胞治疗
除T细胞外,自然*伤杀**细胞(NK)和树突状细胞(DC)也是免疫细胞治疗的研究热点[88]。与T细胞类似,NK细胞同样可以通过CAR激活,有个案报告了CAR-NK对HCC的疗效,患者在接受了17个疗程的治疗后,生存期达到了4年以上[89]。与CAR-T比较,CAR-NK的优势在于安全性较好,特别是细胞因子释放综合征发生率较低,但现有研究还不够深入。
DC细胞治疗的特殊性在于其主要是通过向DC细胞加载肿瘤抗原,刺激抗原呈递而间接发挥抗肿瘤作用,因此又被称为“DC肿瘤疫苗”[90]。现有的几项临床研究证实DC肿瘤疫苗的疗效和安全性,晚期HCC患者中的mOS为7~13个月[91-93]。目前,DC细胞治疗的短板在于DC细胞的自然丰度低、离体增殖能力差。此外,如何选择最佳的肿瘤抗原、高效地激活T细胞,也是后续要解决的问题[94]。
4 结语
随着免疫治疗在肝细胞癌中逐步开展,HCC系统治疗迎来了重大变革。免疫治疗策略由单药过渡到多药联合,以“T+A”为代表的联合方案,和以“可乐组合”为代表的靶向免疫方案,均表现出较好的生存获益,为晚期HCC患者带来希望。在多学科联合的趋势下,特别是内科与外科联合治疗的策略下,免疫治疗的发展空间将更为广阔。从晚期HCC的2、3线治疗,到中期HCC联合血管介入治疗,再到早期HCC进行术后辅助治疗或术前新辅助治疗,免疫治疗将有更广阔的应用前景。在药物研发方面,开发不同的免疫检查点,或通过不同组合多靶点治疗,都是未来的研究方向。
HCC的免疫治疗也仍有诸多问题亟待解决。由于肝癌在病因学上的复杂性,是否合并肝炎病毒感染、是否合并代谢性肝病等,都会造成HCC免疫微环境的改变,从而影响免疫治疗的效果[95-96]。因此,针对患者的分层分析及精准用药是将来HCC免疫治疗研究的重点和难点。在基础研究中,对不同类型肝癌免疫细胞亚群和微环境的深入认识,进行相关生物标志物的研发,将为临床优势人群的确立提供帮助。在新药研发中,减少同质化和重复研发,充分利用祖国医学资源宝库,基础与临床研究相结合,才能让国内科研工作者领跑在免疫治疗的赛道上。
利益冲突 所有作者均声明不存在利益冲突
参考文献(略)
来 源:李靖华,杨丽惠,胡凯文,王婧筱.肝细胞癌免疫治疗临床研究进展 [J]. 药物评价研究, 2022, 45(9): 1725-1734 .