
瑞德西韦是否能成为“特效药”的希望?
BE / EVENT

新型冠状病毒(2019-nCoV)造成的肺炎疫情发展到今天,「瑞德西韦 」(Remdesivir)这个词从2月开始频繁出现在大家的讨论中,这个早在2018年就曾作为抗击埃博拉病毒的新药,如今会不会成为对新冠肺炎具备特效的药物?成了千千万万人目前最关心的问题之一。
关于「瑞德西韦 」(Remdesivir)我们知道多少,瑞德西韦背后的吉利德(Gilead)科学公司又是什么来头,BE把相关重点信息做了检索和罗列。

瑞德西韦什么时候火的? 2019-nCoV
1月24日,上海市公共卫生临床中心*党**委书记卢洪洲发文提到了包括瑞德西韦在内的若干潜在药物,并认为从目前的研究数据看,瑞德西韦可能是最具潜力的抗新冠药物。
1月25日,中国科学院上海药物研究所和上海科技大学免疫化学研究所抗2019-nCoV病毒感染联合应急攻关团队筛选出了30种具备治疗潜力的药物,其中第六项就是瑞德西韦。
1月28日,中国科学院武汉病毒研究所与军事医学科学院毒物药物研究所联合宣布发现了三种已有药物在细胞层面上对新型冠状病毒有较好抑制作用,包括瑞德西韦。

所以,早在1月底,瑞德西韦就已经频繁上榜专家筛选的各个名单,不过真正让瑞德西韦“一夜爆火”的,是1月31日一篇发表在《新英格兰医学杂志》(NEJM)上、记录美国首例新型冠状病毒肺炎患者治疗过程的论文。该患者在住院第7天接受了瑞德西韦静脉输注,次日即退烧、不再需要吸氧,症状只剩下干咳和流涕。

2020年1月31日新英格兰医学杂志在线发表论文
但需要注意的是该研究并未提供前后的外周血病毒载量数据变化,仅有鼻咽/口咽拭子病毒 RNA 数据,不能下判断说症状的减轻和瑞德西韦有直接的关系 ,而且作为孤例也无法证明有广泛适用性,但无可置疑这的确给新冠肺炎的治疗带来了曙光。
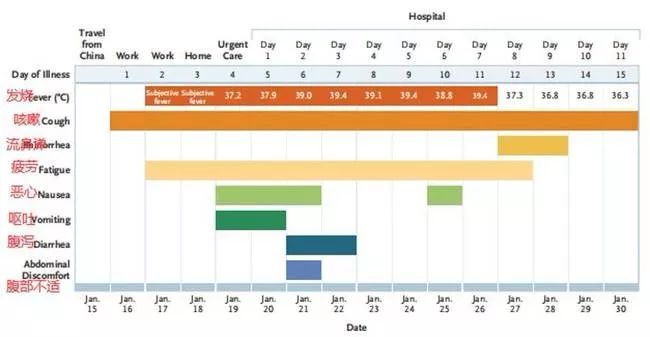
上图记录了1月15日-1月30日美国患者的发病情况
瑞德西韦这个药是怎么来的? 2019-nCoV
这种药物名为瑞德西韦(Remdesivir),为经过改造的核苷酸类似物,主要作用于RNA病毒的RNA聚合酶,使其不能正常发挥作用,从而抑制RNA病毒的复制。
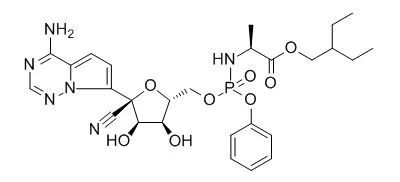
瑞德西韦分子式 | https://file.medchemexpress.com
瑞德西韦由美国生物制药巨头——吉利德科学(GileadSciences)公司研发,原本主要用于治疗埃博拉患者。但是据2019年12月18日《新英格兰医学杂志》公布的一项临床试验报告显示,该临床试验招募了近700名患者,从2018年11月到2019年9月试用了瑞德西韦等四种药物,结果采用瑞德西韦的实验组死亡率高达53%,为四种实验新药最高,而另外两种药物的死亡率可降至30%左右。就这样,瑞德西韦作为抗埃博拉新药的希望宣告破灭。
不过,吉利德公司并没有将瑞德西韦吊死在埃博拉病毒这一棵树上。从两年前开始,吉利德公司的研究人员通过体外细胞试验和体内动物实验陆续发现,瑞德西韦对SARS冠状病毒、MERS冠状病毒、动物源冠状病毒及尼帕病毒等多种RNA病毒具有显著的抗性。
据2020年1月10日《自然通讯》杂志的一篇研究论文,小鼠试验显示,作为预防性和治疗*药性**物,瑞德西韦均可显著降低小鼠肺部的MERS冠状病毒载量,显著改善实验动物的肺功能和严重的肺部症状。
直到2020年2月4日,中国科学院武汉病毒研究所等机构的研究人员在《细胞研究》报道称,他们通过体外细胞试验发现,瑞德西韦与氯喹(抗疟疾特效药)联合使用,可显著抑制人体细胞的新型冠状病毒感染,建议开展临床试验进一步评价这一药物组合的疗效。

2月5日,瑞德西韦临床试验项目负责人、
中日友好医院副院长曹彬教授讲解项目内容
新华社记者程敏摄
瑞德西韦背后的吉利德(GILEAD)科学公司是什么来头? 2019-nCoV
吉利德并非家喻户晓的制药巨擘,但在抗病毒领域展现过足够的实力。这个有着11000的人的生物科技公司,在抗艾滋病,丙肝,以及乙肝方面,都有出色的表现。
2001年,吉利德首个抗艾滋病药物替诺福韦(Viread)上市,至今仍是应用最广泛的抗逆转录药物之一。2013年,吉利德推出丙肝特效药索非布韦(Solvadi),被誉为当年FDA批准的最重磅药物。
此外,抗流感明星药品达菲(Tamiflu)最早由吉利德发现,在后期实验阶段才转让给罗氏。仅用了30年时间,吉利德一度跻身全球十大药企之列。
吉利德科学是很厉害的存在,厉害到能把很多病毒治疗到绝迹,且几乎无副作用,而后果就是公司的收入在不断下降,因为患者是越来越少的。显然,如果这次临床试验有满意的结果,瑞德西韦能够顺利上市,吉利德会打造出另一款“达菲”,再次演绎原研药高投入、高风险、高回报的神话。

瑞德西韦对新冠病毒的临床试验目前有什么进展? 2019-nCoV
新型冠状病毒肺炎疫情发生后,吉利德公司迅速行动,希望能让瑞德西韦在治疗新型冠状病毒肺炎患者中展现积极疗效。除了在美国华盛顿州治疗首例患者之外,吉利德公司还与中国相关医疗机构密切合作,由于瑞德西韦已完成证明人体安全性的的临床I和II试验(治疗埃博拉),因此计划直接开展临床III试验。
5日下午,中日友好医院王辰、曹彬团队在武汉市金银潭医院宣布启动瑞德西韦治疗2019新型冠状病毒感染研究。正式开始进入临床试验。按计划,该试验将入组轻、中症患者308例,重症患者453例。中日友好医院曹彬教授介绍说,这项研究将执行严格的随机双盲。
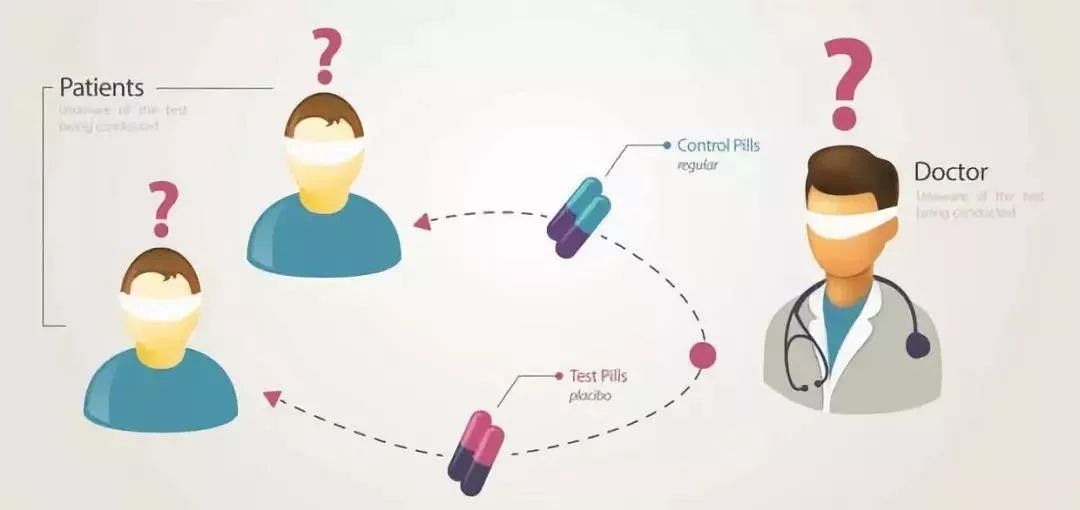
什么是双盲?双盲是实验中极重要的环节。指随机把病人分实验组和对照组,前者吃药,后者吃“药”(实际是维他命或者淀粉药丸等安慰剂),病人和医生都不知道病人所属的组别。这样能减少人为干扰、偏见和无意识暗示。实验结束后通过对比两组,统计上看出吃药究竟有没有更好或更差或没区别。试验预期于4月底结束,届时,该药物是否安全、能否被推广等结论会更清晰。
瑞德西韦能否在挽救新型冠状病毒肺炎患者生命的同时,从对抗埃博拉病毒的失败阴影中“起死回生”,非常值得期待。
一般新药从临床试验到正式用药需多久? 2019-nCoV
新药研发是一个漫长的过程,从药物筛选到上市,一般需要经过10年甚至更长的时间。一般来说步骤如下:
1、早期研发;包括发现靶标、了解机理等,花费时间不等。这些瑞德西韦早就完成了。
2、临床前研发;包括体外、体内安全性和活性;体外有酶水平、细胞水平等;体内有各种层次的动物。瑞德西韦针对其他适应症也在以前完成了,但针对新冠肺炎这个病,武汉病毒所完成了这个部分。
3、注册申报(向国家药监局提交申请)分2阶段:临床申请;临床分I、II、III期(大部分药是需要5年的);临床结束或基本结束,就进行报产申请。瑞德西韦从2020年2月2日受理,到2020年2月4日获得临床批件,只用了3天时间,符合药品特别审批程序,显示我们政府部门在应对重大突发公共卫生事件高效的工作效率和协同机制。
4、批准上市后,企业进行生产。特殊时期,吉利德公司正在采取多种措施加快生产进度,增加 瑞德西韦的库存 供应,以备不时之需。

瑞德西韦的临床试验计划官网预计完成时间为2020年4月27日
什么叫同情用药?瑞德西韦可以申请同情用药吗?2019-nCoV
同情给药有2个要求:
1、有部分数据证明药物极有可能有效(未上市的药物);
2、市场现有治疗手段无有效或无更好的药物/手段治疗。
患者没在临床试验入组,但是又急需这个药,就允许在开展临床试验的机构内使用给急需的患者。美国第一例新冠肺炎患者就动用了“同情用药”原则,当然这需要承担巨大的风险。
如果同情用药的口开的太大,容易让整个药物研发开发和审批的流程彻底失败,因为任何患者和医生都有可能在焦急的情况下尝试任何有可能有用的药物。
所以“同情用药”的约束非常多,每年只会批准1000多个患者提出申请,不过这个数字,相比每年超过10亿人次求医问药来说,范围可以小到忽略不计。


经过十昼夜的奋战,2月6日,
雷神山医院开展验收工作并逐步移交。
而目前吉利德公司赠送的药物,一部分用来抢救病情危重的新冠肺炎患者(中国药监局已经在2017年通过中国版同情用药方案,此操作有章可循),另一部分用来开展正规的人体临床试验,尽快确定它是否对于新冠病毒肺炎患者安全和有效。
如果效果确实安全好用,就可以大大拓展这种药物的使用范围,使更多患者受益,如果效果不好,则第一时间获知风险,及时叫停“同情用药”。
除了瑞德西韦,我们还能对哪些药有所期待?2019-nCoV
2 月 4 日的新闻显示,李兰娟院士团队发现阿比朵尔和达芦那韦对新冠肺炎显示出了良好的抑制效果,并且这两种药物已经开始在部分地区进行使用,并准备之后替代部分效果不佳的药物。
至于之前显示出一定效果的抗 HIV 药物克力芝(洛匹那韦/利托那韦)虽然取得不错效果,但在后续试验中表现并不好,且对肝脏有一定的毒副作用。

2020年1月31日,
中山大学医学院郭旭舜团队在bioRxiv 在线发表题为
“Molecular ModelingEvaluation of the Binding Abilities of Ritonavir and Lopinavir to WuhanPneumonia Coronavirus Proteases”的研究论文
希望瑞德西韦临床试验能够顺利进行,随着治疗方法的改进,目前治愈患者的数量已经开始迅速上升。作为个人,戴口罩勤洗手少出门,减少自己患病的可能就是做到最大的贡献了。
参考文献
[1] Bekker LG, Tatoud R, Dabis F.The complex challenges of HIV vaccine development require renewed and expandedglobal commitment. Lancet. 2020, 395(10221):384-388. doi:10.1016/S0140-6736(19)32682-0.
[2] First FDA-approved vaccine forthe prevention of Ebola virus disease, marking a critical milestone in publichealth preparedness and response.
[3] fda.gov/news-events/pre.
[4] Song Z, Xu Y, Bao L, et al.From SARS to MERS, Thrusting Coronaviruses into the Spotlight. Viruses. 2019,11(1). pii: E59. doi: 10.3390/v11010059.
[5] Yong CY, Ong HK, Yeap SK, HoKL, Tan WS. Recent Advances in the Vaccine Development Against Middle EastRespiratory Syndrome-Coronavirus. Front Microbiol. 2019, 10:1781. doi:10.3389/fmicb.2019.01781.
[6] Modjarrad K, Roberts CC, MillsKT, et al. Safety and immunogenicity of an anti-Middle East respiratorysyndrome coronavirus DNA vaccine: a phase 1, open-label, single-arm,dose-escalation trial. Lancet Infect Dis. 2019, 19(9):1013-1022. doi:10.1016/S1473-3099(19)30266-X.
[7] Michelle L. Holshue, ChasDeBolt, Scott Lindquist, et al. First Case of 2019 Novel Coronavirus in theUnited States. 2020, January 31, DOI: 10.1056/NEJMoa2001191.
[8] Mulangu S, Dodd LE, Davey RTJr, et al. A Randomized, Controlled Trial of Ebola Virus Disease Therapeutics.N Engl J Med. 2019 Dec 12;381(24):2293-2303. doi: 10.1056/NEJMoa1910993.
[9] Sheahan TP1, Sims AC2, Leist SRet al. Comparative therapeutic efficacy of remdesivir and combinationlopinavir, ritonavir, and interferon beta against MERS-CoV. Nat Commun. 2020Jan 10;11(1):222. doi: 10.1038/s41467-019-13940-6.
[10] Wang, M., Cao, R., Zhang, L. etal. Remdesivir and chloroquine effectively inhibit the recently emerged novelcoronavirus (2019-nCoV) in vitro. Cell Res. 2020. doi.org/10.1038/s41422-.
[11] Peter Richardson, Ivan Griffin,Catherine Tucker et al. Baricitinib as potential treatment for 2019-nCoV acuterespiratory disease. 2020. DOI:doi.org/10.1016/S0140-630304-4.
[12] Bo Ram Beck, Bonggun Shin,Yoonjung Choi, Sungsoo Park, Keunsoo Kang. Predicting commercially availableantiviral drugs that may act on the novel coronavirus (2019-nCoV), Wuhan, Chinathrough a drug-target interaction deep learning model. bioRxiv2020.01.31.929547; doi: doi.org/10.1101/2020.01
[13]国内媒体:澎湃新闻、知乎以及凤凰网