作者:中华医学会 中华医学会杂志社 中华医学会消化病学分会 中华医学会全科医学分会 中华医学会《中华全科医师杂志》编辑委员会 消化系统疾病基层诊疗指南编写专家组
通讯作者:吕宾,浙江中医药大学附属第一医院消化科;陈卫昌,苏州大学附属第一医院消化科
本文刊于:中华全科医师杂志, 2020,19(09) :776-782
一、概述
(一)定义
慢性胃炎(chronic gastritis)是由多种病因引起的胃黏膜慢性炎症或萎缩性病变。本质是胃黏膜上皮反复受到损害使黏膜发生改变,最终导致不可逆的胃固有腺体的萎缩,甚至消失。该病易反复发作,不同程度地影响患者生命质量。
(二)流行病学
慢性胃炎是基层消化内科门诊最常见的疾病,大多数慢性胃炎患者缺乏典型临床表现,因此在自然人群中的确切患病率难以获得。慢性胃炎发病率在不同国家与地区之间存在较大差异,其发病率与幽门螺杆菌(Helicobacter pylori,Hp)感染的流行病学重叠[1],并随年龄增长而增加[2]。
(三)分类
1.基于病因分类:
分为Hp胃炎和非Hp胃炎。病因分类有助于慢性胃炎的治疗[3,4]。
2.基于内镜和病理诊断分类:
分为萎缩性和非萎缩性两大类。
3.基于胃炎分布分类:
分为胃窦为主胃炎、胃体为主胃炎和全胃炎三大类。胃体为主尤其伴有胃黏膜萎缩者,发生胃癌的风险增加;胃窦为主者胃酸分泌增多,发生消化性溃疡的风险增加。
4.特殊类型胃炎的分类:
包括化学性、放射性、淋巴细胞性、肉芽肿性、嗜酸细胞性以及其他感染性疾病所致。
二、病因和发病机制
(一)病因、诱因或危险因素
1.Hp感染:
是慢性胃炎最主要的原因。
2.饮食和环境因素:
进食过冷、过热以及粗糙、刺激性食物等不良饮食习惯。
3.自身免疫:
自身免疫性胃炎在北欧多见,我国少有报道。
4.其他因素:
胆汁反流、抗血小板药物、非甾体消炎药(NSAIDs)等药物、酒精等外在因素也是慢性胃炎相对常见的病因。其他感染性、嗜酸性粒细胞性、淋巴细胞性、肉芽肿性胃炎和其他自身免疫性疾病累及所致的胃炎比较少见。
(二)发病机制
1.Hp感染:
Hp具有鞭毛,能在胃内穿过黏液层移向胃黏膜,其释放尿素酶分解尿素产生氨、分泌空泡毒素A等物质而引起细胞损害;细胞毒素相关基因蛋白能引起强烈的炎症反应;其菌体胞壁还可作为抗原诱导免疫反应。这些因素可导致胃黏膜的慢性炎症[5]。
2.十二指肠-胃反流:
各种原因引起的胃肠道动力异常、肝和胆道疾病及远端消化道梗阻,长期反流削弱胃黏膜屏障功能。
3.药物和毒物:
服用NSAIDs或阿司匹林可通过直接损伤胃黏膜或抑制前列腺素等的合成导致胃黏膜损伤,从而导致慢性胃炎甚至消化道出血的发生。摄入酒精可引起胃黏膜损伤,甚至糜烂、出血。
4.自身免疫:
体内产生针对胃组织不同组分的自身抗体,如抗内因子抗体(致维生素B12吸收障碍)、抗壁细胞抗体(破坏分泌胃酸的壁细胞),造成相应组织破坏或功能障碍[6]。
5.年龄和饮食环境:
老年人胃黏膜出现退行性改变、修复再生功能降低,上皮增殖异常及胃腺体萎缩。高盐饮食、缺乏新鲜蔬菜水果、摄入过多硝酸盐和亚硝酸盐、微量元素比例失调也与胃黏膜萎缩、肠化有关。
三、诊断、鉴别诊断与转诊
(一)诊断
胃镜及活检组织病理学检查是慢性胃炎诊断和鉴别诊断的主要手段。
1.临床表现:
慢性胃炎无特异性临床表现,多数无明显症状,有症状者主要表现为上腹痛、腹胀、早饱感、嗳气等消化不良表现[7],部分还伴焦虑、抑郁等精神心理症状,心理因素往往加重患者的临床症状[8]。
症状的严重程度与内镜所见及病理组织学分级并不完全一致。自身免疫性胃炎可长时间缺乏典型临床症状,首诊症状常以贫血和维生素B12缺乏引起神经系统症状为主[9]。
2.内镜检查:
上消化道内镜检查是诊断慢性胃炎的最主要方法,对评估慢性胃炎的严重程度及排除其他疾病具有重要价值。
慢性非萎缩性胃炎内镜下可见黏膜红斑、粗糙或出血点,可有水肿、充血、渗出等表现;慢性萎缩性胃炎内镜下表现为黏膜红白相间,白相为主,皱襞变平、血管透见、伴有颗粒或结节状[10]。
放大内镜结合色素染色、电子染色能清楚地显示胃黏膜微小结构,可指导活检部位,对胃炎的诊断和鉴别诊断及早期发现上皮内瘤变和肠化具有参考价值[11]。放大内镜下慢性萎缩性胃炎具有特征性改变,表现为胃小凹增宽、分布稀疏等。
3.病理组织学检查[12]:
对慢性胃炎的诊断至关重要,应根据病变情况和需要进行活检。
临床实践时可取2~3块,分别在胃窦、胃角和胃体部位活检。病理切片的观察内容有5种组织学变化和4个分级,5种组织学变化即Hp感染、慢性炎症反应(淋巴细胞、浆细胞和单核细胞浸润)、活动性(中性粒细胞浸润)、萎缩(固有腺体减少)及肠化,4个分级为无、轻度、中度和重度4级(0、+、++、+++)。临床医师可结合病理结果和内镜所见做出病变范围与程度的判断。
慢性胃炎可操作的与胃癌风险联系的胃炎评估(Operative Link for Gastritis Assessment,OLGA)/可操作的与胃癌风险联系的肠化生评估(Operative Link on Gastric Intestinal Metaplasia Assessment,OLGIM)系统是胃黏膜炎性反应和萎缩/肠化生程度及范围的分级、分期标准,其基于胃炎新悉尼系统对炎症和萎缩/肠化生程度的半定量评分方法,采用胃炎分期代表胃黏膜萎缩范围及程度,将慢性胃炎的组织病理学与癌变危险性联系起来,为临床医生预测病变进展和制定疾病管理措施提供更为直观的信息[13],见表1、表2。
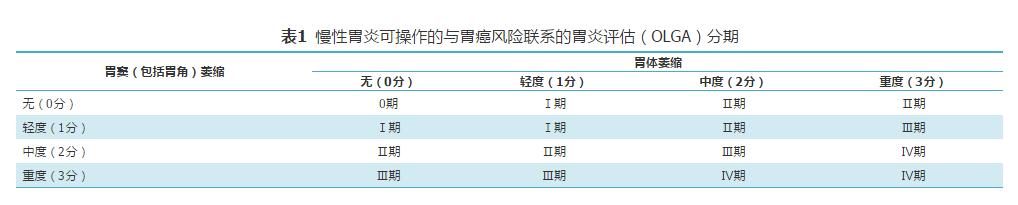
表1 慢性胃炎可操作的与胃癌风险联系的胃炎评估(OLGA)分期
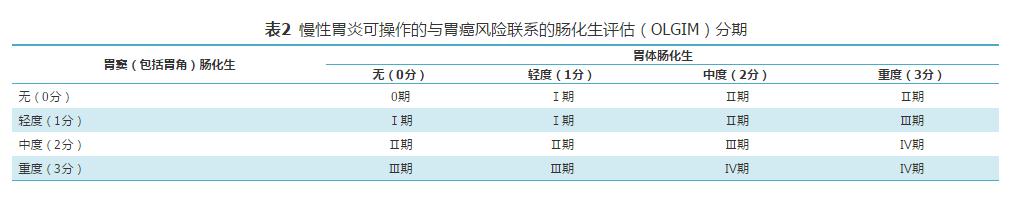
表2 慢性胃炎可操作的与胃癌风险联系的肠化生评估(OLGIM)分期
4.实验室检查:
(1)Hp检测:慢性胃炎患者建议常规检测。常用的Hp检测方法分侵入性和非侵入性方法。侵入性方法需要通过胃镜获取胃黏膜标本进行检测,主要包括快速尿素酶试验、胃黏膜组织切片染色镜检及Hp培养等。非侵入性方法以13C-或14C-尿素呼气试验为首选,是评估根除治疗后结果的最佳方法,目前已广泛应用,但需避免抗菌药物、铋剂、抑酸药物的干扰;单克隆粪便抗原试验可作为备选;血清学试验只用于特殊情况,如流行病学调查、消化性溃疡出血、胃黏膜相关淋巴组织(MALT)淋巴瘤、严重的胃黏膜萎缩。
(2)胃蛋白酶原(pepsinogen,PG)Ⅰ、Ⅱ以及胃泌素-17(gastrin-17,G-17)检测:有助于慢性萎缩性胃炎的诊断。PGⅠ、PGⅠ/PGⅡ比值降低,血清G-17水平升高,提示胃体萎缩为主;若PGⅠ及PGⅠ/PGⅡ比值正常,血清G-17水平降低,提示胃窦萎缩为主;全胃萎缩者,PG及G-17均降低。
(3)血清抗壁细胞抗体、抗内因子抗体及维生素B12水平测定:有助于诊断自身免疫性胃炎。
(二)鉴别诊断
慢性胃炎患者可出现上腹部不适、疼痛、反酸、腹胀等消化不良症状,需要与消化性溃疡、胃癌、慢性胆囊炎、胆结石以及肝、胰腺疾病相鉴别。消化性溃疡常表现为上腹部疼痛,具有周期性、节律性的特点,常伴反酸;胃癌早期往往无明显症状,进展期可出现上腹部痛、呕吐、黑便,甚至呕血;胆囊结石患者常于餐后、夜间发生右上腹痛,涉及背部,呈发作性。
胃镜、肝胆胰超声、腹部CT或磁共振、血液生化检查、肿瘤标志物等有助于诊断和鉴别,对于出现纳差、体重减轻、贫血、呕血或黑便、黄疸等报警征象,尤其是45岁以上、新近出现症状,或症状加重者应及时进行上述检查。
(三)并发症
1.上消化道出血:
慢性胃炎伴有胃黏膜糜烂时可以出现黑便,甚至呕血。
2.胃癌:
慢性胃炎,尤其是伴有Hp持续感染者,少数可逐渐出现萎缩、肠化、异型增生,有一定的胃癌发生风险。胃体为主的萎缩性胃炎,尤其是程度严重者,胃癌发生风险显著增加[14]。
3.消化性溃疡:
胃窦为主的常有较高的胃酸分泌水平,易发生十二指肠溃疡;胃体为主的胃黏膜屏障功能下降,发生胃溃疡的可能增加。
(四)诊断流程
慢性胃炎患者常无临床症状,有症状也缺乏特异性,因此难以通过临床表现进行诊断,确诊必须依靠胃镜及胃黏膜病理学检查,尤以后者的价值更大。特殊类型胃炎的内镜诊断需要结合病因和病理。诊断流程见图1。
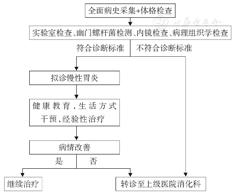
图1 慢性胃炎的基层诊断流程
(五)病情评估
对慢性胃炎患者应评估其病因和类型、病理组织学诊断、心理和睡眠情况等,以帮助制定个体化的治疗和随访方案。
(六)转诊建议
1.普通转诊:
(1)对经验性治疗反应不佳,症状没有得到明显改善的患者。
(2)需要排除器质性、系统性或代谢性疾病引起的消化不良症状的患者。
(3)需行内镜微创治疗或外科手术治疗者。
2.紧急转诊:
有纳差、体重减轻、贫血、呕血或黑便等报警征象者。
四、治疗
治疗的目标是去除病因、缓解症状、改善胃黏膜组织学、提高生命质量、预防复发和并发症。
(一)生活方式干预
宜清淡饮食,避免刺激、粗糙食物,避免过多饮用咖啡、大量饮酒和长期吸烟。对于需要服用抗血小板药物、NSAIDs的患者,是否停药应权衡获益和风险,酌情选择。
(二)药物治疗:
应根据患者的病因、类型及临床表现进行个体化治疗。增加黏膜防御能力,促进损伤黏膜愈合是治疗基础。
1.对因治疗:
(1)Hp阳性慢性胃炎:根除Hp有利于胃黏膜的修复,显著改善胃黏膜炎性反应,阻止或延缓胃黏膜萎缩、肠化的发生和发展,甚至有可能部分逆转萎缩。目前推荐根除治疗方案为铋剂四联方案:质子泵*制剂抑**(PPI)+铋剂+2种抗菌药物,疗程为10 d或14 d,停药1个月后复查。需要注意的是,Hp对克拉霉素、甲硝唑和左氧氟沙星的耐药率(包括多重耐药率)高,而对阿莫西林、四环素和呋喃唑酮的耐药率仍很低。我国多数地区为抗菌药物高耐药地区,推荐经验性铋剂四联治疗方案疗程为14 d,除非当地的研究证实10 d治疗有效(根除率>90%)[15,16]。
(2)伴胆汁反流的慢性胃炎:可应用促动力药和/或有结合胆酸作用的胃黏膜保护剂。促动力药物如多潘立酮(10 mg/次、3次/d)、莫沙比利(5 mg/次、3次/d)等;铝碳酸镁(1 g/次、3~4次/d)可以结合胆汁酸,增强胃黏膜屏障,减轻或消除胆汁反流所致胃黏膜损伤。熊去氧胆酸可以降低胆汁内其他的胆汁酸,缓解胆汁酸对细胞的毒性,对胃黏膜起保护作用[17]。
(3)药物相关性慢性胃炎:首先根据患者使用药物的治疗目的评估患者是否可停相关药物;对于必须长期服用的患者应进行Hp检测,阳性者应进行Hp根除治疗,并根据病情或症状严重程度加强抑酸和胃黏膜保护治疗。PPI是预防和治疗NSAIDs相关消化道损伤的首选药物,优于H2受体*制剂抑**(H2RA)和胃黏膜保护剂[18]。常用的PPI有奥美拉唑、兰索拉唑、泮托拉唑、艾司奥美拉唑、雷贝拉唑、艾普拉唑等。应避免长期服用,并注意PPI的不良反应[19]。
2.对症治疗:
(1)以上腹部灼热感或上腹痛为主要症状者,可根据病情或症状严重程度选用PPI或H2RA、抗酸剂、胃黏膜保护剂。胃黏膜保护剂是慢性胃炎治疗的基础,如硫糖铝、铝碳酸镁、替普瑞酮、瑞巴派特片等[20]。
(2)以上腹饱胀、嗳气、早饱、恶心等为主要表现时,可选择促动力药物如莫沙必利、伊托必利等[21]。与进食相关的中上腹部饱胀、纳差等可应用消化酶,如米曲菌胰酶片、复方阿嗪米特肠溶片、复方消化酶等。消化酶联合促动力药效果更为明显。
(3)伴焦虑、抑郁等精神心理因素、常规治疗无效和疗效差的患者可给予抗抑郁药物或抗焦虑药物[22]。如焦虑抑郁症状比较明显,应建议患者就诊精神卫生专科。
3.中医药及其他治疗:
中医治疗胃炎有一定的效果,但需辨证施治,目前缺乏高质量的临床研究证据;针灸治疗对慢性胃炎的症状改善有作用,用温灸配合艾灸,可有效缓解慢性胃炎脾胃虚寒证患者的症状,适用于基层临床工作者[23]。
五、疾病管理
(一)管理流程
慢性胃炎患者基层管理流程见图2。
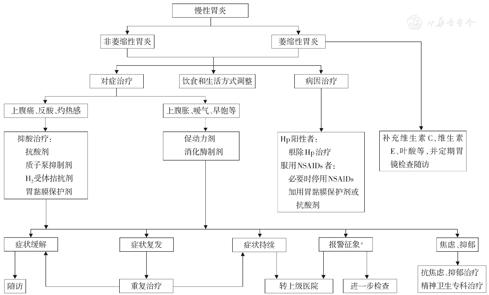
图2 慢性胃炎患者基层管理流程
(二)筛查
慢性胃炎症状无特异性,阳性体征少,仅根据临床表现难以与消化性溃疡、胃癌、肝胆胰腺疾病等鉴别。如果近期出现进行性加重的消化不良症状、吞咽困难、消瘦、黑便、贫血、腹部肿块、黄疸、水肿等症状体征时需要做胃肠镜检查,包括相关的实验室检查或影像学检查,排查器质性、系统性或代谢性疾病。
初步筛查方法包括外周血常规、尿常规、粪便常规+潜血、肝肾功能、血糖、甲状腺功能、ESR、CRP、肿瘤标志物[CA199、CA125、癌胚抗原(CEA)、甲胎蛋白(AFP)]以及腹部超声、胃肠镜检查等。
(三)随访评估
1.全面病史评估,评估疾病诊治及症状复发情况,生活方式改善情况,应重视和警惕原发病不能解释的新发症状,以及治疗效果不佳的顽固病例,必要时转诊。
2.评估Hp感染状态,对于已行根除治疗者要行13C-或14C-尿素呼气试验判断根除成功与否。
3.血清PGⅠ、PGⅡ以及G-17的检测,结合抗Hp抗体有助于胃癌风险分层,辨识出高危个体进行胃镜检查。
4.对于活检病理中有中-重度萎缩并伴有肠化生的慢性萎缩性胃炎应1年左右随访1次胃镜[24]。
5.伴有低级别上皮内瘤变并证明标本并非来于癌旁者,根据内镜和临床情况缩短至6个月左右随访1次;而高级别上皮内瘤变需立即确认,证实后行内镜下治疗或手术治疗。
六、预防与健康教育
(一)一级预防
在一般人群中开展健康教育,避免暴饮暴食、辛辣刺激食物,少吃熏制、腌制、富含亚硝酸盐和硝酸盐的食物;避免长期大量饮酒、吸烟;保持良好心理状态,生活规律,保证充足的睡眠。提倡公筷及分餐制减少感染Hp的机会。
(二)二级预防
对于慢性萎缩性胃炎、肠上皮化生、异型增生者及一级亲属中患有胃癌的危险人群纳入管理,定期随访。对于低叶酸水平患者,可适量补充叶酸,改善慢性萎缩性胃炎的状态。Hp感染者应给予根除治疗,并遵医嘱复诊,情况允许时慎用对胃黏膜有损伤的药物。对于符合转诊条件的患者,应及时转诊上级医院。
(三)三级预防
针对慢性胃炎患者指导合理用药,控制症状。对于伴有上皮内瘤变或早期癌变者,需内镜下治疗,伴有中重度萎缩和肠化生或上皮内瘤变者要定期内镜检查随诊。
七、预后
预后取决于病因。经治疗后大多数患者症状会减轻,但复发很常见。部分萎缩性胃炎可以改善或逆转;肠上皮化生通常难以逆转;轻度异型增生可以逆转,但重度者易转变为胃癌。
《基层医疗卫生机构常见疾病诊疗指南》项目组织委员会:
主任委员:饶克勤(中华医学会)
副主任委员:于晓松(中国医科大学附属第一医院);祝墡珠(复旦大学附属中山医院)
委员(按姓氏拼音排序):迟春花(北京大学第一医院);杜雪平(首都医科大学附属复兴医院月坛社区卫生服务中心);龚涛(北京医院);顾湲(首都医科大学);何仲(北京协和医学院);胡大一(北京大学人民医院);江孙芳(复旦大学附属中山医院);姜永茂(中华医学会);施榕(上海中医药大学);王爽(中国医科大学附属第一医院);魏均民(中华医学会杂志社);吴浩(北京市丰台区方庄社区卫生服务中心);曾学军(北京协和医院);周亚夫(南京医科大学)
秘书长:刘岚(中华医学会杂志社);郝秀原(中华医学会杂志社)
消化系统疾病基层诊疗指南制定学术指导委员会成员(按姓氏拼音排序):白文元(河北医科大学第二医院);陈东风(重庆市大坪医院);陈旻湖(中山大学附属第一医院);陈其奎(中山大学孙逸仙纪念医院);陈卫昌(苏州大学附属第一医院);房静远(上海交通大学医学院附属仁济医院);郭晓钟(北部战区总医院);李景南(北京协和医院);李鹏(首都医科大学附属北京友谊医院);李延青(山东大学齐鲁医院);刘玉兰(北京大学人民医院);陆伟(天津市第二人民医院);吕宾(浙江中医药大学附属第一医院);吕农华(南昌大学第一附属医院);钱家鸣(北京协和医院);唐承薇(四川大学华西医院);田德安(华中科技大学同济医学院附属同济医院);庹必光(遵义医学院附属医院);王江滨(吉林大学中日联谊医院);王兴鹏(上海交通大学附属第一人民医院);吴开春(空军军医大学西京医院);谢渭芬(第二军医大学附属长征医院);杨云生(解放军总医院);张军(西安交通大学医学院第二附属医院);周丽雅(北京大学第三医院);邹多武(上海交通大学医学院附属瑞金医院)
消化系统疾病基层诊疗指南编写专家组:
组长:李景南 周亚夫
副组长:方力争 吴东
秘书长:吴东
消化专家组成员(按姓氏拼音排序):何文华(南昌大学第一附属医院);季国忠(南京医科大学第二附属医院);寇毅(北京市房山区良乡医院);李景南(北京协和医院);梁晓(上海交通大学仁济医院);刘岩(解放军总医院第五医学中心);王红(广州市第一医院);吴东(北京协和医院);夏璐(上海嘉会国际医院);于岩波(山东大学齐鲁医院);祝荫(南昌大学第一附属医院)
全科专家组成员(按姓氏拼音排序):方力争(浙江大学医学院附属邵逸夫医院);冯玫(山西大医院);刘军兴(北京市丰台区方庄社区卫生服务中心);吴浩(北京市丰台区方庄社区卫生服务中心);习森(北京市怀柔区怀柔镇社区卫生服务中心);闫文冰(山东省肥城市边院镇中心卫生院);周亚夫(南京医科大学);朱兰(上海市徐汇区斜土街道社区卫生服务中心)
本指南执笔专家:寇毅 赵晶 审校专家:吕宾 李景南