Kymriah癌症基因疗法请点击此处输入图片描述
美国食品和药物管理局(FDA)首次在美国批准了一项治疗白血病的基因治疗方案。
基因治疗的目的是在药物或癌症治疗失败的情况下,给予患者第二次机会。 FDA将其称为美国首例可用于癌症的基因治疗。这种治疗方案被设计为“治疗儿童和青少年经常致死型血液与骨髓癌”。
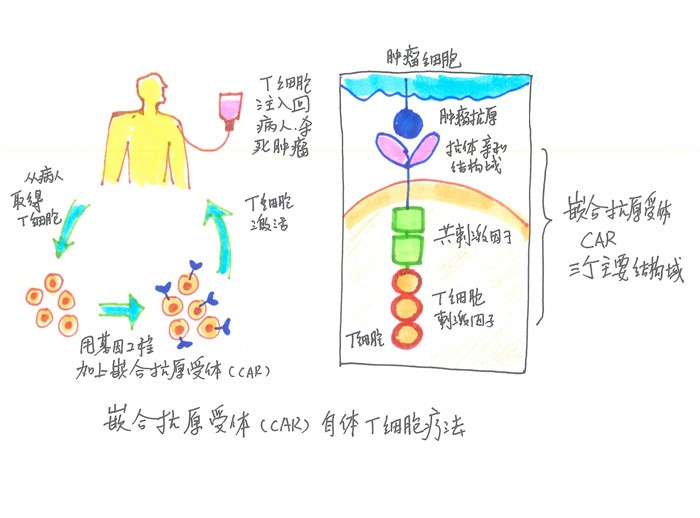
治疗流程
CAR-T(嵌合抗原受体T细胞)癌症基因治疗方案将由位于瑞士巴塞尔的跨国制药公司诺华公司提供,诺华将其定名为“Kymriah”(tisagenlecleucel)。
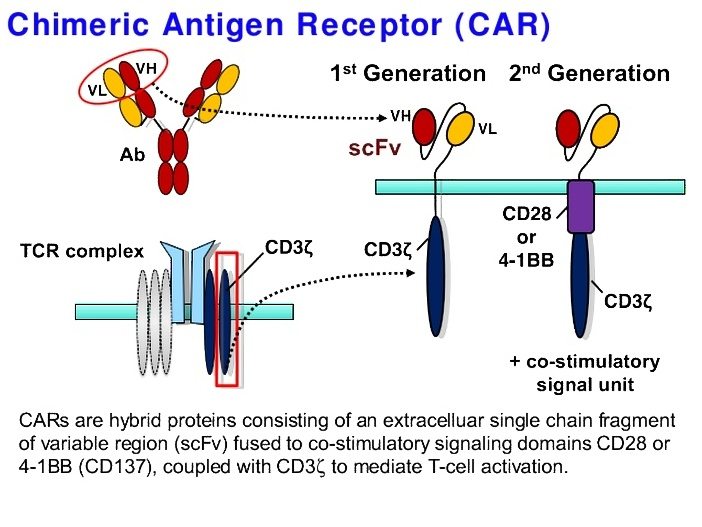
嵌合抗原受体
具体流程如下:Kymriah方案使用癌症患者自己的T细胞,并进行低温冷冻。然后,冻结的细胞被运往位于新泽西州诺华公司的制造工厂。在这里,T细胞将被进行基因重组,产生称为嵌合抗原受体(CAR)的新基因细胞。新基因细胞将引导T细胞在其表面上靶向杀死具有特异性抗原的白血病细胞。之后,将基因修改过的细胞注入患者体内。
FDA批准Kymriah是基于前期ELIANA实验的结果。ELIANA试验被认为是第一个全球儿科CAR-T细胞治疗试验,涉及美国,欧洲,加拿大,澳大利亚和日本25个医疗中心的68例患有急性淋巴细胞白血病的患者。实验结果显示,经过癌症基因治疗试验的68例患者中,有63例评价具有疗效。63例患者中有52例接受了Kymriah基因治疗,83%的受试者注射进基因修改细胞后三个月内,癌症得到完全缓解(CR),或出现不完全血细胞恢复(CRi)。
六个月后,89%接受癌症基因治疗的患者仍然存活,12个月后,79%的患者在试验中幸存下来。此外,参与试验的研究人员和医生没有发现任何痕量残留病(MRD)的迹象,这是一种表明潜在的癌症复发的血液标志物。
患者治疗后最常见的不良反为细胞因子释放综合征(CRS),比如发热,食欲降低,头痛,出血发作,心动过速,恶心,腹泻,呕吐,病毒感染性疾病,疲劳,急性肾损伤和妄想等。
诺华将“Kymriah”基因疗法定价为47.5万美元。