4 脓毒症的预防与阻断
4.1 及时确定高危人群:所谓高危人群即脓毒症易感人群,包括特定基因人群及脓毒症高发生率的感染部位或病原体感染的人群。对老年、营养不良、有基础疾病或免疫力低下的患者,应当尽快确定其感染部位及可能病原体 ;对严重肺部感染、腹腔感染及泌尿系统感染的患者,应当及时进行细胞因子筛查。任何感染患者都应当及时进行疑似脓毒症评估,对 SOFA 评分为 1 分、qSOFA 评分≥2 分或 NEWS 评分 4~6 分的患者应当进行重点关注,采取脓毒症阻断措施,并建议每 2 h 进行重复评分。
4.2 感染控制4.2.1 病原微生物检测 :引起急性感染的病原体包括细菌、病毒、真菌、支原体或衣原体、寄生虫等,但导致脓毒症的病原体主要为细菌、病毒和真菌。尽快确定病原体,并采取针对性抗微生物治疗是治疗感染性疾病的重点。传统的微生物培养存在耗时长、覆盖面窄的缺陷,急性感染更需要病原学的快速检测体系。针对常见的细菌和病毒等病原体,目前已有的快速检测方法包括:①肺炎链球菌尿抗原检测、军团菌尿抗原检测、GXpert艰难梭菌检测及FilmArray/罗氏 Cobas/Luminex 等推出的多重病原体检测平台等细菌检测方法;②真菌荧光染色、六胺银染色耶氏肺孢子菌检测等,新型隐球菌抗原检测、G试验、GM试验和曲霉免疫球蛋白(IgG 和 IgE)等真菌检测方法 ;③ 抗原和核酸检测,各种病毒的实时聚合酶链反应(PCR)等病毒检测方法。目前,二代测序技术不断成熟并应用于临床,可覆盖上千种病原体,最大程度地避免了漏检,已成为病原学诊断的有力手段。
4.2.2 抗感染治疗:虽然病毒、细菌和真菌等都有引起脓毒症的可能性,但在临床上依然以细菌和病毒引起的脓毒症为多。病毒感染目前尚缺乏特效治疗,通常采用免疫调节或中药制剂控制感染。在细菌感染中,控制感染不仅是预防脓毒症的重要措施,也是防止感染直接造成死亡的重要措施。抗菌药物的选择以覆盖可疑病原体及在可能感染部位浓度较高的抗菌药物为宜。同时,需要考虑患者的年龄、免疫状态和过敏反应等特殊情况。在急诊科抗感染治疗中,我们既要考虑覆盖病原体,控制感染,又要考虑避免抗菌药物滥用造成耐药菌的增加。快速病原体检测以及基于感染部位和高发致病菌的经验性思维将是我们选择抗菌药物的重要依据。《热病:桑福德抗微生物治疗指南 2018》对临床抗感染治疗给出了建议(表 4)。
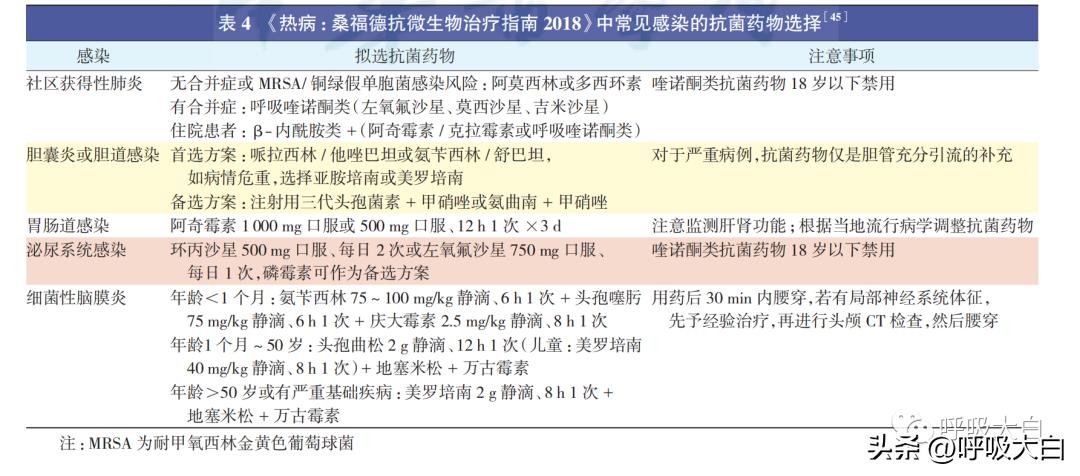
此外,抗感染治疗要及时,严重感染在诊断 1 h 内开始抗感染治疗,轻症感染在诊断后 4 h 内使用抗菌药物,并且建议在使用抗菌药物前采集病原学标本。
4.2.3 去除引起感染的病因 :对于有明确感染灶的创伤感染、化脓性胆囊炎、腹腔感染和泌尿系结石梗阻合并感染等,单纯抗菌药物治疗常常难以奏效,必须结合感染部位的局部处理,包括引流、清创和手术切除等。及时采取干预措施,也是防止脓毒症发生的一个重要环节。4.3 发现及阻断“细胞因子风暴”:感染引起的局部炎症反应可促进新生组织置换损伤组织,起到使已发生的损伤弱化的作用,但当过度炎症反应出现时,则有可能引起 SIRS,并导致脓毒症的发生。因此,及时发现“细胞因子风暴”并适时适量地调控炎症反应,对预防脓毒症的发生有重要意义,而且是预防脓毒症的核心。4.3.1 细胞因子筛查与 SIRS 确定:对脓毒症高危患者及可疑出现全身炎症反应的患者,应当进行细胞因子筛查,以确定 SIRS 的状态。主要参与 SIRS 的促炎因子包括 TNF-α、IL-1、IL-6、IL-12、巨噬细胞移动抑制因子(MIF)、sCD74 和高迁移率族蛋白 B1(HMGB1)等,参与代偿性抗炎症反应综合征(CARS)的抗炎细胞因子包括 IL-4、IL-10、IL-35、IL-37、转化生长因子 -β(TGF-β)和 IL-13等。有证据显示,当促炎因子明显升高,或出现炎症反应失衡时,即应当开始炎症调控。因此,对于脓毒症高危感染患者,应当定期进行细胞因子监测(2~4 h 重复 1 次),及时发现可疑脓毒症患者。目前医院普遍检测的细胞因子是 IL-6。IL-6 主要刺激参与免疫反应的细胞增殖和分化,并在机体的抗感染免疫反应中起重要作用。当炎症反应发生时,IL-6 血清水平升高早于其他生物标志物,IL-6 升高后诱导 PCT 和 CRP 生成。
4.3.2 炎症调控 :当发现细胞因子明显升高或炎症失衡的感染患者时,应当尽早进行炎症调控,使体内炎症反应恢复稳定平衡状态。4.3.3 糖皮质激素 : 大多数研究者认为使用糖皮质激素的适应证是脓毒性休克。在无持续休克和死亡风险较低的脓毒症患者中并未发现糖皮质激素能够降低脓毒症的病死率。目前已有足够的临床试验证据支持糖皮质激素可以调节脓毒症患者的固有免疫,促进炎症反应和器官衰竭问题的解决,并纳入了《中国脓毒症 / 脓毒性休克急诊治疗指南(2018)》。4.3.4 非激素类抗炎药物 :乌司他丁对调节细胞因子具有明确的作用。乌司他丁是一种能抑制多种蛋白水解酶活性的糖蛋白,是蛋白酶*制剂抑**,对胰蛋白酶等多种酶有抑制作用,具有稳定溶酶体膜、减少溶酶体酶释放、抑制心肌抑制因子(MDF)产生、清除氧自由基及抑制细胞因子释放的作用。在细胞因子升高的早期,使用小剂量的乌司他丁可以起到对细胞因子的调控作用 ;而在细胞因子失控阶段,促炎细胞因子与抗炎细胞因子失去平衡,对器官功能造成损伤,采用大剂量乌司他丁可以阻止患者脓毒症相关指标的进展。4.3.5 中药制剂 :祖国传统医学在治疗理念上主张调节机体平衡、标本兼治的原则。推荐了包括热毒宁注射液、血必净注射液和参附注射液等疗效相对明确的药物。此类药物不影响抗菌药物对细菌的杀灭作用,不会导致感染的扩散。临床实践证实,适时适量使用热毒宁注射液可缩短疾病治疗时间和症状缓解时间,降低疾病进展为器官功能损害的概率,有效预防脓毒症的发生和疾病进展。血必净注射液具有活血化瘀、舒通络脉和溃散毒邪的功效。
4.3.6 炎性介质特异性抗体 :目前研究较成熟的炎性介质特异性抗体是 TNF-α、IL-1 抗体和抗内毒素脂多糖(LPS)抗体,结果提示上述抗体可通过诱导促炎细胞因子失活达到减轻脓毒症的效果。4.3.7 免疫调理 :最近研究者发现炎症反应和免疫抑制共同贯穿于脓毒症发生发展过程中,而不是以往认为的先出现促炎反应后出现抗炎反应。在脓毒症发生过程中存在固有免疫和适应性免疫受到抑制的现象,表现为成熟粒细胞减少及成熟比例下降、单核 / 巨噬细胞“内毒素耐受”现象、树突细胞和淋巴细胞减少等。因此,及时进行免疫调理是预防脓毒症的重要环节之一。目前常用方法包括 :使用粒 - 巨噬细胞集落刺激因子(GM-GSF)和γ- 干扰素(IFN-γ) 调节固有免疫反应,采用胸腺素 α1 和 IL-7 等调节适应性免疫功能。
4.4 血管内皮保护与凝血调节 :血管内皮损伤和微血栓形成导致组织细胞的灌注下降,被认为是器官功能障碍的直接原因。这种内皮细胞损伤及微血栓形成引发弥散性血管内凝血(DIC)。引起 DIC 的机制包括促凝物质上调、抗凝物质下调及纤维蛋白溶解机制受损等。特别是血小板计数(PLT)。血浆 D- 二聚体也是临床常用的凝血功能参考指标,可反映凝血功能激活状态。DIC 不同进程中,其临床表现不同,主要包括出血、器官功能衰竭、休克及微血管病性溶血(表 5)。

4.4.1 抗凝治疗 :脓毒症伴随的炎症反应通过破坏凝血系统,损耗内源性抗凝因子,使纤溶活性受到抑制,发生血栓,从而导致组织缺氧、器官功能受到损伤。炎性因子及炎性细胞破坏生理抗凝机制的同时,还会增加组织因子的释放,使外源性凝血因子被激活,加重炎症反应。而整个过程一直循环,导致抗凝物质持续消耗而衰竭,最终导致凝血机制出现异常,甚至可发展成多器官功能衰竭,造成死亡。针对感染患者采取适当的抗凝治疗是防止微血栓形成、预防脓毒症发生的措施之一。临床采用的药物主要是普通肝素和低分子肝素。4.4.1.1 普通肝素 :普通肝素是有效的抗凝血药物,其应用及剂量因 DIC 临床类型和分期的不同而异。及时肝素治疗可以改善周围组织灌注,有降低病死率趋势,但也有可能增加严重出血的风险,并未被推荐为脓毒症并发DIC 的常规用药。但重点在于如何早期发现高凝状态,只有处于高凝期的患者,凝血酶增多,微循环有血栓形成时,应用肝素抗凝治疗才能够取得满意效果。4.4.1.2 低分子肝素:低分子肝素作为由普通肝素解聚而成的抗凝药物,在用药后能迅速发挥抗血栓作用,且研究显示其同时可显著改善血流动力学,兼有生物利用度高、出血风险低和免疫活性及半衰期较长的特点。此外,运用低分子肝素治疗可能发生脓毒症的感染患者,可抑制异常的凝血功能,减少血小板的异常损耗,阻止氧自由基损伤,对微循环存在明显的改善作用。在抑制病理性凝血系统激活的同时,低分子肝素还能有效减少严重出血的发生。4.4.2 替代治疗 :替代治疗取决于是否因某种血液成分减少而导致的出血或极高的出血风险。患者如出现以下情况时,可考虑使用血液制品替代治疗。4.4.2.1 血小板:对于活动性出血患者来说,PLT 需要达到 50×109/L 以上。 其他输入血小板的指征包括:①PLT<10×109/L而无明显出血征象;②PLT<20×109/L 而存在高出血风险。4.4.2.2 凝血因子:① 在没有出血或侵入性操作计划时,不建议用新鲜冰冻血浆纠正凝血功能异常;②伴有凝血酶原时间(PT)或活化部分凝血活酶时间(APTT)延长>1.5 倍,或纤维蛋白原(FIB)<1.5 g/L,可静脉输注新鲜冰冻血浆 15~30 mL/kg ;③ 因液体负荷过多导致 DIC 患者出血时,可使用浓缩凝血因子。DIC 患者血浆 FIB 至少应维持在 1.0~1.5 g/L。4.5 循环容量支持 :“拯救脓毒症”的重要手段之一是液体复苏,“复苏”的前提是出现明确的有效循环血容量下降或休克。早期的内皮细胞损伤和毛细血管渗漏可以造成隐形的容量不足,此时需要我们尽快识别并给予液体补充支持,支持的时机越早越好。因为液体的有效补充既可以保证组织灌注,也可以防止血液高凝状态和微血栓形成。要在脓毒症前期就开始EGDT的液体支持,并且要尽快将qSOFA及 NEWS 评分降低。对于急诊科而言,患者能够接受治疗的时间远远早于ICU。因此,专家们认为早期积极的液体支持对急诊科防止脓毒症发生仍然是重要的治疗策略之一。理论上首先选择晶体液,特别是与细胞外液离子成分、酸碱度和电荷等影响内环境的因素相近的晶体液。有专家认为,由于晶体液相对分子质量小,易于通过毛细血管渗漏至组织间隙,不作为首选。补液量以维持大循环稳定(心率、平均动脉压和中心静脉压在正常范围)及动脉血乳酸正常为标准。 4.6 器官功能保护4.6.1 提高预防意识 :从感染到脓毒症,再从脓毒症初期到器官功能不全,最终发展为多器官功能衰竭,是一个连续性过程。急诊医生需要准确认识脓毒症引起 MODS 的过程,尽早排查高危患者,确定感染程度,发现和控制“炎症风暴”,进行呼吸循环支持,尽早实施器官功能保护。对于已有 MODS迹象的患者,应尽快采取措施,避免器官功能不全进一步加重,也避免器官损伤数目的进一步增加。4.6.2 提高整体观念 :人是一个整体,生理状态下各器官相互作用,人体功能处于稳定状态。一方面,当存在器官功能不全时,人体的平衡将被打破。若无法尽早调整这一失衡,将可能导致原有器官损伤进一步加重并逐渐出现其他器官功能不全。另一方面,任何干预措施均有可能打破原有的平衡,造成后续出现一系列器官损伤。4.6.3动态评估:综合检测及动态评估器官功能对于早期发现器官损伤,评估MODS治疗的疗效至关重要。应重视患者生命体征、尿量、肢体末梢及皮肤黏膜等临床重要参数的改变,亦需采用一些无创和有创的客观监测手段。呼吸循环监测是急重症患者诊治的核心,而对于疑似脓毒症患者,感染和炎症等指标的监测亦尤为重要。在临床上可以动态监测 NEWS 评分、SOFA 评分及 MODS 严重度评分等,获取不同系统的监测指标,从不同角度进行综合分析,有利于早期预见 SIRS 和 MODS,有利于脓毒症的阻断。4.6.4 早期干预 :脓毒症的早期干预重点在于对人的调整,进而减少过度反应对器官功能的损害,在这方面,应该充分发挥中医中药的治疗作用。脓毒症属于祖国医学“外感热病”“脱证”“血证”“暴喘”“神昏”“脏竭症”等范畴,其造成机体损害的主要原因是素体正气不足,外邪入侵,入里化热,耗气伤阴;正气虚弱,毒邪内陷,络脉气血运行不畅,导致毒热、瘀血、痰浊内阻,瘀阻脉络,进而令各脏器受邪而损伤。早期预防和阻断脓毒症的思路与《黄帝内经》提出的“治未病”理论不谋而合。临床多分为“四证四法”,即毒热证与清热解毒法、腑气不通证与通里攻下法、血瘀证与活血化瘀法、急性虚证与扶正固本法。4.6.4.1 中医辨证施治 :① 毒热证 :症见高热持续不退、烦躁、神昏、恶心呕吐、舌质红绛、脉数等。临床常用清热解毒的中药治疗,如热毒宁注射液、清开灵注射液、醒脑静注射液和安宫牛黄丸等。② 腑气不通证 :症见西医学肠梗阻的表现,包括腹胀、呕吐、无排便排气、肠鸣音减弱或消失等。代表方大承气汤能显著降低 MODS 患者病死率,用于脓毒症的治疗可减少炎性介质的产生、抑制炎症反应、调节免疫功能,同时还具有抗菌作用。③ 血瘀证 :症见高热,或神昏,或疼痛状如针*刀刺**割、痛处固定不移,常于夜间加重,肿块,出血,舌质紫暗或有瘀斑,脉沉迟或沉弦等。常予以红花、赤芍、川芎、当归、丹参等活血化瘀中药及血府逐瘀汤等方药治疗 ;中成药以复方丹参注射液和血必净注射液为代表。④ 急性虚证 :阴脱症见意识恍惚或烦躁不安、面色潮红、两眶内陷、皮肤皱褶、身热心烦、口渴欲饮、少尿或无尿、舌红干燥、脉细数等,与西医学的休克表现相似 ;临床常用生脉注射液或参麦注射液以益气养阴固脱。阳脱症见冷汗淋漓、四肢逆冷、忽尔昏愦、面赤唇紫、口开目闭、手撒遗尿、舌淡或紫、脉微欲绝或散大无根等;临床常用参附注射液以益气温阳固脱。阴阳俱脱而症见急病重病,突然大汗不止或汗出如油,精神疲惫不支,声短息微,遗尿*禁失**,舌卷少津,脉微细欲绝或脉大无力等 ;临床上可联用生脉注射液、参麦注射液及参附注射液。4.6.4.2 单味药 :① 大黄 :单味生大黄具有促进胃肠蠕动、保护肠道黏膜、促进内毒素排出、减少细菌和毒素移位及抗炎抑菌作用,对 MODS 有显著的预防治疗作用,能提高累及 4 个以上器官 MODS 的存活率。② 丹参 :丹参的水溶性成分具有良好的抗血栓形成和改善循环作用,从而减轻器官功能损害。体外实验表明,丹参有拮抗 LPS 作用,其对肺的保护作用可能是通过抑制或减少 TNF-α等细胞因子在血及肺组织中的表达,减轻了由此介导的肺部急性炎症反应。③ 人参 :有实验研究证实,人参多种有效成分对内毒素结构的直接破坏作用不明显,但对其引起的发热、白细胞骤降及休克、死亡均有较强的拮抗和防护效果。
5 结 语 脓毒症起始于感染,经过“细胞因子风暴”、毛细血管内皮损伤、毛细血管渗漏、微血栓形成和组织灌注下降,最终导致器官功能损害。多年来,医学界已在器官功能保护和替代等方面积累了丰富的实践经验,但脓毒症救治效果仍有待提高。目前在发生感染后至走向脓毒症的过程中所做的工作还很有限,分析其原因:一是病理生理复杂、临床难点多;二是对脓毒症预防认识的局限性。急诊医学作为一个接触患者最早的临床专科,其工作特点与优势就在于对疾病的早期诊断、危险分层、合理分流及科学救治(图 1)。
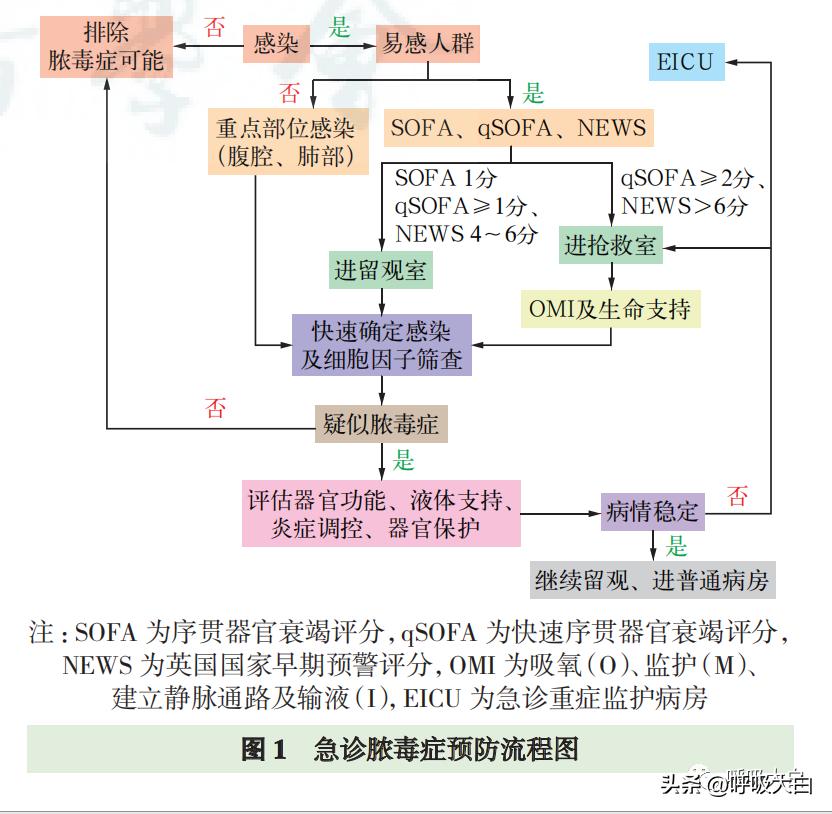
通过早期干预疾病的病理生理发展进程,实现脓毒症的阻断,进而降低脓毒症的发病率。此外,通过对于围脓毒症期患者的合理诊治,降低脓毒症的病死率。当然,这项工作刚刚起步,MODS 还面临着众多挑战,如感染性疾病的复杂性、易感人群的复杂性、“细胞因子风暴”的启动和发展的复杂性等。脓毒症的预防与阻断工作还有赖于所有临床工作者和基础研究人员的共同努力,可以相信这是一个好的开端。