2020年全球爆发新冠疫情以来,在大家对新冠病毒传染恐惧的影响下,世界各国政府将资源全力投入到新冠疫情防治中,世界各国对于癌症筛查形成资源排挤与下降的趋势。发表在《预防医学》杂志上的一篇论文,研究了2020 年 1 月至 6 月COVID-19 对癌症早期检测计划的筛查服务的影响。与前 5 年的平均值相比,2020 年 4 月,美国女性接受的乳腺癌和宫颈癌筛查检测总数分别下降了87% 和84%!导致这段时间筛查率下降的可能因素包括筛查场地关闭、乳腺癌和宫颈癌筛查服务因COVID-19暂时停止、要求或建议减少外出等,对感染COVID-19的恐惧也可能阻止了个人寻求卫生保健服务,包括癌症检查。

在中国依然如此!新冠疫情间,武汉大学人民医院宫颈癌筛查访问量下降约50%,HPV 感染率下降约10%。其中新冠大流行后,HPV 感染率低于疫情前(23.3% VS 21.2%),可能是严格的隔离政策减缓HPV传播所致。一项基于4个高收入国家建模分析:由于新冠疫情防控筛查中断12个月,到2030年预估将增加5-6%的宫颈癌病例[1]!

如何在新冠疫情下消除宫颈癌,减少疫情对宫颈癌二级和三级预防的影响?
由IARC(国际癌症研究所)早期检测、预防与感染部的Partha Basu博士国际同事讨论后在nature cancer发表评论:“新冠疫情时代消除宫颈癌,科技创新至关重要,包括有效可负担疫苗、自采样床旁检测(POCT)HPV、更实惠、便捷、安全的分流及诊断(癌前最高风险人群)”。

中国目前有效可负担的疫苗
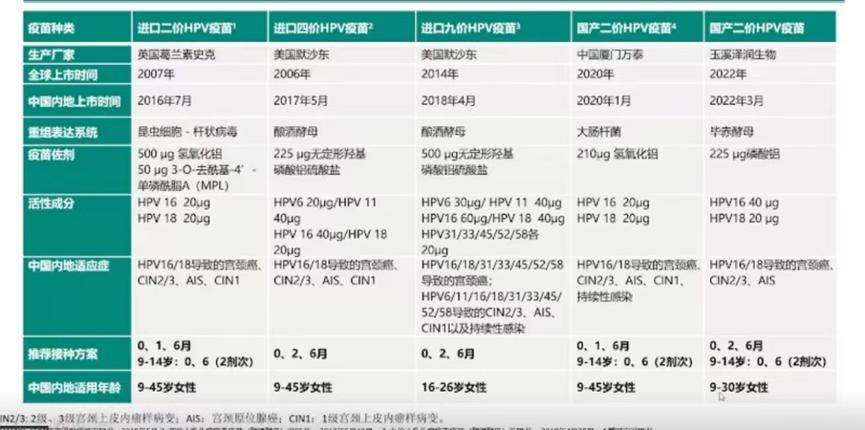
目前在中国大陆获批上市了5种HPV疫苗,具有很好的保护效力,积极推动HPV疫苗的接种率。
九价疫苗的批签发量呈现出明显的增长势态,但面对中国如此大的人口基数,仍然是杯水车薪,“一针难求”!
根据Frost&Sullivan公布的数据统计,中国九价HPV疫苗适龄人群(16-26岁)约1.2亿。按照第0-2-6月的接种程序来看,截至2021年上半年全部获批签发的一千一百多万支九价HPV疫苗无异于杯水车薪,仅可供三百多万适龄女性完整接种三针,这个数字仅为适龄女性人数的3%左右。
加之各地政策和疫苗库存不同,“抢针”情况不容乐观,摇号中签率基本不超过2%。不少适龄女性,尤其是26岁即将超出适龄范围的女性对是否还能顺利接种九价HPV疫苗表示非常焦虑!
HPV自采样
在新冠疫情大环境下,禁止筛查中心人群聚集,以此避免新冠的传播和感染。因此在这种情况下,自采样HPV检测作为一种便捷、安全且简单的筛查手段替代医师取样,能够大大提高了宫颈癌筛查的覆盖率。研究证明自采样对于CIN2+的病例,具有与临床医师取样相当的诊断准确性[2-4]。新冠疫情促进全球加速引进HPV自采样检测,因为它降低了接触病毒风险并扩大了卫生服务,有助于解决筛查延误的问题。
长期以来,国际上一直建议,目标女性的最低筛查覆盖率需要达到 70%,才可以观察到早期筛查对疾病死亡率的影响。世卫组织消除宫颈癌计划正在加强这一目标,即 70% 的 35- 45 岁女性至少接受两次高质量的检测[5]。目前,筛查和治疗已发现的宫颈病变是短期内减少宫颈癌的主要策略。而中国现在的宫颈癌筛查率不足40%,尤其是在新冠疫情大环境和资源不足的地区(例如,基础设施、专业人员非常有限),距离70%的目标相差甚远。鉴于 HPV 自采样的安全便捷及不受筛查场所限制的优势,成为一个增加筛查覆盖率的关键机会。
结合中国当前实际情况,做好HPV疫苗的接种和定期的宫颈癌筛查(HPV自采样作为优势补充)相结合才可在新冠疫情下消除宫颈癌减少疫情对宫颈癌二级和三级预防的影响。
99.7%的宫颈癌是由高危型人乳头瘤病毒(HPV)持续感染所致。HPV感染发展到宫颈癌通常需要5-10年,如能早筛查、早发现,宫颈癌完全可以成为一种可以预防和治疗的癌症。E6/E7 是HPV的主要致癌基因,最终导致宫颈癌变,癌症发生!检测E6/E7 mRNA就能评估癌变风险,宫颈病变进展程度及HPV病毒活跃程度。
HPV E6/E7 mRNA自采样是宫颈癌的另一种筛查工具,全面覆盖世界卫生组织公布的14种高危型HPV。受检者无需前往医院等候医生取样,而是在家中自行采集收集宫颈细胞样品进行检测。
HPV E6/E7 mRNA自采样不受时间、地域限制,简单快捷易操作,无创无痛,足不出户即可做宫颈癌筛查。
•准确率高, 99%的女性第一次就能成功完成自采样
•自采样检测与专业医师采样准确率相当
•与全国多家医院采用相似的检测方法
参考文献:
[1]2022 CSCCP会议——隋龙,《新冠疫情对消除宫颈癌战略实施影响及应用探讨》。
[2]. H. Nishimura, P.T. Yeh, H. Oguntade, C.E. Kennedy, M. Narasimhan. HPV self-sampling for cervical cancer screening: a systematic review of values and preferences. BMJ Glob. Health, 6 (5) (2021 May), p. e003743.
[3]. M. Arbyn, S.B. Smith, S. Temin, F. Sultana, P. Castle. Detecting cervical precancer and reaching underscreened women by using HPV testing on self samples: updated meta-analyses. BMJ., 363 (2018 Dec 5), p. k4823.
[4]. A. Kamath Mulki, M. Withers. Human Papilloma Virus self-sampling performance in low- and middle-income countries. BMC Womens Health, 21 (1) (2021 Jan 6), p. 12.
[5]. WHO. Cervical Cancer Elimination Strategy. 2020.
免责声明:本文不构成临床诊疗建议,具体情况请参考专业医生的指导。
转载声明:本公众号所发布的相关内容,未经授权,严禁转载。如需转载,需注明来源。