肺癌是世界范围内高发病率和高死亡率的常见恶性肿瘤,非小细胞肺癌占肺癌的80%左右,其中25%为鳞状非小细胞肺癌,约70%的非小细胞患者确诊时已为晚期。
在过去,与非鳞状非小细胞肺癌相比,肺鳞癌的一线治疗选择更加有限。更新的抗代谢药物如培美曲塞,在鳞状细胞患者中的活性很低或没有,抗血管生成治疗如贝伐单抗,因为毒性问题无法使用。含铂两药化疗是晚期肺鳞癌的标准治疗。
然而事情就在2008年开始有了转变。那年8月,一个名为MDX1106-03的新药悄然发布了临床试验信息开始招募第一批患者,而这个就是后来声名鹊起的O药。
2019年7月25日JAMA Oncology 杂志在线发表了这项研究的二次分析结果。可以用4个字概括:不负众望!
CA209-003是一项评估nivolumab治疗晚期或复发性恶性肿瘤患者的安全性和有效性,此次分析了270名接受nivolumab的晚期黑色素瘤患者、肾癌和非小细胞肺癌患者。
研究结果着实令人欣喜!
黑色素瘤5年生存率为34.2%;
肾癌5年生存率为27.7%;
非小细胞肺癌5年生存率为15.6%
值得注意的是,该研究所纳入的患者都至少接受过1次全身癌症治疗,71.9%的患者接受过2次或更多次全身性癌症治疗。如果这些患者继续按当时标准治疗,那么结果会如何?
当时的晚期黑色素瘤的3年生存率约5%,晚期非小细胞肺癌5年生存率约6%。
可以说,O药的治疗大大提高了这些癌症患者的5年生存率!
此外,还有一个有意思的发现,与未出现不良反应的患者相比,出现O药不良反应的患者的总生存期显著延长。
对于有任何不良反应事件的患者,中位生存19.8个月
对于出现严重不良反应的患者,中位生存20.3个月
未出现不良反应的患者,中位生存5.8个月
这么看起来不良反应时间似乎是O药患者长期生存的标志,研究者还在进一步研究。
那么中国患者的数据如何呢?
CheckMate 078研究是首个在国内开展,以中国患者为主,一项比较纳武利尤单抗(简称O药)和多西他赛用于治疗含铂化疗失败的非小细胞肺癌的有效性与安全性的研究。O药也正是基于该研究结果获批非小细胞肺癌适应症,成为我国首个获批上市的PD-1*制剂抑**。该研究也是唯一具有2年随访数据的PD-1*制剂抑**的研究,在今年的中国临床肿瘤学会(CSCO)大会公布了最新研究数据。
研究结果显示,与多西他赛单药相比,O药组持续显示总生存(OS)获益,O药组与多西他赛组2年OS 率分别为28% VS 18%;客观缓解率 (ORR)O药组为18%,多西他赛组仅为4%;与多西他赛相比,O药组显示无进展生存期(PFS)获益,O药组与多西他赛组2年PFS率分为为11%和2%。

CheckMate 078研究的2年随访数据
数据分析还发现,对于O药存在客观应答的患者中有39%在2年时仍持续应答,而多西他赛组2年仍持续应答率为0%,这就意味着O药治疗有效的患者,有很大机会长期有效且持续超过两年。
此外亚组分析表明,接受O药的所有亚组中均观察到OS获益,包括鳞癌或非鳞癌,PD-L1表达≥1还是<1%。虽然从研究结果显示PD-L1水平越高,获得长期生存的机会越大,但该研究的首要研究者、广东省人民医院的吴一龙教授表示无论PD-L1状态如何,患者均能从O药治疗中获益。
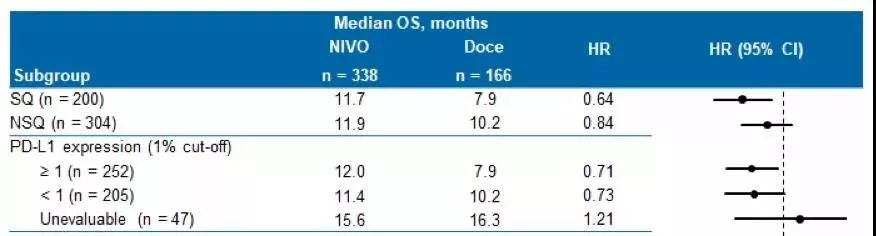
CheckMate 078研究的亚组分析结果
与全球研究CheckMate 017/057相比,CheckMate 078研究中鳞癌OS优于全球数据,分别为12.3个月 VS 9.2个月,非鳞癌基本与全球研究一致,分别为11.9个月和12.2个月,这表明了中国鳞癌患者可能获益更多。
也许,从当时看来,这些第一批使用PD-1的人是孤注一掷的选择一种新药,但正是因为他们的勇气与信任,才有了如今这样的研究成果!
因此,参加临床试验,不仅能够让自己从新药中获益,而且还能帮助他人,并推动医学的发展。
目前肺癌有多个临床试验项目正在开展,如果是肺鳞癌,刚确诊或已经进行化疗或免疫治疗都可能有适合你的临床试验哦~
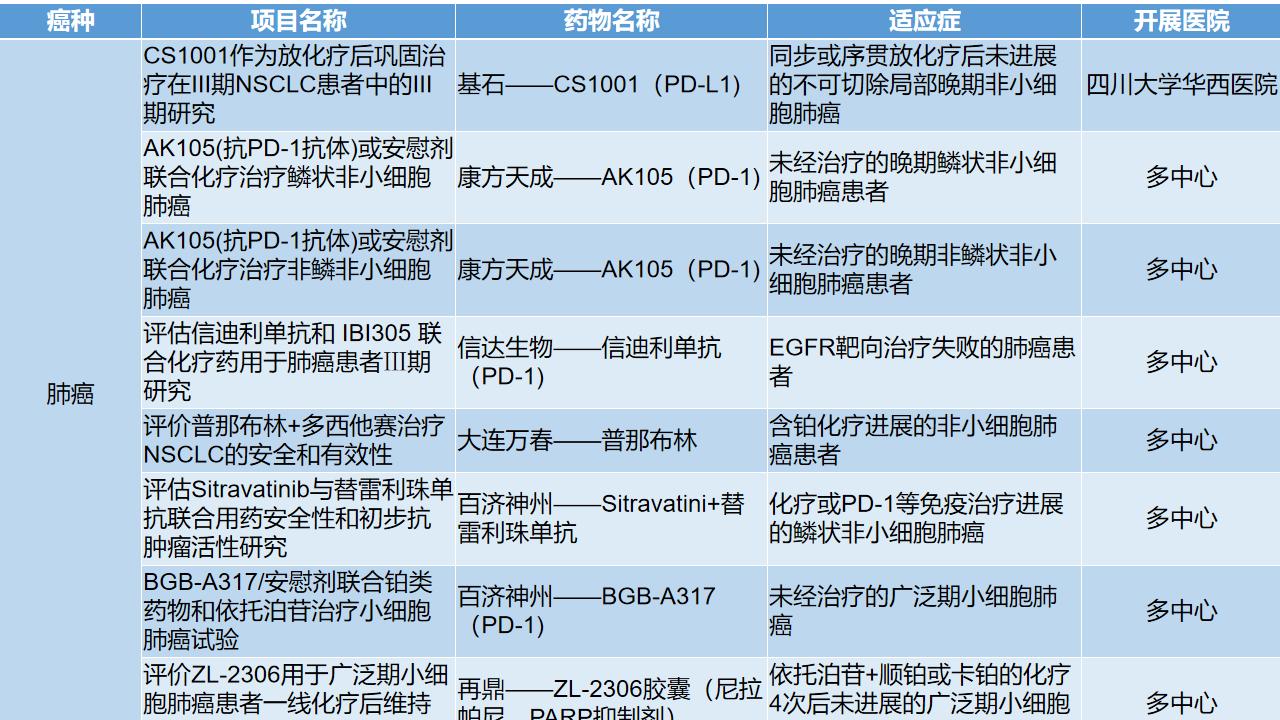
点击“了解更多”获取临床试验信息
参考文献:
1 Korn EL,Liu PY,Lee SJ,et al。对转移性IV期黑色素瘤的II期合作组试验进行Meta分析,以确定未来II期试验的无进展和总体生存基准。 J Clin Oncol。2008; 26(4):527-534。doi:
2 Hodi FS,O'Day SJ,McDermott DF,et al。使用ipilimumab改善转移性黑色素瘤患者的生存率。 N Engl J Med。2010; 363(8):711-723。doi:3.Goldstraw P,Chansky K,Crowley J,et al; 国际肺癌分期和预后因素研究委员会咨询委员会和参与机构。IASLC肺癌分期项目:在即将出版的(第八版)TNM肺癌分类中修订TNM分期分组的建议。 J Thorac Oncol。2016; 11(1):39-51。doi: