
视网膜变性 (Retinal Degeneration, RD)疾病是世界上最常见的致盲性眼病之一。RD晚期视网膜神经元进行性退化,现有的治疗方法均效果有限。近年的研究发现,干细胞移植可替代退化的视网膜神经元并且恢复RD模型视力,被认为是最有希望的治疗策略 【1】 。目前,已有的基础和临床研究报道了移植视网膜祖细胞(retinal progenitor cells, RPCs)可以替代RD中受损的视网膜细胞,并提高受体视功能 【2, 3】 。在对晚期变性的治疗效果以及治疗机制方面的讨论仍是近期研究的热点。主流观点认为细胞移植后,物质交换与细胞替代都有助于修复变性视网膜 【4】 ,但发生物质交换与细胞替代的比率是由受体视网膜的微环境所决定的 【5】 。在晚期变性视网膜(advanced degenerative retina, ADR)中,外核层(ONL)明显变薄,而内核层(INL)和神经节细胞层(GCL)的厚度保持不变。外界膜完整性遭到破坏,允许大量供体移植细胞迁移到内层视网膜并在形态学上与宿主神经元形成连接。而在之前的研究中,C-Kit+ RPCs能够与早期变性视网膜中的神经元建立形态上的突触样连接 【6, 7】 。由此推断,C-Kit+ RPCs可能会与 ADR 中的宿主细胞更高效地产生突触样连接。这些新形成的突触样连接的功能也需要进一步研究。因此,有必要建立一种可以实时观察大量供受体间突触连接功能的方法。此方法对阐明移植细胞整合进入神经回路并改善ADR视功能的机制具有重要意义。
2021年7月13日,陆军军医大学西南医院眼科团队在国际干细胞研究协会 (The International Society for Stem Cell Research,ISSCR)会刊 Stem Cell Reports 杂志发表了题为 Synaptic repair and vision restoration in advanced degenerating eyes by transplantation of retinal progenitor cells 的封面论文。 该研究将视网膜类器官来源的C-Kit+/SSEA1- RPCs移植到终末期RD大鼠的视网膜下腔后,RPCs能成功分化为视网膜神经元,移行到视网膜神经上皮全层,与宿主残存神经元形成新的功能性神经突触并与视网膜神经回路连接,从而有效改善终末期RD模型的视功能。


Stem Cell Reports 杂志封面图片展示了移植的 C-kit+/SSEA1- RPCs在受体视网膜铺片上的移行分布。RPCs已用GECI (GCaMP5,绿色)标记。受体视网膜照片与蝴蝶剪影相结合寓意重获新生——干细胞移植使终末期变性视网膜再生,宛如蚕蛹破茧成蝶的生命更新过程。
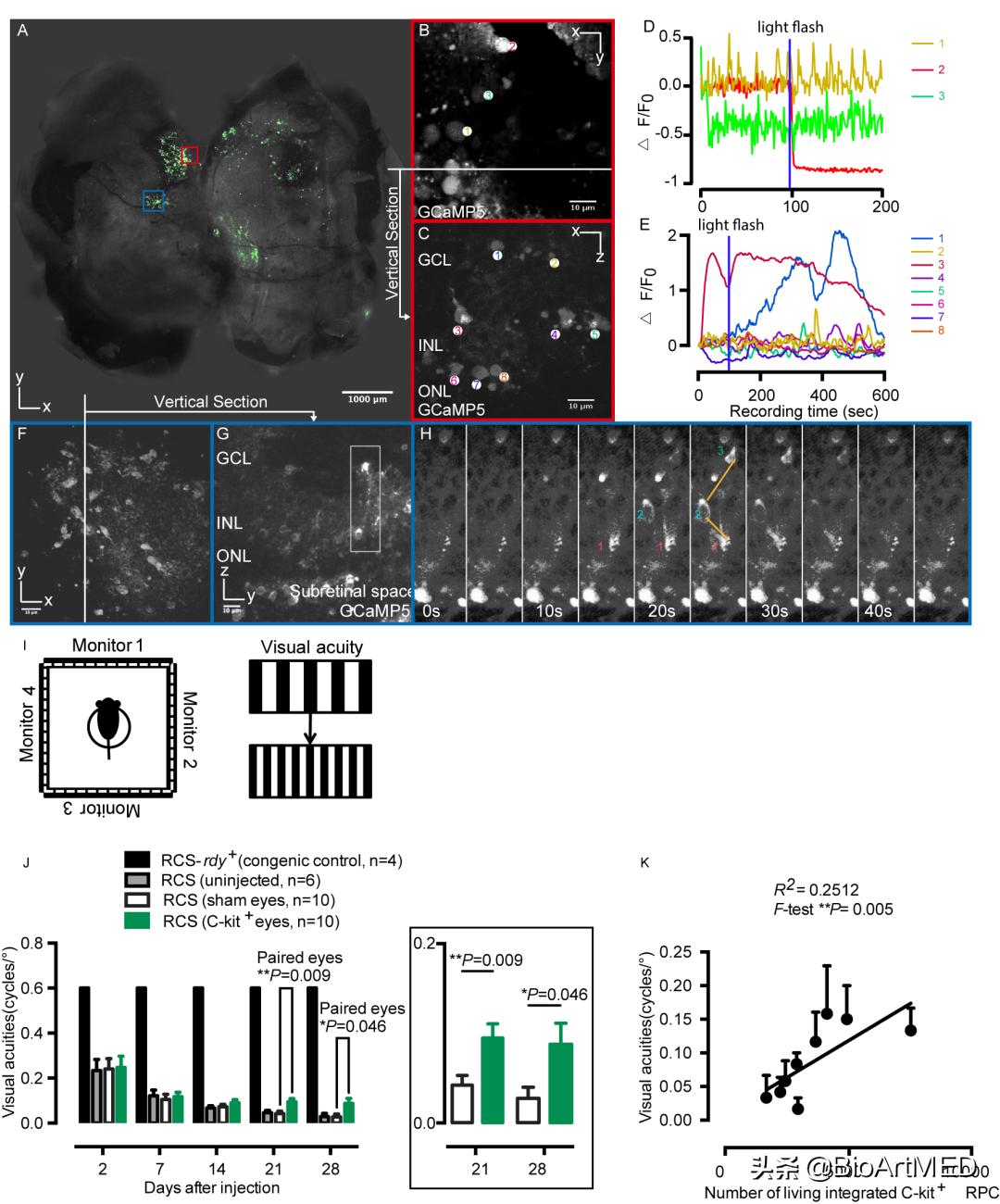
图1 在GECI的帮助下,直观地展示了RPCs修复突触并恢复视力的过程。
该研究借鉴了中枢神经系统中神经突触的研究方法,首次 从功能整合角度为干细胞移植修复和再生变性视网膜的细胞替代学说提供了新证据 。研究结果表明:特定RPCs群可以在终末期RD神经元大量损失的环境中,分化为有功能的成熟神经元,整合进入视网膜神经回路,从而修复动物模型视功能。该研究应用了一系列先进的实验技术,其中包括双光子显微镜钙成像技术,结合形态与功能, 直观地展示出的变性视网膜神经突触修复和视力恢复的过程,为采用RPCs治疗终末期RD及其临床转化提供了重要依据 (图1) 。
据悉,该研究的通讯作者为陆军军医大学西南医院眼科、视觉损伤与再生修复重点实验的 阴正勤 教授和 刘勇 教授, 何翔宇 博士为该论文的第一作者。
原文链接:
DOI:https://doi.org/10.1016/j.stemcr.2021.06.002
制版人:十一
转载须知
【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经允许禁止转载,作者拥有所有法定权利,违者必究。