进化适应论决定了哺乳动物体内大部分生理过程遵循周期性近日节律波动,其产生的分子基础为内源性 生物钟 (circadian clock) ,使机体得以预测外部环境变化并同步内环境改变。人体生物钟系统具有严格的等级结构,其调控中枢位于下丘脑视交叉上核 (SCN) ,而诸多外周节律器官则被称为外周生物钟 (peripheral clocks) ,它们在接收SCN中枢调控的同时又具有高度的自主性和自我维持性。 虽然胰腺是一个已被阐述的外周节律器官,但由于其组织构成的复杂性,相较于内分泌胰腺,外分泌胰腺的时相调控机制及病理生理功能并未得到充分研究。
2022年9月28日,上海交通大学医学院附属第一人民医院消化中心、上海市胰腺病重点实验室 蒋巍亮 、 万荣 课题组,北京生命科学研究所 张二荃 课题组,重庆医科大学 鞠大鹏 课题组等合作在 Science Translational Medicine 发文题为 The pancreatic clock is a key determinant of pancreatic fibrosis progression and exocrine dysfunction , 揭示胰腺生物钟在慢性胰腺炎(CP)病程中发挥的作用。

这项研究围绕三个关键问题展开:一、生物钟紊乱 (circadian disruption) 是作为CP发病的始动亦或维持/推动因素而存在?二、生物钟如何调节胰腺外分泌以及在复杂的计时系统中哪个元件起了主导作用?三、我们是否可以靶向生物钟以预测或治疗CP?
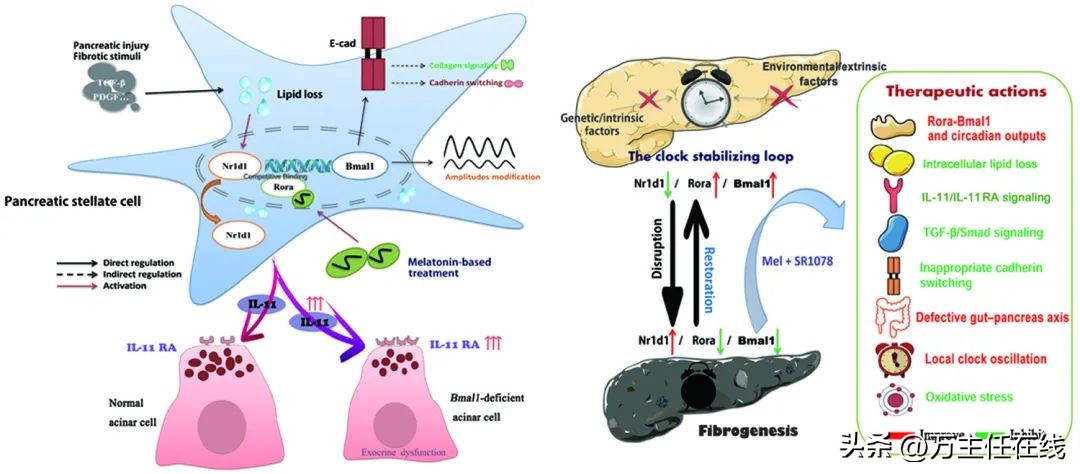
研究者首先通过临床样本确定了胰腺纤维化组织中生物钟核心转录—翻译反馈环路 (TTFL) 显著紊乱,部分元件出现表达降低以及节律减弱、振幅减小。为了进一步解释这些现象,研究者使用多种转基因工具小鼠 ( mPer2 ::luc, Bmal1 −/−, Clock ⊿19, Nr1d1 −/−, Bmal1 PKO等) ,并建立了两种CP动物模型以模拟不同病理过程。由于完整的生物钟振荡机制包含输入信号、振荡器以及输出通路三个部分,他们还建立了一个时间限制性进食 (daytime-restricted feeding) 模型,以观察内源或外源因素造成的生物钟紊乱对疾病的影响。动物实验结果显示,无论通过干涉小鼠摄食模式或者敲除核心钟基因 Bmal1 均可明显加重胰腺组织损伤和纤维化,尤其是 Bmal1 缺陷小鼠模型出现了类似CP晚期外分泌功能衰竭的表现。随后,研究人员通过体外共培养模型,观察生物钟如何调控CP中两类重要的效应细胞:胰腺腺泡细胞 (PAC) 和胰腺星状细胞 (PSC) 之间的信号转导。通过筛选,他们发现 Bmal1 PKO-PSC分泌过量的白介素11 (IL-11) ,而 Bmal1 PKO-PAC则由于本身受损的分泌功能储备以及IL-11RA高表达而导致更显著的细胞脆性。
另一方面,研究人员从头探索胰腺生物钟紊乱的原因。由于分子钟核心TTFL与多条次级环路 (secondary loops) 紧密衔接,其中一条由Ror/Rev/Bmal1构成的环路保证了core loop的稳定运行,因此其也被称为“circadian stabilizing loop”。然而,CP时Rora和Nr1d1对 Bmal1 启动子的竞争性结合平衡被打破,Nr1d1抑制 Bmal1 转录进而导致其低表达以及下游通路失调——这也说明既往受到关注相对较少的次级环路或许在一些生理/病理过程也发挥了极为重要的功能。
自上世纪70年代Konopka和Benzer首次在果蝇中成功克隆出第一个钟基因 Period 后,关于生物钟相关的理论研究逐渐系统丰富,并衍生出专门的“时间生物学 (Chronobiology) ”,拉斯克奖、诺贝尔奖也先后授予这一领域的杰出工作者们。但是需要看到,在生物钟逾40多年的研究历程中始终存在转化与应用的巨大鸿沟。迄今,通过调节生物钟/昼夜节律来治疗疾病的可能性仍然面临挑战,生活方式及行为管理、时辰疗法 (chronotherapy) 和药物干预均是潜在的方法。 本研究将褪黑素与Rora激动剂SR1078联用,两者协同稳定stabilizing loop并重启胰腺生物钟 (Restarting the clock) , 可显著加强其在体内的效力从而改善CP进程、减轻纤维化。这些研究成果进一步丰富了胰腺生物钟的理论框架,并为后续研究、开发作出铺垫。
论文链接:
https://www.science.org/doi/10.1126/scitranslmed.abn3586
