来源:上海市胸科医院呼吸科
近日,我科韩宝惠教授、钟华主任、陆俊博士在生物标志物专业期刊Biomarker Research 发表一篇题为“Blood-based tumor mutation index act as prognostic predictor for immunotherapy and chemotherapy in non-small cell lung cancer patients”的研究论文。该研究综合不同肿瘤突变参数指导临床疗效差异和不同临床特征在临床治疗预后方面的差异,建立肿瘤突变指数(TMI,Tumor Mutation Index),并将该指数作为生物标志物用于筛选潜在响应患者。
前期,生物标志物TMI已在多靶点抗血管生成药物安罗替尼临床疗效预测方面得到验证。该研究首次将生物标志物TMI应用于免疫治疗和化学治疗响应人群筛选,并观察TMI是否具有较好的预测价值。由于肿瘤内组织间的异质性和疾病发展的复杂性,用于跨治疗方式(如抗血管生成治疗,化学治疗,免疫治疗等)的生物标志物建立始终是临床生物标志物开发的难题和瓶颈。此研究成果可能为生物标志物TMI应用于临床实践提供重要依据。
研究背景:
近年来,基于循环肿瘤DNA (ctDNA) 测序的生物标志物(如bTMB)可能为非小细胞肺癌(NSCLC)患者的免疫治疗疗效预测提供帮助。是否有更好更稳定的生物标志物既可用于免疫治疗预测又可用于化学治疗预测仍不清楚。该研究旨在评估基于ctDNA测序建立的肿瘤突变指数(TMI)模型能否用于筛选对化学治疗多西他赛或免疫治疗阿替利珠单抗单药治疗响应的NSCLC患者。
研究设计:
POPLAR临床试验(NCT01903993)和OAK(NCT02008227)临床试验不仅证实了免疫*制剂抑**阿替利珠单抗临床治疗PD-L1高表达NSCLC患者疗效显著优于化学治疗多西他赛,而且还提供了丰富的伴随诊断数据(ctDNA高通量测序数据)。本研究基于上述两个研究的伴随诊断数据筛选出三个生物标志物:即血液肿瘤突变负荷(bTMB)、血液敏感突变肿瘤突变负荷(sbTMB)和不利突变评分(UMS)。在整合了三个独立生物标志物的优缺点及其结合临床特征后建立了TMI模型,并基于该模型作为生物标志物筛选接受多西他赛或阿替利珠单抗单药治疗后在总生存期(OS)方面可能获益的NSCLC患者。
研究发现:
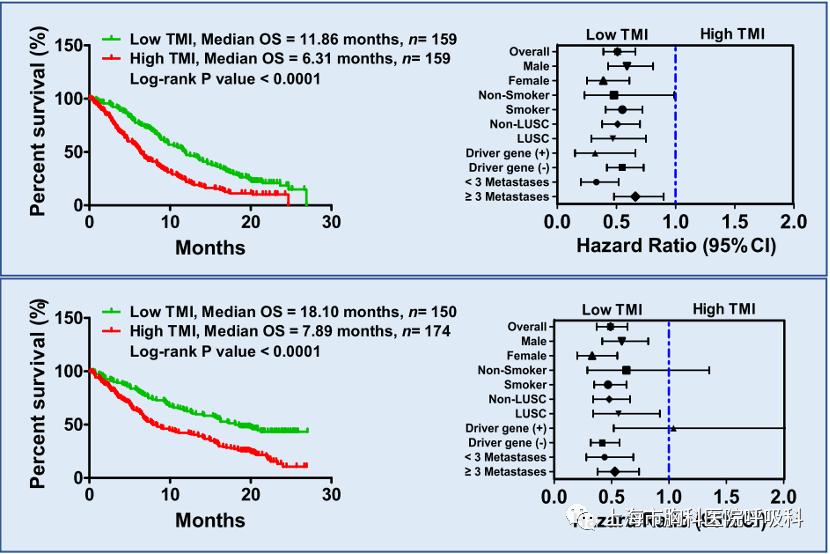
团队首先使用TMI模型作为生物标志物在OAK队列(Discovery cohort)中对接受多西他赛治疗的NSCLC患者进行响应分层。采用TMI中位法分析结果显示:Low TMI的患者(响应者)中位OS是11.86月,High TMI的患者(非响应者)中位OS是6.31月,响应者OS持续时间比非响应者长5.55个月(P值小于0.0001),且风险比(HR)显著降低。除此之外,TMI模型作为生物标志物也在OAK队列(Discovery cohort)中对接受阿替利珠单抗治疗的NSCLC患者进行响应分层。结果显示:Low TMI的患者(响应者)中位OS是18.10月,High TMI的患者(非响应者)中位OS是7.89月,响应者OS持续时间比非响应者长10.21个月(P值小于0.0001),且HR显著降低。
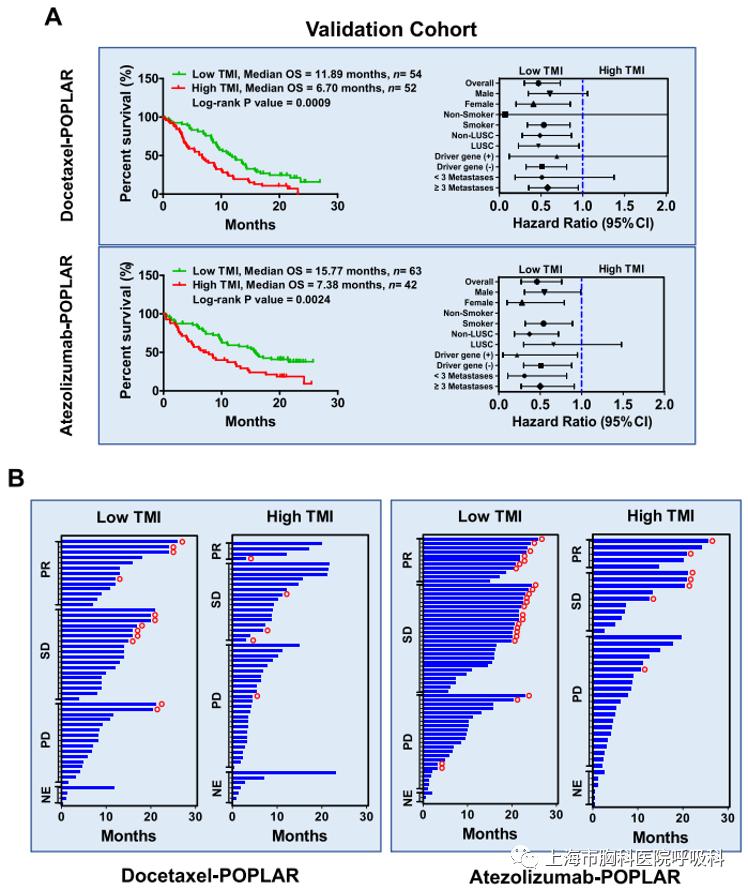
使用POPLAR队列作为生物标志物TMI预测疗效的验证集(Validation cohort)。结果显示:
在接受多西他赛治疗的NSCLC患者中,Low TMI的患者(响应者)中位OS是11.89月,High TMI的患者(非响应者)中位OS是6.70月,响应者OS持续时间比非响应者长5.19个月(P值等于0.0009),且HR显著降低;在接受阿替利珠单抗治疗的NSCLC患者中,Low TMI的患者(响应者)中位OS是15.77月,High TMI的患者(非响应者)中位OS是7.38月,响应者OS持续时间比非响应者长8.39个月(P值等于0.0024),且HR显著降低。该模型很好的在验证集中验证TMI对多西他赛或阿替利珠单抗单药治疗响应患者及非响应患者筛选的有效性。
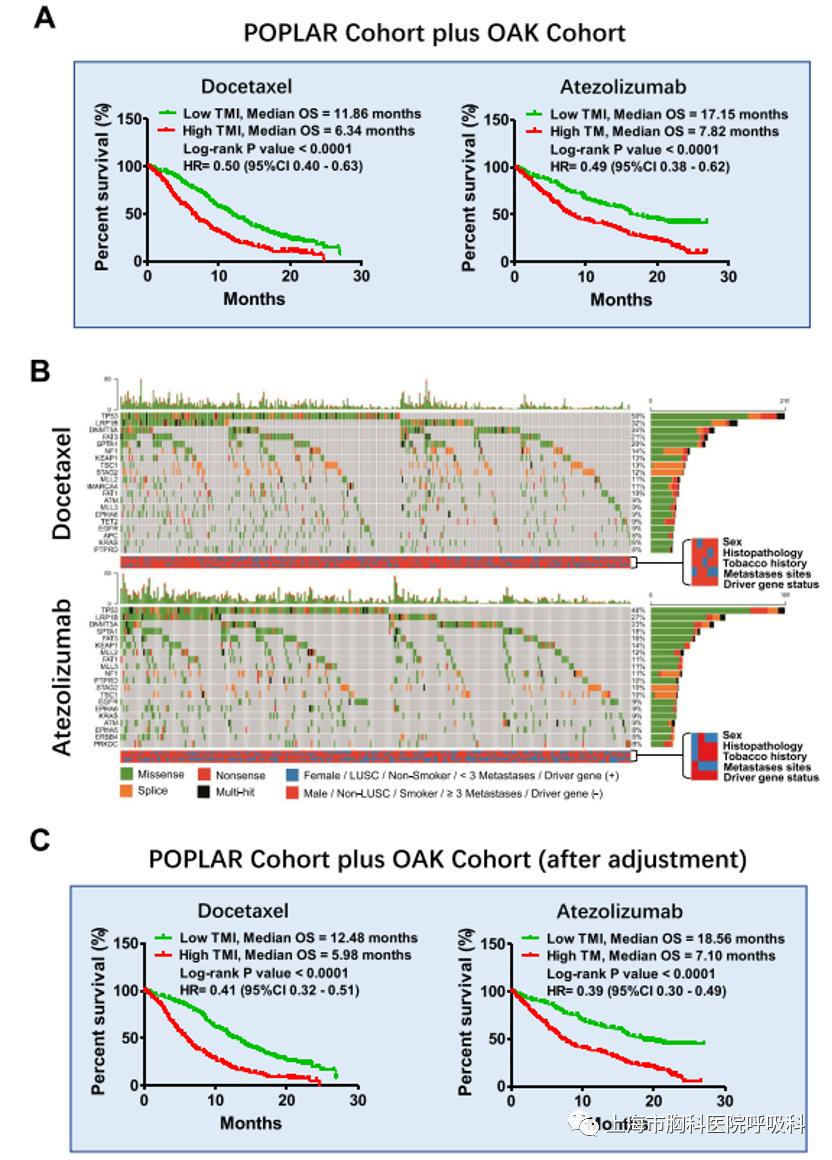
此外,该研究还整合相关数据对TMI模型进行校正。校正前TMI在POPLAR和OAK总人群中筛选响应患者的效果已经十分理想,即在接受多西他赛治疗的NSCLC患者中,Low TMI的患者(响应者)中位OS是11.86月,High TMI的患者(非响应者)中位OS是6.34月,响应者OS持续时间比非响应者长5.52个月(P值小于0.0001,HR= 0.50);在接受阿替利珠单抗治疗的NSCLC患者中,Low TMI的患者(响应者)中位OS是17.15月,High TMI的患者(非响应者)中位OS是7.82月,响应者OS持续时间比非响应者长9.33个月(P值小于0.0001,HR= 0.49)。
校正后TMI在POPLAR和OAK总人群中筛选响应患者的效果更加优秀,即在接受多西他赛治疗的NSCLC患者中,Low TMI的患者(响应者)中位OS是12.48月,High TMI的患者(非响应者)中位OS是5.98月,响应者OS持续时间比非响应者长6.50个月(P值小于0.0001,HR= 0.41);在接受阿替利珠单抗治疗的NSCLC患者中,Low TMI的患者(响应者)中位OS是18.56月,High TMI的患者(非响应者)中位OS是7.10月,响应者OS持续时间比非响应者长11.46个月(P值小于0.0001,HR= 0.39)。
研究结论:
在本研究中,该团队建立了一种新的TMI模型用于在多西他赛或阿替利珠单抗二线单药治疗的NSCLC患者中筛选出对治疗方案响应的患者。相信TMI模型在未来有可能被用于指导NSCLC治疗的临床实践。
译者:李雨婧 硕士研究生
导师:张伟 上海市胸科医院呼吸内科 主任医师
参考文献:Lu, J., Wu, J., Lou, Y., Shi, Q., Xu, J., Zhang, L., ... Chu T., Zhong H. & Han, B. (2022). Blood-based tumour mutation index act as prognostic predictor for immunotherapy and chemotherapy in non-small cell lung cancer patients. Biomarker Research, 10(1), 55. doi: 10.1186/s40364-022-00400-5.