在女性恶性肿瘤中,宫颈癌是第二位导致女性死亡的恶性肿瘤,每年新增病例超过50万例。
宫颈癌按照组织学分类,可分为鳞状细胞癌、腺癌和腺鳞癌。
宫颈癌人类肿瘤中唯一病因可知的恶性肿瘤,人类乳头瘤病毒(HPV)感染已被证实是90%子宫颈癌发生的重要前提,HPV-16 和 HPV-18 是导致宫颈上皮细胞恶性转化的重要驱动因素问。
HPV-16与约80%的宫颈鳞状细胞癌相关,HPV-18与20%的宫颈腺癌相关。
虽然大部分的宫颈癌可通过定期的检查和早期处理癌前病变来防止发生,但宫颈癌仍然是发展中国家女性癌症死亡的主要原因。
对于宫颈癌的临床治疗,可以采用各种治疗方法,如手术、放化疗9以及靶向治疗O和免疫治疗等等多种策略。
宫颈癌的手术治疗仅适用于非常早期(IA-IIA)的宫颈癌患者,放疗或同步放化疗是局部晚期 (IIB-IVA)或复发患者的主要治疗方法。
化学药物可以通过静脉注射或口服方式进行治疗。
这些药物进入血液,可以扩散至身体的所有部位,因此这种治疗方法有助于杀死身体大部分部位的癌细胞。
近年来,开发出药物递送系统以及基于实现更好的临床反应和耐受性的概念的抗癌药物。
从药代动力学角度,尤其是药物分布方面,这些可能会导致抗癌药物在作用部位的生物利用度降低,以及限制最大耐受剂量的高器官毒性。
虽然在化疗方面有所进展,但是对于那些有转移性肿瘤患者和复发或持续性疾病状态的患者,其治疗方法的选择仍然有限。
许多化疗药物在晚期和转移性宫颈癌中显示了作用,其中包括顺铂、卡铂、紫杉醇、异环磷酯胺和拓扑替康。
在所有的化学治疗方案中,顺铂被认为是治疗晚期宫颈癌最有效的化疗药物。
其功能是通过与抑制基因转录的DNA形成加合物直接相互作用,从而导致肿瘤细胞内的诱导氧化应激和凋亡。
但是,其在临床上使用受限,主要是因为肿瘤耐药性和其他一些严重的不良反应,如血小板减少、中性粒细胞减少、肾毒性、神经毒性、血液毒性引起的贫血和骨髓抑制。
对于复发或有转移的患者,使用顺铂、紫杉醇药物为基础的化疗以及肿瘤血管靶向药物如贝伐单抗(靶向血管内皮生长因子,VEGF)已被美国食品和药物管理局 (FDA) 批准为一线治疗药物。
然而,基于顺铂类药物的化学疗法通常会引起肿瘤耐药性,而目前的一些新疗法如VEGF 靶向治疗和免疫治疗等对其效果有限。
例如,在 KEYNOTE-158试验中,PD-1*制剂抑**在总人群中的客观应答率(ORR)仅为 12.2%。
因此,迫切需要开发新的策略来提高宫颈癌的治疗效率。

纳米技术在宫颈癌治疗中的应用
纳米粒子作为抗肿瘤药物载体
近年来,纳米载体因为其独特的结构、成分多样和表面性质等特点,将治疗药物包封在纳米载体中可以促进药物的持续释放、系统分布和良好的吸收效率,基于纳米载体的给药系统成为了国内外研究的热点之一。
它们是一类有良好药物作用的靶向载体,最常见的结构包括脂质体、聚合物、树状大分子和无机材料(金属或非金属) 等。
这些纳米粒子的尺寸通常在10 nm到150 nm之间,保证了药物在肿瘤细胞内的聚集增加,循环周期的延长。
直径小于10 nm的纳米粒子可以被肾脏迅速清除,而直径大于150 nm的纳米颗粒则有被巨噬细胞识别和清除的风险。
将化疗药物封装在纳米载体中具有许多优点,例如防止血液中的降解,增强药物稳定性、靶向给药、降低毒副作用和增加药物的生物利用率。
另外,纳米颗粒也可以被设计为能够在一定时间内以预定的速率递送治疗药物的可控制和/或持续的药物释放系统。
控制药物递送系统可以降低患者药物治疗的时间需求,从而提高患者的依从性。

有研究认为,长期释放的控释制剂会增加药物的局部浓度,从而改善化疗的治疗效果。
人类癌症细胞系无论是在体外还是在体内进行异种移植,都是研究治疗方法在癌症治疗中的疗效的基本模型。
Hela是第一个培养的宫颈癌细胞系。
从那时起,建立了包括 SiHa、CaSki、C-33A和ME-180 在内的多个宫颈癌细胞系。
然而,由于这些细胞系与肿瘤模型相比并不具有同样的作用,因此在体外实验中,药物疗效的结果也不尽相同。
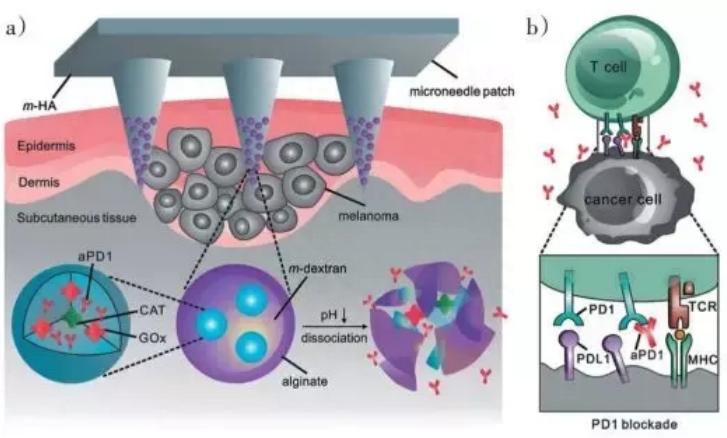
脂质体纳米粒子给药系统
目前研究最多的纳米载体之一是脂质体,脂质体是由脂质双层和水核组成的球形囊泡。
水溶性的药物被包裹在水性核心中,而脂质双层则包覆缠绕在脂溶*药性**物上。
脂质体可以负载亲水性和疏水性的药物,例如用于治疗癌症的化疗药物和免疫细胞因子。为了实现药物的靶向递送,可以在脂质体表面连接针对肿瘤细胞受体的特定配体。
脂质体由于其灵活的性质,如zeta电位、粒径和控释速率,可以克服膜介导的屏障,用于输送化疗药物。
脂质载体在通过亲脂性/亲水性和EPR效应提高药物的渗透性和缩短全身给药周期方面具有优热。

聚合物纳米粒子控制性释放抗肿瘤药物
生物可降解聚合物纳米粒子由于其具有高载药量、自稳定性、高细胞摄取能力、更理想的生物分布以及可以同时递送亲水性和疏水*药性**物的能力,已成为肿瘤药物递送领域相当热门的重要研究课题。
聚合物纳米颗粒(PNPs)由具有核壳结构的聚合物组成,如聚硫酷、聚丙烯酸酷和明胶,直径在几十到几百纳米之间。
PNPs作为治疗宫颈癌的药物载体,具有灵活的控释特性、对TME(肿瘤微环境) 的响应性以及可以提高不溶性抗癌药物的溶解度。
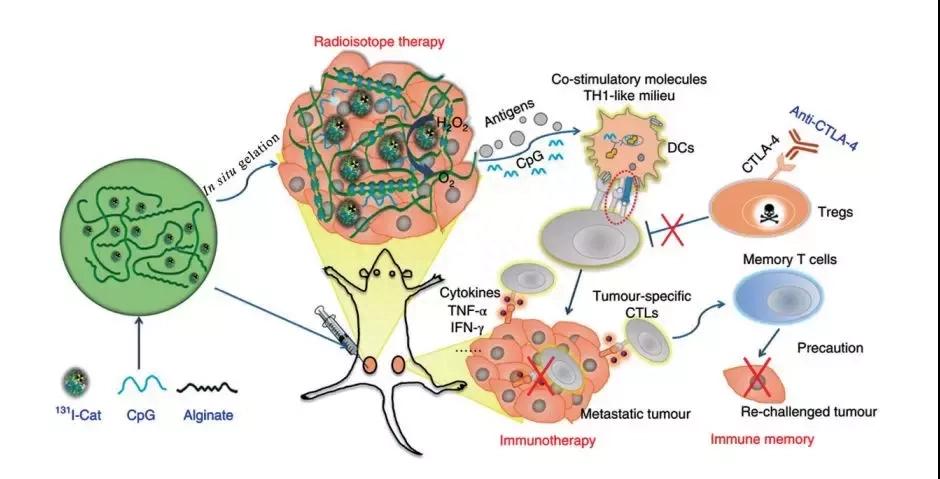
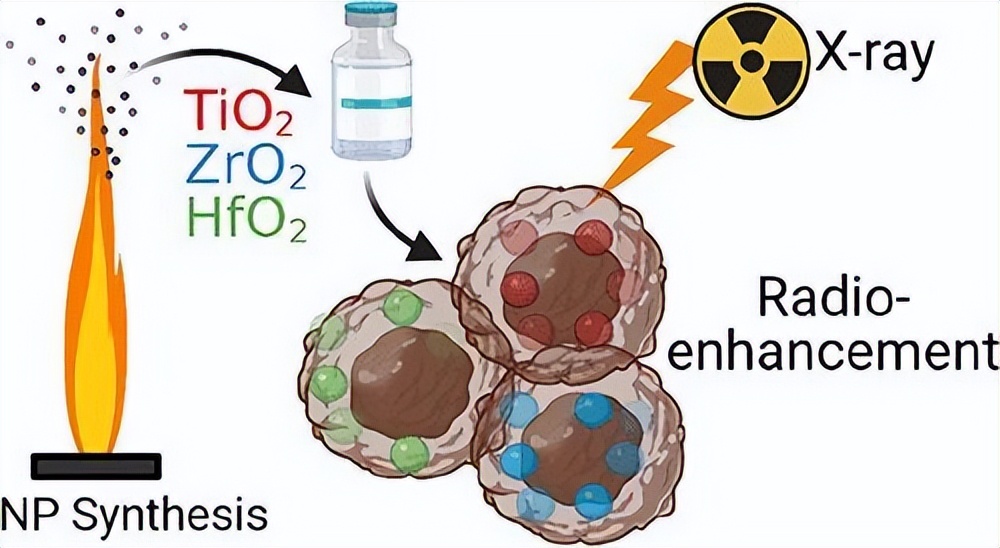
无机物作为药物载体的应用
无机纳米载体可被分为几种类型,包括非金属载体,如氧化石墨烯(GO)氧化硅或碳,以及金和铜等金属载体。
目前,多种无机材料已被用作基因或药物载体,具有更有效的细胞摄取和更高的分散性。
然而,低降解率和潜在毒性的特点也是不容忽视的问题,对其进行结构优化,是确保内部降解和安全清除的必要条件。
金属纳米颗粒(NPs)由于具有一些独特的优点,例如易于合成、简单的表面化学和功能化、广泛的光学性质和表面体积比高等。
有报道称NP对某些细胞系具有抗肿瘤效力。
它们的有效性来自于它们与细胞的相互作用,细胞的摄取导致活性氧物种产生的氧化应激,因为NPs很容易穿过核膜并直接或间接与 DNA相互作用,通过一种仍然未知的机制与细胞内大分子(如 DNA 和蛋白质)发生反应。

纳米 CRISPR 系统实现靶向基因治疗
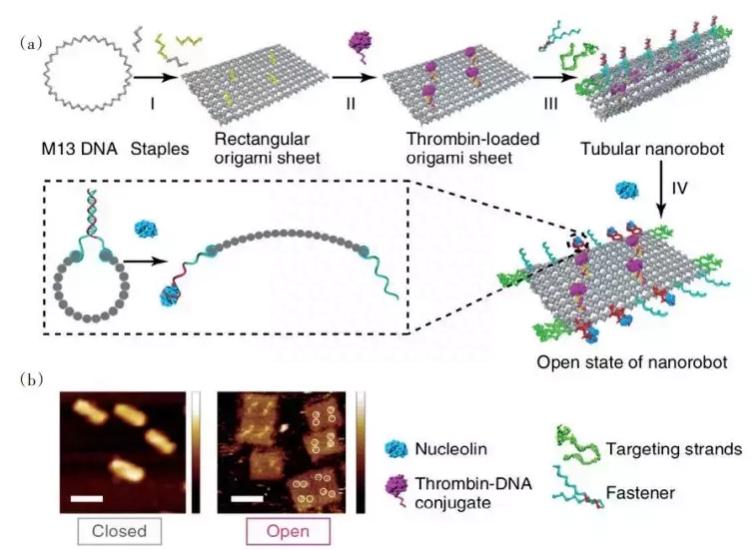
最近几年来,由于纳米粒子和新兴的基因组编辑方法相结合,如聚集的有规则的间隔短回文重复序列(CRISPR)等,使宫颈癌的靶向性治疗得到了创新性的发展。
CRISPR系统源自细菌的自身产生的适应性免疫防御系统,包含Cas9内切酶和单导向RNA (sgRNA),sgRNA可以引导Cas9向前移动,然后瞄准特定序列。
CRISPR 基因的编辑过程主要通过三个系统组成: gRNA核糖核蛋白 (RNP)、质粒和mRNA系统。
最常用的RNP系统可以在不需要转录和翻译过程的情况下,简化编辑步骤和过程,但可能会造成内毒素污染,降低效率,影响工作的进行。
与RNP系统相比,质粒系统具有更好的稳定性、更经济,然而,其较大的尺寸是质粒递送和靶向递送中的不可忽视的障碍。
mRNA系统是一种降低脱靶率的替代方法,但本质上较不稳定。
虽然病毒载体和物理载体在减少降解和确保精确靶向方面都得到了广泛的验证,但由于其强大的免疫原性、增加某些癌症的风险和复杂的作用过程,病毒载体的临床应用受到了限制。
与此形成对比的是,无机和脂质纳米载体等非病毒运载系统有巨大的前景有很好的应用潜力。
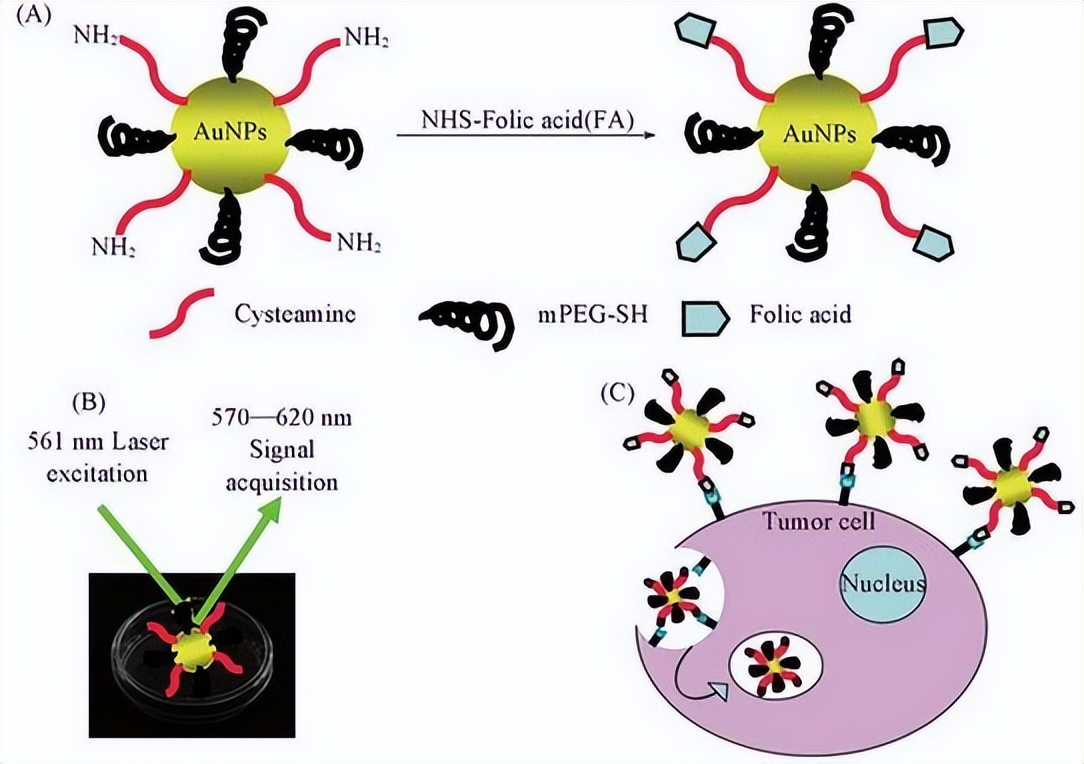
例如,正如之前所提到的,AuNP 具有特殊的物理和化学特性,可以应用于定向输送。
学者开发了-种pH依赖的自组装 AuNP,通过将Cas-9导入细胞核,然后敲除E6基因来恢复 p53 在细胞中的表达水平。
此外,还建立了另一种由聚环氧丙烷和两亲性嵌段共聚物组成的自组装胶束来封装质粒 CRISPR 体系。正如预期的一样,胶束-E7-Cas-9系统在HeLa细胞异种移植模型中完全诱导E7 敲除并显著抑制细胞活性。
此外,通过p16免疫组化染色实验确认,肿瘤消退的残留部分可由基质细胞取代。因此,脂质CRISPR平台对于体内基因组编辑是有效的。
纳米载体与 CRISPR的结合可能是近期宫颈癌靶向基因治疗的一种有前景的方法。