中华医学会消化内镜学分会外科学组, 中华医学会消化内镜学分会经自然腔道内镜手术学组, 中国医师协会内镜医师分会消化内镜专业委员会, 等. 中国消化道黏膜下肿瘤内镜诊治专家共识(2023版)[J]. 中华消化内镜杂志, 2023, 40(4): 253-263. DOI: 10.3760/cma.j.cn321463-20230310-00039
摘要
2018年由复旦大学附属中山医院牵头,组织专家共同制订了《中国消化道黏膜下肿瘤内镜诊治专家共识(2018版)》,该共识是国内首部关于消化道黏膜下肿瘤内镜诊治的专家共识,一经发布在国内外取得强烈反响,在日常工作中规范了我国消化道黏膜下肿瘤内镜诊治流程。近年来消化内镜学飞速发展,五年来在超声内镜诊断、内镜切除及缝合方面已取得长足的进步。为了更好地服务临床,结合国内外内镜诊疗的新理念、新技术、新经验,制定新的消化道黏膜下肿瘤内镜诊治专家共识已迫在眉睫。因此,由复旦大学附属中山医院内镜中心牵头,成立了共识更新工作组,在原有共识的基础上对近年新的证据结果进行分析并形成相关推荐意见,以期为从事消化道黏膜下肿瘤诊治相关工作的临床医师及基层医疗机构等相关工作人员提供参考和指导。
关键词
消化系统肿瘤; 消化道黏膜下肿瘤; 内镜诊治; 专家共识
随着于内镜和超声内镜(endoscopic ultrasonography,EUS)检查技术的发展与成熟,以及居民健康意识的增强,消化道黏膜下肿瘤(submucosal tumors,SMT)的检出率大幅提高。为了规范内镜微创治疗SMT,从而改善SMT患者生活质量、减轻家庭和社会负担、节约国家医疗资源,2018年由复旦大学附属中山医院牵头,制订了SMT内镜诊治共识意见——《中国消化道黏膜下肿瘤内镜诊治专家共识(2018版)》。为了更好地服务临床,本版更新主要结合国内外内镜诊疗的新理念、新技术、新经验,在原有共识的基础上对近年新的证据结果进行分析并形成相关推荐意见,以期对内镜诊治SMT临床决策的制订提供具有参考价值的推荐意见。
一共识更新流程
本共识由复旦大学附属中山医院内镜中心牵头,成立共识更新工作组启动共识的更新工作,在《中国消化道黏膜下肿瘤内镜诊治专家共识(2018版)》的基础上对国内外内镜诊疗的新理念、新技术、新经验进行评价形成相关推荐意见,使其更加符合中国国情及医疗现状。
1.专家共识发起机构与专家组成员:本共识由中华医学会消化内镜学分会外科学组、中华医学会消化内镜学分会经自然腔道内镜手术学组、中国医师协会内镜医师分会消化内镜专业委员会、中华医学会外科学分会胃肠外科学组发起,共识更新启动时间为2022-09-20。
2.临床问题的遴选和确定:共识更新工作组通过系统查阅国内外SMT内镜诊治领域已发表的系统评价和指南,初步拟定了13个临床问题。第1轮问卷调查邀请全国107位专家对拟定临床问题进行重要性评价,并通过共识指导委员会会议,最终遴选出本共识拟解决的问题。
3.证据的检索:共识更新工作组成立了证据检索与评价小组,针对最终纳入的关键临床问题进行中英文数据库检索,检索截至2022-09-30。具体检索数据库包括PubMed、Web of Science、中国知网、万方数据库,同时利用数据库的相似文献功能追踪SMT相关综述和系统评价或Meta分析的参考文献,继续补充检索。
4.推荐意见的形成:专家组针对基于证据检索与评价小组提供的临床问题进行系统评价,并基于证据给出推荐意见,同时考虑我国患者的偏好与价值观、干预措施的成本和利弊后,提出了符合我国诊治实践的推荐意见,于2022年12月进行第二轮德尔菲法推荐意见调查,收集到50位专家反馈建议并进一步修改,形成本共识文本的推荐意见(表1)。
二关键问题及推荐意见
(一)SMT流行病学特征
问题1:SMT在消化道不同部位的发病率和病理类型。 推荐意见:(1)SMT在消化道各部位的发病率不均衡,胃是SMT最好发部位。 (98%的专家赞同) (2)SMT的组织病理学类型复杂,但大多SMT为良性病变,仅少部分表现为恶性。 (100%的专家赞同)
SMT是起源于黏膜肌层、黏膜下层或固有肌层的隆起性病变,也可以是腔外病变。国外指南较常应用胃肠道上皮下肿瘤(subepithelial lesions,SEL)这一术语。一般情况下,<2 cm的SMT多无明显的临床症状,多在内镜体检中偶然发现。但一部分特殊类型或特殊部位的病变,随着疾病的进展和病变的增大,也可发生腹痛、出血和梗阻等症状。国外的研究表明,在常规内镜检查中,每300例就能发现1例SMT。近年来,由于内镜检查的普及和EUS检查技术的发展与成熟,SMT的检出率也在不断上升。
SMT在消化道各部位的发病情况不均衡,以上消化道较为多见。其中,2/3发生在胃部,其次是食管、十二指肠和结肠。SMT包括异位胰腺组织等非肿瘤性病变和肿瘤性病变。在肿瘤性病变中,胃肠道平滑肌瘤、脂肪瘤、布氏腺瘤、颗粒细胞瘤、神经鞘瘤和血管球瘤等多表现为良性,仅少于15%的可表现为组织学恶性。SMT中胃肠道间质瘤(gastrointestinal stromal tumors,GIST)和神经内分泌肿瘤(neuroendocrine tumors,NET)是具有一定的恶性潜能的肿瘤,但这取决于它的大小、位置和分型。据文献报道,<2 cm的胃GIST,无论其有丝分裂指数多少,其转移风险较低,而病变大小为3~5 cm时,在有丝分裂指数较低的情况下,其转移风险增加到3%,在有丝分裂指数较高的情况下增加到16%;而在小肠中,有丝分裂指数较高的情况下,无论病变大小,GIST的转移率高达50%。Ⅰ型和Ⅱ型小于1~2 cm的胃NET,通常分化良好,有丝分裂指数低,很少转移;Ⅲ型分化程度较低,具有一定的侵袭性。
不同类型SMT的好发部位与其组织病理学有一定的相关性,因此,SMT的发生部位在临床诊断中也具有一定的意义。平滑肌瘤是食管常见的SMT病理类型,占食管SMT的60%~80%,好发于食管中下段。胃SMT病理类型较为复杂,以GIST、平滑肌瘤和异位胰腺较为多见。胃SMT中,GIST最常见于胃底和胃体,平滑肌瘤通常在贲门和胃体上部,异位胰腺和脂肪瘤多见于胃窦部。在十二指肠降部和球部,脂肪瘤和囊肿较为多见。下消化道SMT中,在结肠以脂肪瘤为主,而在直肠以NET为主。对于SMT的诊治要综合其组织学类型、位置、大小和症状以及患者自身情况。
(二)SMT术前检查和评估
问题2:单独使用常规白光内镜评估SMT的效果。 推荐意见:常规白光内镜用以观察病变位置、大小、活动度、隆起部位黏膜的色泽、形态、糜烂出血情况,无法提供病变性质和来源相关信息,不推荐单独使用常规白光内镜作为SMT的术前检查。 (100%的专家赞同)
常规白光内镜是检测SMT的基础和起点,可以提供病变位置、大小、活动度、黏膜色泽、形态、糜烂出血情况等信息,但其无法判断病变的性质和来源,尤其是表现出外生性生长模式的SMT,不能单独通过常规白光内镜诊断。对于具有特殊特征的SMT,结合其好发部位和特征性颜色及表现,提高基于其内镜特征诊断SMT的能力并制订下一步诊疗方案对内镜医生来说也至关重要。例如,当SMT呈淡黄色时,可考虑为脂肪瘤或颗粒细胞瘤;呈蓝色时,可考虑为血管瘤;当SMT具有明显的液体成分时,可考虑囊肿的诊断;当SMT有明确的开口、脐孔和(或)中央凹陷时,可考虑为异位胰腺;当SMT表现为糜烂或溃疡时,其为恶性病变的可能性增加。
问题3:白光内镜联合EUS评估SMT的效果。 推荐意见:EUS可以在常规白光内镜的基础上观察病变的内部回声、来源、异质性、生长方式和血管的关系等,可以初步提供病变的良恶性信息。推荐所有SMT患者在自愿的前提下采用常规白光内镜联合EUS作为术前检查。 (98%的专家赞同)
EUS是诊断SMT的一线检查方法,可以提供病变来源、壁内或壁外位置、大小和形状、回声、血管和相关淋巴结病变的信息。通过这些特征,我们可以评估组织学甚至恶性潜能。EUS能够以92%的敏感度区分腔外压迫和腔内的病变,其对GIST诊断的准确率为77%~89%。一项回顾性研究比较了EUS与CT诊断SMT的准确率,结果提示EUS和CT对GIST的诊断准确率分别为83.9 %和74.2 %,对平滑肌瘤的诊断准确率分别为37.5 %和0.0 %,对异位胰腺的诊断准确率分别为57.1%和14.3%,EUS的诊断准确率均高于CT。但EUS诊断也具有一定的局限性,对胃小SMT的鉴别诊断准确性较差,诊断准确率仅为45.5%~48.0%。同时,EUS仅能显示肿物的某一个截面,该截面显示出的肿物起源层次可能与其他截面不符合;其次,EUS对操作者的操作手法和经验要求较高,操作熟练的医师和有经验的专家才能达到较高的EUS诊断准确率。人工智能在医学图像诊断领域显示出了卓越的性能,在辅助诊断SMT中也有一定的价值,内镜专家通过EUS图像诊断GIST的准确率为73.3%~75%, 而非专家的准确率仅为54.9%,人工智能的诊断准确率高于内镜专家,但其在临床实践中的应用和涉及的医学伦理有待进一步深入研究。
问题4:其他影像学检查评估SMT的价值。 推荐意见:(1)通过CT和MRI对肿瘤进行分级、治疗和预后评估,对怀疑潜在恶性或瘤体较大(长径>2 cm)的SMT,建议CT和MRI评估。 (94%的专家赞同) (2)EUS弹性成像和对比增强EUS(contrast‑enhanced endoscopic ultrasonography, CE‑EUS)作为新兴的鉴别GIST的检查手段,是具有发展前景的诊断模式,常规检查中不做推荐。 (96%的专家赞同)
包括CT和MRI在内的其他影像学手段对SMT的诊断也具有重要意义,能直接显示肿瘤发生的部位、生长方式、病灶大小、形态、有无分叶、密度、均质性、强化程度以及边界轮廓等,并能发现胃肠壁是否增厚及增厚的程度。更重要的是,这些影像学检查能发现病灶邻近结构有无侵犯以及周围腹膜、淋巴结和其他脏器有无转移,是临床对肿瘤进行分级、治疗和预后评估的主要方法。虽然CT在SMT诊断准确率方面低于EUS,但与EUS相比,对于较大瘤体,CT可清晰显示肿瘤的整体情况,在EUS的基础上可作为诊断SMT的一种补充手段。
随着EUS技术的发展,EUS弹性成像和CE‑EUS等附加技术也显示出了提高EUS诊断性能的潜力。2012年一项包含17例胃或食管黏膜下病变患者的初步研究中,8例GIST均表现为CE‑EUS高增强,而9例脂肪瘤和平滑肌瘤表现为低增强,初步揭示了CE‑EUS在鉴别GIST与良性SMT中的潜在价值。目前研究提示以CE‑EUS高增强作为诊断GIST的准确率为82%~98%,但在这些诊断分析中,增强程度是由观察者主观决定的。因此,需要进一步评估这种非侵入性方法鉴别GIST的实用性。EUS弹性成像是根据目标病灶的硬度,通过显示彩色频谱进行诊断。研究显示,GIST相较于其他SMT硬度更硬,在弹性成像中倾向于显示蓝色,但与平滑肌瘤的鉴别仍较为困难。随后的研究发现以应变率比值作为评价指标,可将平滑肌瘤与GIST相鉴别,且具有良好的敏感度和特异度。EUS弹性成像和CE‑EUS作为新兴的鉴别GIST的检查手段,具有发展前景,但需要进一步的大规模临床研究证实其有效性。
问题5:SMT活组织病理学检查的必要性和评估效果。 推荐意见:不推荐对可通过常规内镜联合EUS确诊的良性SMT,如脂肪瘤、囊肿和异位胰腺等进行组织取样。对怀疑恶性的病变或常规内镜联合 EUS 无法对病灶良恶性进行评估时,可采用EUS引导细针穿刺抽吸术/活检术(endoscopic ultrasonography guided fine needle aspiration/biopsy,EUS‑FNA/FNB)、黏膜切开活检(mucosal incision‑assisted biopsy, MIAB)等进行活组织取样从而进行术前病理评估。鉴于EUS‑FNA的局限性和后续对内镜切除手术的影响,对于符合内镜下手术适应证者,在保证肿瘤可完整切除的前提下,可在内镜治疗技术成熟的单位,由经验丰富的内镜医师直接内镜下切除,无需获取术前病理诊断。 (94%的专家赞同)
组织病理学检查是确诊SMT的金标准,由于SMT被正常黏膜覆盖,常规内镜活检技术难以获取足够的组织样本,采用同一部位多次活检,虽能获得深部病变组织,但出血风险增加,并且获得的组织也可能不足以用于明确诊断。因此,相继出现了其他针对SMT组织病理检查的方法,例如MIAB、EUS‑FNA、EUS‑FNB等。EUS‑FNA和EUS‑FNB的诊断准确率为46%~93%,其准确率因病灶大小等因素而异。EUS‑FNA对大小为2 cm和2~4 cm的病灶诊断准确率分别为71%和86%,而在>4 cm的病灶中诊断准确率为95%~100%。对于<2 cm的病灶,EUS‑FNA/FNB可能由于取材不足导致无法获得准确的病理学诊断。一项meta分析报道对于小SMT,MIAB表现出了更好的诊断准确率,诊断准确率为89%(95% CI :82.65%~93.51%, I2=0.00%)。
值得注意的是,任何一种术前获取病理标本的方式都具有侵入性,会损伤黏膜或造成与黏膜下组织粘连,从而增加手术难度,还可能增加出血穿孔、肿瘤播散等风险,因此术前活检不一定是必要的,尤其对于可通过常规内镜结合EUS确诊的SMT,如脂肪瘤、囊肿和异位胰腺等,无需组织取样。另外,对于符合内镜下手术适应证的潜在恶性的SMT,由经验丰富的内镜医师经过术前评估,在保证肿瘤可完整切除的前提下,可在内镜治疗技术成熟的单位由经验丰富的内镜医师直接内镜下切除,术前可不做病理诊断。
(三)SMT的内镜下治疗
问题6:内镜治疗SMT的原则。 推荐意见:没有淋巴结转移或淋巴结转移风险极低、使用内镜技术可以完整切除、残留和复发风险低的病变,有治疗必要的均适合进行内镜下切除。完整切除肿瘤可以最大限度降低肿瘤残留和复发风险。内镜切除过程中应遵循无瘤治疗原则,切除过程中应保证瘤体包膜完整。 (100%的专家赞同)
问题7:内镜治疗SMT的适应证和禁忌证。 (1)内镜下切除的适应证 推荐意见:①对于术前检查怀疑或活检病理证实存在恶性潜能的肿瘤,特别是对于术前评估肿瘤长径≤2 cm疑似GIST且复发转移风险低并可能完整切除的可内镜下切除;对于肿瘤长径>2 cm的疑似低风险GIST,术前评估除外淋巴结或远处转移者,在保证肿瘤可完整切除的前提下,可考虑在内镜治疗技术成熟的单位由经验丰富的内镜医师开展内镜下切除。 (100%的专家赞同) ②有症状(如出血、梗阻)的SMT。 (84%的专家赞同) ③术前检查怀疑或病理证实良性,但患者不能规律随访或随访期内瘤体短时间增大及内镜治疗意愿强烈的患者。 (94%的专家赞同) (2)内镜下切除的禁忌证 推荐意见:①明确发生淋巴结或远处转移的病变。 (98%的专家赞同) ②对于部分明确发生淋巴结或远处转移的SMT,为获取病理需大块活检,可视为相对禁忌证。 (100%的专家赞同) ③经过详细的术前评估,确定为一般情况差、无法耐受内镜手术者。 (96%的专家赞同)
脂肪瘤、异位胰腺等良性病变一般不会引起疼痛、出血、梗阻等症状。而当SMT表现为糜烂、溃疡,或短时间内迅速增大时,其为恶性病变的可能性增加。所有的GIST都具有恶性潜能,目前西方指南仅推荐对于有症状的GIST、≥2 cm的GIST或具有高危特征的GIST行手术切除。一大型流行病学研究提示,<2 cm的GIST患者与无论任何大小的GIST接受手术切除治疗的患者相比,疾病特异性死亡率没有显著差异。结合临床实践,内镜和EUS作为侵入性的检查,部分患者随访依从性较低,对于这类不能规律随访及内镜治疗意愿强烈的患者,可以进行内镜下治疗。
问题8:SMT内镜切除方式的选择。 推荐意见:(1)内镜圈套切除术:对于较为表浅、术前EUS和CT检查确定突向腔内且通过圈套器可以一次性完整切除的SMT,可采用内镜圈套切除。 (98%的专家赞同) (2)内镜黏膜下挖除术(endoscopic submucosal excavation, ESE):对于长径≥2 cm的SMT或术前EUS和CT等影像学检查确定肿瘤突向腔内,内镜圈套切除困难的SMT,可行ESE。 (100%的专家赞同) (3)经黏膜下隧道内镜肿瘤切除术(submucosal tunneling endoscopic resection, STER): 对于食管、贲门、胃体小弯、胃窦和直肠等易于建立隧道部位的固有肌层来源SMT,横径≤3.5 cm者,STER可作为首选的治疗方式。 (100%的专家赞同) (4)内镜全层切除术(endoscopic full‑thickness resection, EFTR):对于难以建立隧道部位的SMT或肿瘤最大横径>3.5 cm不适合STER者,肿瘤突向浆膜下或部分腔外生长、术中发现瘤体与浆膜层紧密粘连而无法分离者可选用EFTR进行内镜下治疗。 (94%的专家赞同)
对于内镜圈套切除术切除SMT,国内外研究已证实其在<2 cm的浅表SMT中是安全有效的,其出血风险为4%~13%,穿孔风险为2%~7%。
ESE沿用了内镜黏膜下剥离术(endoscopic submucosal dissection, ESD)及内镜黏膜切除术的技术习惯,常规在肿瘤周边采用环形“掀盖”的切口以切除覆盖在SMT上方的黏膜,充分暴露肿瘤,达到保留肿瘤完整性、提高手术根治性、降低术中并发症的目的。文献报道ESE的完全切除率可达92%,对于≤1.5 cm的肿瘤,可达到100%的完全切除率;对于>1.5 cm的肿瘤,ESE完全切除率也可达到77.8%。
STER技术是在经口内镜下食管括约肌切开术(peroral endoscopic myotomy, POEM)基础上发展而来的一项新技术,也是ESD技术的延伸。STER治疗SMT的整块切除率达84.9%~97.5%。气体相关并发症是STER最常见的并发症,但这些并发症大多是轻微的,一般可自行吸收或经保守治疗后好转,术中全程应用CO2气体,可有效减轻气体相关并发症的严重性。
EFTR治疗SMT的完全切除率可达100%,且并发症发生率极低,仅有少数研究报道患者行EFTR后发生腹腔感染。EFTR后妥善缝合穿孔部位是EFTR成功的关键。为了准确评估肿瘤复发风险及减少肿瘤播散风险,不建议在EFTR过程中对切除的肿瘤标本进行切割后取出。如确需分块取出瘤体,则需先修复穿孔,以减少肿瘤种植播散风险。
金属夹缝合术是EFTR术中修补最为基础的缝合技术。内镜直视下应用金属夹自创面两侧向中央完整对缝创面。由于金属夹跨度有限,不能一次性将穿孔夹闭,适当吸引消化道腔内气体,充分缩小穿孔,利用多个金属夹夹闭穿孔,即“吸引-夹闭缝合”。如果创面较大,无法关闭,可负压吸引大网膜进入消化道腔,应用金属夹沿创面边缘夹闭大网膜和黏膜闭合创面,为“网膜垫(omental patch)缝合”技术。亦可换用双钳道内镜,一个钳道置入尼龙绳圈于穿孔创面切缘,经另一钳道置入多枚金属夹夹闭切缘黏膜组织和尼龙绳,最后收紧尼龙绳关闭创面,为尼龙绳结合金属夹的“荷包缝合”方法。近年来,也有采用耙状金属夹闭合系统(over the scope clip,OTSC)、OverStitch 缝合等新型技术修补消化道损伤和处理出血。同时,一种EFTR和缝合结合的全层切除装置(full thickness resection device,FTRD)开始应用于临床, 此装置头部安装了一个带圈套器的透明帽,透明帽上带有OTSC,手术过程中将病灶拉入透明帽切除病灶的同时缝合创面。在近期一项前瞻性多中心试点研究中,应用胃FTRD治疗胃SMT的完全切除率为89.7%,但31%的患者围手术期出现轻微出血。
问题9:内镜治疗SMT操作相关并发症定义。 推荐意见:(1)术中出血:导致患者血红蛋白下降20 g/L以上的出血。(2)术后出血:术后出血表现为呕血、黑粪或便血等,严重者可有失血性休克的表现,多发生于术后 1 周内,但也可出现于术后 2~4 周。(3)迟发性穿孔:通常表现为腹胀、腹痛加重、腹膜炎体征、发热,影像学检查有积气或积气较前增多。(4)气体相关并发症:包括皮下气肿、纵隔气肿、气胸和气腹等。(5)消化道瘘:因内镜手术造成的消化液经过漏道流入胸腔或腹腔。 (100%的专家赞同)
术中出血:为了预防术中大量出血,在手术过程中黏膜下注射要充分,可使较大血管显露,有利于电凝止血。术中出血可使用各种切开刀、止血钳或金属夹等治疗,剥离过程中对发现裸露的血管进行预防性止血。
术后出血:如出现呕血、黑便量较多、色较鲜艳、血红蛋白下降较明显等症状时,应及时行内镜检查,仔细观察创面,若发现有活动性出血,用热电咬钳或金属夹夹闭止血。术后出血往往与术后血压控制不佳、胃酸对残留血管的腐蚀等因素有关。此外,术后出血与病变的部位也有一定关系,多见于胃窦部和低位直肠。
迟发性穿孔:术后迟发性穿孔多与创面缝合不佳、过度电凝、过早起床活动、过早进食、血糖控制不佳、胃酸对创面的腐蚀等因素有关。为减少术后迟发性穿孔的发生,如创面大、深或者创面出现裂隙样改变,术后应适当延长卧床时间及禁食时间、胃肠减压(下消化道术后患者置肛管引流);对于糖尿病患者应严格控制血糖;对于穿孔较小、胸腹腔感染程度较轻者,给予禁食、抗感染、抑酸等治疗;对于积液者可进行胸腔闭式引流、腹腔穿刺置管等保持引流通畅;经保守治疗感染无法局限或合并严重的胸腹腔感染,则应尽早行外科腹腔镜手术探查,行穿孔修补、腹腔引流术。
气体相关并发症:术中皮下气肿(表现为面部、颈部、胸壁和阴囊等气肿)和纵隔气肿(胃镜可发现会厌部肿胀)常无需特殊处理,气肿一般会自行消退。术中发生严重气胸[手术过程中气道压力超过20 mmHg(1 mmHg=0.133 kPa),SpO2<90%,行急诊床旁胸片证实]者,予胸腔闭式引流后,常可继续手术。术中明显气腹者,通过气腹针于右下腹麦氏点穿刺放气并留置穿刺针至术毕,确认无明显气体排出时再拔除。
消化道瘘:常见食管纵隔瘘和食管胸腔瘘等,一旦瘘出现,行胸腔闭式引流等,保持通畅引流,并给予充分的营养支持,必要时可采用金属夹及各种闭合器械,或全覆膜可回收支架等方式堵塞瘘口。严重者需及时外科手术干预。
(四)SMT术后管理
问题10:内镜治疗SMT操作报告的书写规范。 推荐意见:术者应及时书写操作报告,详细描述操作过程中的发现和治疗方法、步骤及结果,如有必要还应描述操作过程中出现的特殊情况。 (100%的专家赞同)
对病变的描述:包括病变的位置、形态、大小、颜色、表面黏膜状态、边界、活动度、触感、距门齿或距肛门的距离。
操作过程的详细记录:采用的手术方式,手术过程中应用的器械,操作步骤按顺序详细记录。
术*特中**殊情况、特殊操作的描述:术中病灶相关特殊情况记录,如与肌层粘连情况等;术中操作过程相关的特殊情况记录,如术中并发症及处理情况;术中非操作相关特殊情况记录,如麻醉导致不良反应记录。
问题11:内镜治疗SMT后用药规范。 推荐意见:(1)术中全层切除、术后伴有全身感染、穿孔或免疫力低下者,可参考相关抗生素应用指南规范使用抗生素。(2)上消化道术后患者常规给予质子泵*制剂抑**(proton pump inhibitor, PPI),恢复进食后持续口服PPI和黏膜保护剂至术后6~8周,以促进创面修复。 (100%的专家赞同)
内镜治疗SMT后相关菌血症等鲜有报道,国外早期文献推荐对于囊性病变在EUS‑FNA前预防性使用抗生素,但缺乏前瞻性大样本的临床研究。近期国内的一项研究结果显示,对于胃ESD或ESE后无穿孔、无严重合并症患者的发热,无需应用抗生素。术后使用抗生素的目的在于预防手术创面周围的纵隔、后腹膜或游离腹腔的感染及术后可能发生的全身性感染。对于操作范围较大、操作时间长或并发消化道穿孔和大量出血者,或术后伴有全身感染及免疫力低下者,可根据患者情况,具体参考相关抗生素应用指南规范使用抗生素。
根据文献报道,ESD治疗后黏膜伤口处的血小板聚集和凝血功能强烈依赖于胃内pH值。先前的研究表明PPI在内镜治疗后伤口愈合和预防迟发性出血方面有一定的作用。同时,黏膜保护剂可以上调血管生长因子的表达,对伤口愈合也发挥促进作用。近期一项纳入156例患者的随机对照研究提示,PPI联合黏膜保护剂(瑞巴派特)在降低ESD后溃疡残留率方面的效果比单用PPI更佳。因此,对上消化道SMT患者内镜治疗后常规给予PPI,恢复进食后持续口服PPI和黏膜保护剂至术后6~8周,以促进创面修复。
问题12:SMT术后标本的处理规范。 推荐意见:术后对整块切除的标本进行冲洗和展平等处理,观察、测量并记录新鲜标本的大小、形状、SMT的肉眼所见(大小、形状、颜色、硬度、包膜完整程度等),再将标本浸泡于甲醛进行下一步病理学检查。 (100%的专家赞同)
由于病理学的最终诊断关系到后续治疗方案的选择,是诊断 SMT 性质、鉴别良恶性病变的金标准,故切除肿瘤及获取准确、完整的病理诊断是必要的。规范化的病理报告需包括:(1)标本类型、肿瘤部位、病变肉眼下形态及大小;(2)组织学类型及分级(注明核分裂象数/10HPF);(3)标本包膜是否完整;(4)标本侧切缘及基底切缘的状态;(5)被覆黏膜有无病变[53]。
常规苏木精-伊红染色(HE染色)鉴别困难的病例,需加做免疫组化染色(包括 CD117、CD34、DOG‑1、SMA、Desmin、S‑100、Ki‑67、CgA、Syn等指标)以明确诊断。对于有恶性潜能的SMT,如GIST及NET等病理评估更应准确仔细。
问题13:SMT治疗后的内镜随访策略选择。 推荐意见:(1)良性病变:病理提示为良性病变如脂肪瘤、平滑肌瘤,无需强制规律随访。 (100%的专家赞同) (2)无恶性潜能SMT:如<1 cm且分化良好的直肠NET,一般病程良好,术后常规随访。 (100%的专家赞同) (3)低恶性潜能SMT:如低风险GIST,需在治疗后每6~12个月进行EUS或影像学评估,再按照临床指示进行处理。 (96%的专家赞同) (4)中高恶性潜能SMT:如术后病理证实为3型胃NET,长径>2 cm的结直肠NET及中高风险GIST,应行完整的分期并强烈考虑追加治疗(手术、放化疗、靶向治疗)。方案的制订要基于多学科会诊,以个体为基础。 (100%的专家赞同)
术后病理学诊断是明确SMT性质的金标准,而内镜下完整切除 SMT 是准确充分的病理学评估的基础。病理学最终诊断后,根据不同病理类型和切除的完整性选择不同的处理方式。
术后病理为良性病变,如脂肪瘤、平滑肌瘤等,可无需随访。低风险且<2 cm的直肠NET可选择局部切除,且内镜治疗可达到较高的完整切除率。一项中位随访时间长达61个月的研究表明,内镜治疗<2 cm的NET具有较高的完全切除率,研究结果提示切缘阳性并不影响直肠NET患者的生存;此外,与切缘阳性的患者相比,行挽救性ESD的患者表现出了更高的并发症发生率,对患者来说却无明显的生存获益。同时,以往也有关于>1 cm的直肠NET复发转移的报道。综合考虑,对<1 cm且分化良好的直肠NET,一般病程良好,术后仅需常规随访。对于术后病理提示具有恶性潜能的肿瘤,对其复发风险的评估尤为重要,主要关注局部复发、肝转移以及腹腔播散等。对比增强CT对复发的监测具有优势,在多个GIST临床实践指南中均被推荐为随访检查方法。另外,高危SMT在EUS下可表现出一些特定的高危回声特征,故对于具有恶性潜能的SMT,推荐EUS为随访检查的方法。对于完整切除的低风险GIST,在最初10年每6~12个月的随访间隔中很少观察到复发。如前所述,术后提示为中高恶性潜能的SMT具有极高的复发和转移风险,应通过多学科会诊讨论,根据患者的个体情况精确评估受益和风险,考虑进一步追加手术、放化疗或靶向治疗。诊疗流程见图1。
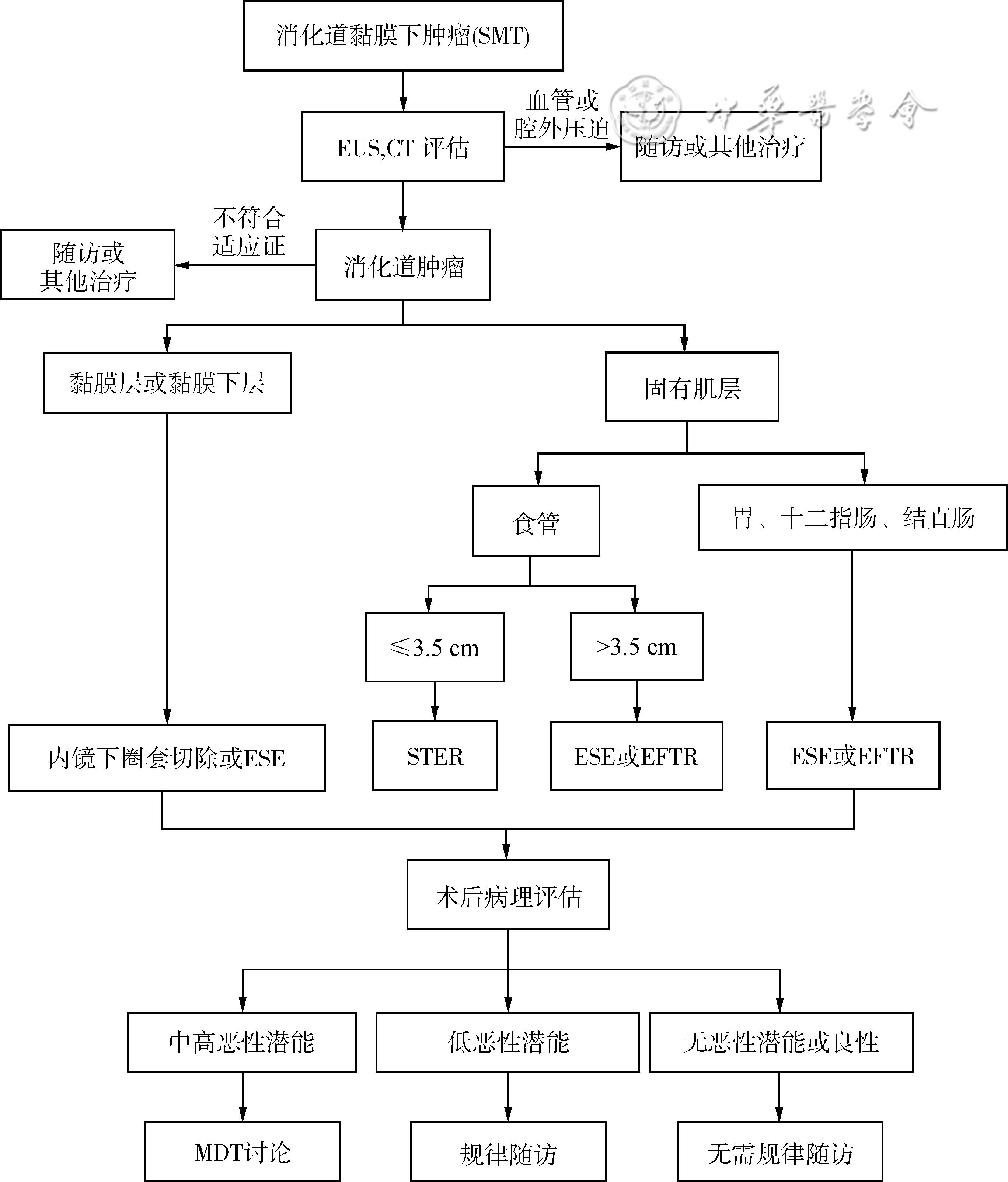
图1 消化道黏膜下肿瘤的诊疗流程
注:EUS指超声内镜;ESE指内镜黏膜下挖除术;STER指经黏膜下隧道内镜肿瘤切除术;EFTR指内镜全层切除术;MDT指多学科会诊
参与制订本共识的专家(按姓氏拼音排序):艾合买江·库尔班江(*疆新**维吾尔自治区人民医院)、柏健鹰(陆军军医大学第二附属医院)、包郁(四川省肿瘤医院)、蔡开琳(华中科技大学同济医学院附属协和医院)、蔡明琰(复旦大学附属中山医院)、曹占国(天津市南开医院)、陈巍峰(复旦大学附属中山医院)、陈卫刚(石河子大学医学院第一附属医院)、陈幼祥(南昌大学第一附属医院)、崔红元(北京医院)、*党**彤(包头医学院第二附属医院)、樊超强(陆军军医大学第二附属医院)、范志宁(江苏省人民医院)、方莹(西安交通大学附属儿童医院)、冯志杰(河北医科大学第二医院)、伏亦伟(南京医科大学附属泰州人民医院)、戈之铮(上海交通大学医学院附属仁济医院)、郭瑾陶(中国医科大学附属盛京医院)、郝建宇(首都医科大学附属北京朝阳医院)、和水祥(西安交通大学第一附属医院)、侯波(山西省人民医院)、胡冰(海军军医大学附属东方肝胆外科医院)、胡兵(四川大学华西医院)、胡皓(复旦大学附属中山医院)、胡*卫健**(复旦大学附属中山医院)、黄留业(青岛大学医学院附属烟台毓璜顶医院)、黄晓伟(华中科技大学同济医学院附属同济医院)、黄永辉(北京大学第三医院)、姜慧卿(河北医科大学第二医院)、金震东(海军军医大学第一附属医院)、李俊(昆明医科大学第二附属医院)、李柯(北京大学第三医院)、李启勇(浙江大学国际医院)、李全林(复旦大学附属中山医院)、李文(天津市人民医院)、李修岭(河南省人民医院)、李汛(兰州大学第一医院)、李延青(山东大学齐鲁医院)、李兆申(海军军医大学附属长海医院)、梁玮(福建省立医院)、林生力(复旦大学附属中山医院)、令狐恩强(解放军总医院)、刘冰熔(郑州大学第一附属医院)、刘德良(中南大学湘雅二医院)、刘海峰(解放军总医院第三医学中心)、刘梅(华中科技大学同济医学院附属同济医院)、刘鹏(湖南省人民医院)、刘小伟(中南大学湘雅医院)、刘晓岗(四川省人民医院)、马丽黎(复旦大学附属中山医院)、马颖才(青海省人民医院)、梅俏(安徽医科大学第一附属医院)、梅浙川(重庆医科大学附属第二医院)、缪林(南京医科大学第二附属医院)、聂占国(*疆新**军区总医院)、彭贵勇(陆军军医大学西南医院)、彭琳(内蒙古自治区人民医院)、覃山羽(广西医科大学第一附属医院)、秦新裕(复旦大学附属中山医院)、任重(复旦大学附属中山医院)、戎龙(北京大学第一医院)、荣光宏(广东医科大学附属东莞第一医院)、沙卫红(广东省人民医院)、尚东(大连医科大学附属第一医院)、盛剑秋(解放军总医院第七医学中心)、施新岗(海军军医大学第一附属医院)、时强(复旦大学附属中山医院)、司丽娟(厦门大学附属中山医院)、孙光斌(天津市第五中心医院)、孙明军(中国医科大学附属第一医院)、孙晓滨(成都市第三人民医院)、孙晓梅(黑龙江省医院)、唐涌进(中华消化内镜杂志编辑部)、唐秀芬(黑龙江省医院)、田利国(中国实用外科杂志编辑部)、王邦茂(天津医科大学总医院)、王波(华中科技大学同济医学院附属同济医院)、王成(中国科技大学附属第一医院)、王晟(中国医科大学附属盛京医院)、王雷(海军军医大学第一附属医院)、王鹏飞(兰州大学第二医院)、王庆(天津市南开医院)、王秋生(北京大学人民医院)、王祥(兰州大学第二医院)、王晓枫(解放军总医院第三医学中心)、王学红(中南大学湘雅二医院)、王雪峰(上海交通大学医学院附属新华医院)、王晓艳(中南大学湘雅三医院)、王燕斌(首都医科大学附属北京朝阳医院)、王拥军(首都医科大学附属北京友谊医院)、*震王**宇(天津市南开医院)、王中华(*藏西**自治区人民医院)、王子恺(解放军总医院第一医学中心)、韦红(海南省人民医院)、吴东方(首都医科大学附属北京朝阳医院)、邢象斌(中山大学附属第一医院)、徐雷鸣(上海交通大学医学院附属新华医院)、徐美东(上海市东方医院)、许国强(浙江大学医学院附属第一医院)、许树长(上海市同济医院)、杨少奇(宁夏医科大学总医院)、易滨(海军军医大学附属东方肝胆外科医院)、于红刚(武汉大学人民医院)、俞力(首都医科大学附属北京友谊医院)、原丽莉(山西医科大学第二医院)、张国梁(天津市第一中心医院)、张继军(山西医科大学第一医院)、张继伟(吉林市人民医院)、张磊(兰州大学第一医院)、张鸣青(厦门大学附属东南医院)、张铭(中国医学科学院肿瘤医院山西医院)、张澍田(首都医科大学附属北京友谊医院)、张筱凤(浙江大学医学院附属杭州市第一人民医院)、张轶群(复旦大学附属中山医院)、张月寒(河北省人民医院)、张震(复旦大学附属中山医院)、张志强(*疆新**医科大学第一附属医院)、赵贵君(内蒙古自治区人民医院)、赵秋(武汉大学中南医院)、赵永捷(天津市人民医院)、智发朝(南方医科大学南方医院)、钟芸诗(复旦大学附属中山医院)、周平红(复旦大学附属中山医院)、周益峰(浙江大学医学院附属杭州市第一人民医院)、朱苏敏(徐州医科大学第二附属医院)、祝喜萍(哈尔滨医科大学附属第一医院)、祝荫(南昌大学第一附属医院)、邹晓平(*京大南**学医学院附属鼓楼医院)
参考文献略,原文见《中华消化内镜杂志》2023年第4期