研究背景
随着全球肥胖率的上升,2型糖尿病(T2DM),非酒精性脂肪性肝炎(NASH)等肥胖并存病的患病率也以惊人的速度不断上升,对药物治疗的需求越来越迫切。然而,为这些慢性疾病确定和开发新的治疗策略需要对其安全性进行考虑,这也阻碍了其向临床的转化。在肥胖症中,过量的脂质堆积会导致胰岛素抵抗,表现为肝脏叉头框蛋白O1(Foxo1)依赖性肝葡萄糖生成(HGP)增加。于是在研究Foxo1对2型糖尿病病理生理的影响时,作者发现肝细胞Notch信号通路的再激活。Notch是一个进化上保守的细胞信号系统,指导胚胎的发育,在标准的生理条件下,静止的肝细胞Notch活性持续到成年,然而,在肥胖小鼠和患者中,作者观察到异常的肝细胞Notch活性与存在T2DM以及NASH的生化和组织学数据密切相关,肝细胞Notch功能丧失小鼠显示出饮食诱导的肝脏病理学减弱,包括喂食高脂饮食(HFD)小鼠的葡萄糖耐受不良改善,以及NASH饮食诱导的小鼠的肝纤维化减轻,增强肝细胞Notch活性则加速了两种模型的饮食效应。
先前的研究表明,Notch*制剂抑**将会有代谢方面的益处,目前研究得最好的Notch拮抗剂是γ-分泌酶复合物(GSI)的小分子*制剂抑**,它可以阻止Notch受体的分裂,目前正在癌症的临床试验中。事实上,GSI治疗降低了肝脏Notch活性,改善了葡萄糖代谢,改善了NASH饮食诱导的肝纤维化,但其肝外副作用,尤其是杯状细胞转化,限制了其治疗效果。于是作者假设肝脏特异性GSI给药可以在保持疗效的同时避免肠道副作用。纳米药物介导的治疗可以增强靶向药物传递,许多纳米颗粒成分(如PLGA)具有良好的生物降解性和相容性,为了测试这种潜力,作者开发了PLGA包裹的GSI纳米粒(GSI NPs)(如下图)。通过一系列的实验证明了GSI NPs对肝脏Notch信号有局部有效的抑制作用,可以改善肥胖诱导的糖耐量受损和肝纤维化,且无明显的肠道副作用。
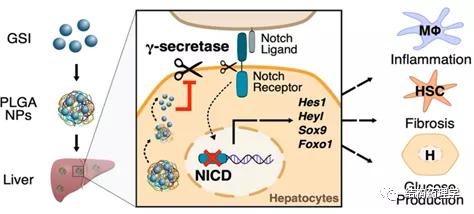
研究内容
1. GSI NPs的合成与表征
作者采用溶剂/溶剂蒸发法制备GSI NPs,以PLGA为基质,用二氯甲烷(DCM)和3%聚乙烯醇(PVA)溶液溶解γ-分泌酶*制剂抑**DBZ和PLGA,将PLGA混合物超声处理后分散于0.3%PVA溶液中,蒸发DCM。离心法收集合成的NPs,使用Cy5.5荧光团标记,根据动态光散射测定发现,合成的球形NPs直径约为180nm,且在7天内其大小保持相对不变(图a-c)。为了监测GSI的解离行为和释放动力学,作者使用负载纳米粒的GSI在含有20%乙醇的磷酸盐缓冲溶液(PBS)(pH 7.4)中孵育,NPs由于PLGA的生物降解而逐渐解离,从而触发包裹物的释放。根据缓冲液中GSI的浓度测量,这种解离和释放持续了8天以上(图d)。在体内,静脉注射(IV)尾静脉后1小时和24小时,发现纳米颗粒主要分布在肝脏和肾脏,反映了其积聚在肝脏和肾脏中排泄(图e)。
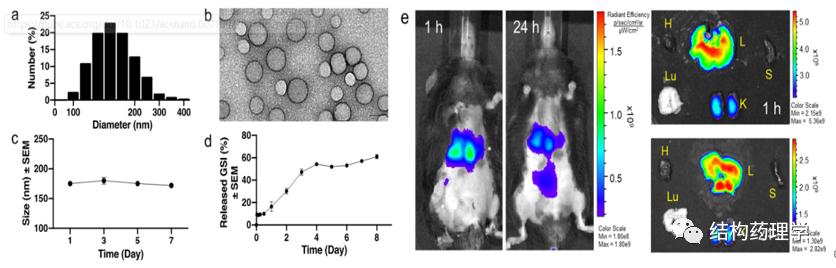
2. GSI-NPs阻断肝脏Notch活性
为了评估Notch*制剂抑**在体内的作用效果,作者通过尾静脉方式给C57BJ/6雄性小鼠单剂量5µmol/kg悬浮在生理盐水中的GSI NPs,结果发现,GSI NPs可以在肝脏中直接观察到,而胃肠道中没有发现(图a-d)。接下来,作者分析了一些经经验选择的Notch靶基因的肝脏表达,并在治疗后的多个时间点体内外跟踪肝细胞Notch活性,发现在第二天和第四天肝Notch靶基因表达降低(图e)。
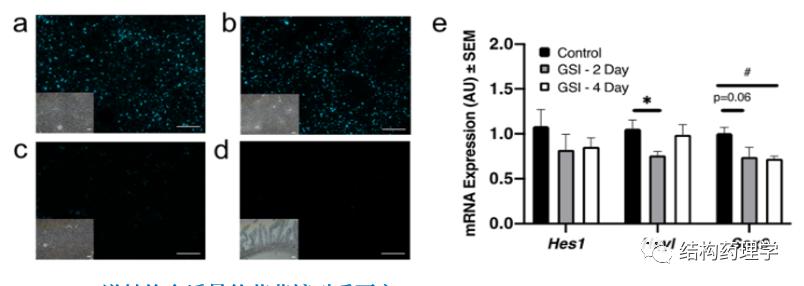
3. GSI NPs逆转饮食诱导的葡萄糖耐受不良
接下来,作者将GSI NPs应用于饮食诱导的肥胖和葡萄糖耐受不良/胰岛素抵抗的小鼠模型。作者将8周龄的C57BL/6雄性小鼠喂食HFD共18周(图a),饲喂14周后,将小鼠随机分为两组,GSI NPs组和对照组均通过尾静脉注射的方式每周两次,为期四周。结果发现,GSINP处理的小鼠在葡萄糖负荷为2g/kg时,与对照组相比,葡萄糖耐量显著改善(图b,c),同时作者观察到GSI NP治疗小鼠的空腹血糖水平有所降低(图d),尽管通过磁共振成像(MRI)测量的体脂相同,肝脏,腹股沟白色脂肪组织(iWAT)和附睾白色脂肪组织(eWAT)的重量也相似(图e-g),同时也未观察到肝脏脂质含量或转氨酶的显著差异(图h)。以上数据表明,GSI NP治疗改善了葡萄糖耐量,但不是由于体重,肥胖或肝脂质含量/损伤的改变引起的。
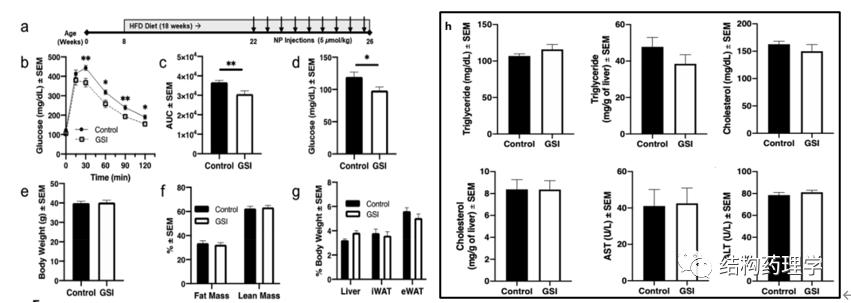
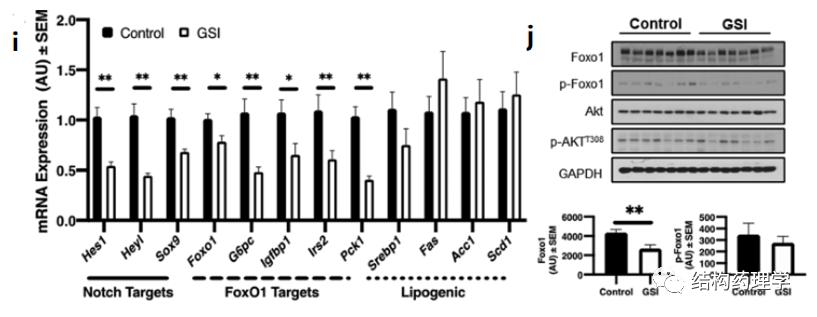
接着,作者评估了GSI NP治疗小鼠改善葡萄糖耐量的潜在分子途径,如预期的那样,GSINPs将Notch靶基因的表达下调了约34%-58%,同时作者还观察到Foxo1表达显著降低,导致包括与肝葡萄糖生成相关的多个Foxo1靶基因的下降(图i)。WB结果同样显示GSI NP处理的小鼠肝Foxo1显著减少38%,且磷酸化的Foxo1成比例减少,但磷酸化的Akt不变(图j)。综上所述,这些数据表明GSI NP诱导的肥胖糖耐量改善是由于Foxo1介导的HGP的减少。
4. GSI NPs治疗不会引起胃肠道或脾*毒脏**性
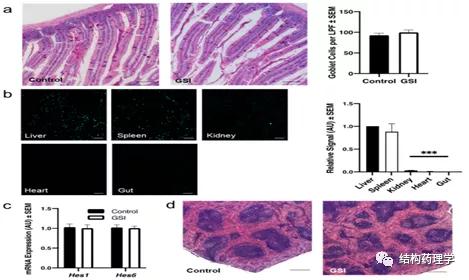
接下来,作者研究了目前已知的GSI副作用:肠化生和脾脏边缘区萎缩。作者在对照组和GSINP治疗组小鼠的小肠中都观察到了最小的Cy5.5信号且GSI NP治疗组的杯状细胞数目无明显变化(图a),这与同样剂量的未包被GSI的小鼠形成鲜明对比,GSI显示杯状细胞增加了3倍,导致粘液性腹泻、脱水、体重减轻,最终死亡。根据NP的大小,作者在脾脏中观察到了Cy5.5信号,但并没有在其他肝外组织中观察到NP外壳(图b)。同时,作者通过对脾脏中最丰富的Hes/Hey基因的表达进行评估,观察到脾脏Notch活性并没有改变(图c),也未发现脾脏结构上的差异(图d)。作者这里认为,脾脏中的Cy5.5信号可能是循环中的单核细胞清除的NP外壳或是随着时间推移少量的NPs被累积包埋,因为在注射后的最初24小时,脾脏并没有显示出明显的信号。
综上,虽然GSI NPs可以通过全身循环到达其他器官,但大多数药物作用依然是在肝脏中按预期发生的。
5. GSI-NPs逆转NASH诱导的肝纤维化而无胃肠毒性
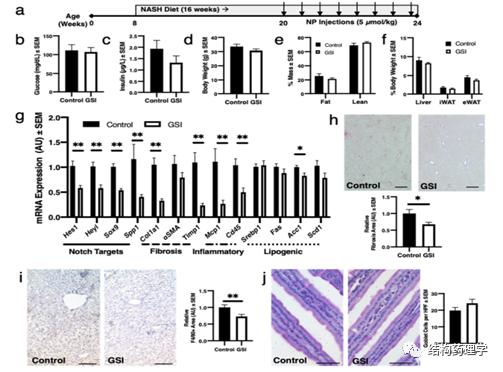
作者观察到NASH患者或者NASH饮食激发的小鼠肝细胞Notch活性异常,全身GSI治疗可减少这些小鼠的肝纤维化,但具有显著的肠胃道毒性。为了测试GSI纳米粒改善NASH诱导的肝纤维化的安全性和有效性,作者每周两次使用GSINPs或对照连续四周尾静脉注射C57BL/6雄性小鼠(图a)。作者观察到各组之间的体重,组织重量等并没有明显差异(图b-f),同时,GSI NPs降低了Notch靶基因的表达,也显著降低了炎症和纤维化基因的表达(图g)。另外,作者观察到肝胶原染色减少了32%,肝巨噬细胞数量减少了27%(图h,i),这两种情况均有助于改善肝炎症和纤维化,最重要的,与对照组相比肠道杯状细胞数量并没有增加(图j)。
总的来说,这些数据表明,GSI NPs可以改善NASH饮食诱导的肝纤维化和炎症,且无传统GSI治疗的肠道毒性。
总结与思考
在这篇文章中,作者描述了一种基于肝脏PLGA NP摄取的药物传递技术,它可以阻断病理性肝细胞Notch信号,同时相较于传统的GSI给药,显著降低了肠道和脾脏的毒性问题,是本文的一大亮点。GSINPs治疗显著降低了饮食诱导的小鼠模型葡萄糖耐受不良以及肝纤维化,且GSI能够有效传递到预期靶点,同时减少或避免了对其他组织的毒性。文章中作者巧妙地将纳米医学利用到以前无法耐受的药物上且达到了预期想要的结果,为今后的研究奠定了基础。
作者为了解决Notch*制剂抑**GSI在拥有较好的抑制效果的同时却伴随着严重的副作用,开发了一种纳米粒子介导的靶向传递系统。并通过一系列实验证明了,在保持传统GSI治疗效果的同时,GSI NPs治疗能够显著降低胃肠道和脾*毒脏**性,达到了预期想要的效果,提示我们以前具有临床毒性的药物是否可以通过结合其他技术减轻这些副作用以更好地重新利用。另外这篇文章中,作者需要对药物的持续效应和NASH纤维化的潜在可逆性进行观测,以更好地解决肥胖在临床环境中面临的问题。
本文于2020年5月22日在线发表于期刊 ACS Nano
第一作者是Lauren R. Richter,万千芬,通讯作者为古震,Utpal B. Pajvani,美国哥伦比亚大学和加利福尼亚大学为共同通讯单位。
原文链接:https://dx.doi.org/10.1021/acsnano.0c01007
#头条知士#