
马依彤
*疆新**医科大学第一附属医院
出血是冠心病(coronary heart disease,CAD)患者经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)术后严重并发症之一,其对临床预后不良的影响不亚于缺血并发症或更甚,合理抗凝可减少或预防PCI过程中的出血事件。在急性冠脉综合症(acute coronary syndrome, ACS)患者行PCI过程中如出现出血,死亡率将明显升高。减少出血风险的一些策略虽已明确,包括使用药物进行干预(如鱼精蛋白),但针对CAD患者群体PCI的抗凝治疗进展迅猛,许多实际问题都与抗凝药物的选择及其剂量相关,同时药物之间的相互组合对出血也有一定的影响。通过回顾近期的临床试验研究,主要包括目前临床常用和指南推荐的药物,以期阐明PCI术后出血与抗凝药物的选择和剂量的关系。
一、PCI中出血的定义
抗凝药在治疗PCI过程中引起的出血率为1~10%,但使用双重抗血小板治疗(dual antiplatelet therapy,DAPT)联合抗凝药治疗时,出血率可高达20%。出血率的差异主要由出血的定义、患者个体差异、辅助治疗和不良事件报告的时机来决定。出血定义在不同研究中存在显著差异,为此出血学术研究协会(Bleeding Academic Research Consortium, BARC)对血管介入过程中的出血和终点事件报告进行了统一的界定,以便更严格地质控出血从而更好地规范血管介入治疗。根据BARC出血的定义,将出血分为5型:0型,无出血证据;1型,不需要处理的出血,如擦伤、血肿、鼻出血、痔出血;2型,任何具有临床意义需要处理的出血征象,但不符合3型、4型(CABG相关)或5型(致命性出血)的标准,该型出血需要住院治疗;3型:临床、检验或影像证据提示的出血,需要住院治疗,根据出血严重程度及出血部位细分为3a型(需要输血的明显出血,明显出血伴血红蛋白减少≥3但<5 g/dL=、3b型(明显出血伴血红蛋白减少≥5 g/dL,心脏压塞,需要外科干预和静脉给予血管活*药性**物的出血)和3c型(颅内出血和影响视力的眼出血);4型:冠状动脉旁路移植(Coronary Artery Bypass Graft,CABG)相关出血,包括围手术期48小时内的脑出血,关胸后重新手术以控制出血,术后48小时内外源性输注全血或浓缩红细胞≥5U,胸腔引流量24小时内≥2L;5型,致命性出血,出血直接导致死亡,其细分为5a型(可能致命性出血,临床上可疑的致死性出血,但未直接观察到,同时无尸检或确定的影像证明)和5b型(确定的致命性出血,通过临床标本如血、呕吐、大便直接观察到或影像证实,或通过尸检证明),致命性出血部位可明确为颅内、胃肠道、腹膜后、肺部、心包、泌尿生殖系统等,而且致命性出血与死亡直接相关,而与其他原因无关。
二、抗凝出血的相关因素
出血相关的一些危险因素在PCI抗凝治疗选择和给药剂量时应充分考虑,包括:高龄、女性、肾功能不全、低体重(low body weight,LBW)、既往出血病史、低平均动脉压、进行有创操作,以及使用如糖蛋白IIb / IIIa*制剂抑**(GPI)和纤溶剂抗栓治疗。在CRUSADE研究中风险分数用以评估患者入院时的出血风险,包括:红细胞压积、肌酐清除率(ClCr)、心率、性别、心力衰竭体征、既往血管疾病、糖尿病和收缩压。CRUSADE出血风险评分可以用于评估使用药物前的基线风险和指导出血时的治疗强度,其整合了6个基线因素(女性、高龄、血清肌酐水平升高、白细胞计数升高、贫血和ACS的表现),以及一个治疗相关变量(使用肝素加GPI或单用比伐卢定)。
三、出血对预后的影响
关于出血尚无统一定义,但无论出血定义为何,出血与非致死性心肌梗死、支架内血栓和中风发生率及死亡率增加均明显相关。CathPCI注册研究显示PCI术后严重出血并发症导致的死亡占所有住院死亡患者的12.1% 。住院患者每发生16~117例出血,可发生1例死亡,主要取决于出血的风险与出血部位。相关研究数据表明出血患者在30天和1年时的死亡相对风险度(relative risk,RR)增加2至10倍,而PCI术后出血与PCI术后心肌梗死的1年死亡率相同。急性心肌梗死(acute myocardial infarction,AMI)患者置入药物洗脱支架(drug eluting stent,DES)后,约三分之一患者出现出血,而出血也将影响患者对DAPT药物的依从性。除由于停药导致支架内血栓和再梗死风险增加,出血本身可能也预示着预后更差,其机制包括由于低血压、休克和/或贫血导致的缺血,以及输血相关的促炎症和促血栓形成反应。出血不仅影响临床疗效,也会增加医疗成本(输血和住院时间延长)。
四、规避出血策略
评估患者的基线出血风险可协助预测预后和合理制定“个体化”治疗方案。相关出血规避策略(bleeding avoidance strategies,BAS)已经在PCI的结果中得到证实,包括药物使用(如:比伐芦定、短效的GPI),临床操作(如:提前拔除鞘管,桡动脉入路),相应器械的使用(血管封堵器)。注册数据表明PCI相关的出血事件在主要血管并发症中呈总体下降趋势,这主要得益于药物治疗的改善,如2005至2009年比伐芦定的使用提高了约20%。目前已证实PCI术前风险评估可预测PCI术后出血,同时使用BAS可显著降低的出血相关风险。可以预见在PCI实践中BAS使用的越广泛,出血的可能性越小。
尽管目前BAS得到认可,但PCI相关的抗栓策略仍在快速更新。许多实际问题与合理选择抗凝剂及合适的给药剂量密切相关。根据美国心脏病学会/美国心脏协会/美国心血管造影和介入学会(ACC/ AHA/ SCAI)指南及欧洲心脏病协会和欧洲经皮心血管介入学会(ESC/EAPCI)指南更新,可以体现抗凝药物在PCI中应用的进展。表1总结了目前临床常用抗凝药物,包括普通肝素、低分子肝素、直接凝血酶*制剂抑**和Xa因子*制剂抑**的主要特性。表2总结了在PCI治疗过程中可减少出血风险的抗凝药物治疗策略。

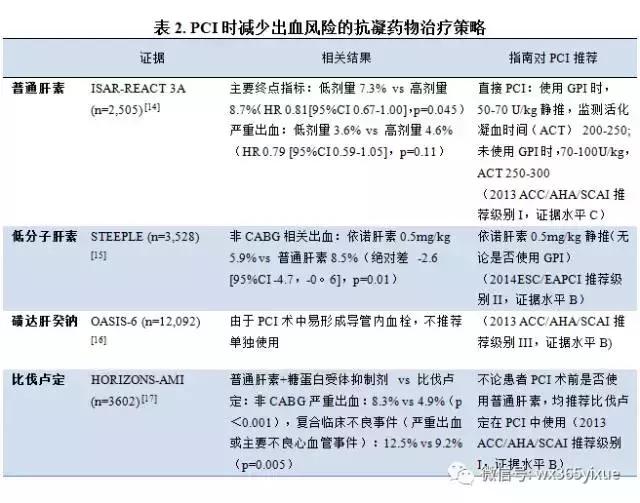
五、主要的抗凝药物剂量与出血的关系
普通肝素
普通肝素自1916年发现以来,在STEMI的治疗中作为主要抗凝剂使用。肝素的抗凝效果不仅具有剂量依赖性,同时其药效与给药方式也有关,静脉给药药效强于皮下给药。此外,由于抗凝效果存在个体差异,使用肝素需要监测活化凝血时间(ACT)。上世纪90年年代,国际梗死生存研究-ISIS-2临床试验表明普通肝素与阿司匹林联用在接受链激酶基础治疗的患者中,较单独使用肝素或阿司匹林在降低30天死亡率方面更有效。随后的ISIS-3和GISSI-2试验显示,联合使用溶栓、肝素和阿司匹林较溶栓联合阿司匹林在降低院内和30天死亡及再梗死更有效。之后的GUSTO试验证实,在服用阿司匹林的患者中,联合使用组织纤溶酶原激活物和普通肝素与其他治疗方案相比可改善冠脉通畅情况和30天生存。但是与缺血获益相对应,这些研究也强调了肝素剂量相关的出血风险。表2中列了目前在直接PCI中根据体重给药的治疗剂量。除外出血,肝素由于其生物学和药代动力学机制导致的低治疗指数缺陷也妨碍了其使用。而非特异蛋白结合导致其生物利用度低、肝素抵抗、骨量减少和肝素诱导的血小板减少。
低分子肝素
低分子肝素(LMWH)由普通肝素解聚而来,其分子量相对小,生物利用度高,血浆内半衰期长,较普通肝素具有更稳定的抗凝作用。低分子肝素在纤维蛋白溶解试验中得到广泛研究,ENTIRE-TIMI 23替奈普酶试验结果表明使用依诺肝素较普通肝素有较低的死亡率或再梗死率(4.4% vs 15.9%, p=0.005),严重出血率相似(1.9% vs 2.4%)。但在PCI的相关研究中,关于低分子肝素的研究较少,以至于ACC/AHA在2013年STEMI指南中仅在溶栓治疗中推荐为I A类适应证,但在直接PCI中却未提及。但在2014年ESC/EAPCI关于PCI的治疗中推荐依诺肝素作为IIa B类适应证使用。这主要得益于ATOLL试验,这是唯一一个比较低分子肝素和普通肝素在直接PCI中应用的随机试验。该试验共纳入910位患者,其中80%患者接受了GPI治疗,三分之二患者经桡动脉入路手术。术中根据体重给予0.5mg/kg的依诺肝素静推,对照组则给按照体重给予70-100U/kg的低分子肝素。其主要净临床获益终点为复合指标(包括:死亡、心肌梗死并发症、手术失败或严重出血),两组间无差异,但次要终点指标(ACS复发或紧急血运重建)在依诺肝素组显著降低(7% vs 11%, p=0.01)。根据STEEPLE定义的出血标准,两组间出血无差异。但是根据试验的方案的定义,依诺肝素在主要终点事件(RR 0.76, p=0.01),次要终点事件(RR 0.37, p<0.0001),以及严重出血(RR 0.46, p=0.05)方面均优于普通肝素。
磺达肝葵钠
磺达肝葵钠是一种合成的肝素戊多糖,仅对Xa因子具有抗凝血酶依赖活性。在OASIS 6 ACS试验中对比了磺达肝葵钠使用7天与普通肝素使用48小时的疗效,磺达肝葵钠在减少缺血事件中疗效较普通肝素好(30天死亡或再梗死率9.7% vs 11.2%,p=0.008),同时在不增加出血(1.0% vs 1.3%,p=0.13)。但在行PCI的患者中使用磺达肝葵钠不仅无明显获益,反而增加了导管内血栓形成风险(22 vs 0,p<0.001)。据此指南仅推荐磺达肝葵钠作为普通肝素或低分子肝素的替代治疗,而在PCI中作为III B类证据级别不推荐使用。
直接凝血酶*制剂抑**:比伐芦定
直接凝血酶*制剂抑**比伐芦定主要作用于纤维蛋白结合及凝血酶,对Xa因子不起作用,同时不需要结合抗凝血酶来发挥抗凝作用。比伐芦定已成为避免PCI术患者出血的关键药物。多个随机对照临床试验都已证明,比伐芦定可显著减少ACS患者的出血而又不影响缺血结果(死亡、心肌梗死和心肌血运重建),单用比伐芦定对比肝素(依诺肝素或普通肝素)加GPI,可相对减少40-50%非CABG相关严重出血的风险;但常规使用GPI则会抵消减少出血的作用。
六、结语
接受PCI术患者的抗凝治疗方案随着新型抗凝药物的出现更迭迅速。随着PCI术前强效P2Y12*制剂抑**(如:普拉格雷和替格瑞洛)和新型口服抗凝药物(NOACs)在冠心病患者中的广泛应用,丰富接受PCI术患者的抗血小板及抗凝药物治疗,但同时也增加其潜在的出血并发症。出血患者伴发较并发症和死亡率均升高。但随着相关大型随机对照试验的开展,循证医学证据不断丰富,为行PCI患者进一步更安全有效的抗凝策略的制定和个体化治疗提供了指导。因此,根据指南及近期大型临床试验的结果,结合患者具体病情,选择恰当的抗凝药物和剂量至关重要,同时可以采用BAS辅助治疗,在临床实践中进一步降低出血事件的概率。患者诸多个体因素及药物特性与潜在的出血风险相关,如年龄、肾功能、体重和遗传因素,因此须充分考虑个体因素。临床医师在选择合适的药物、控制给药剂量和监测药效及减少或避免出血事件中的作用至关重要。未来的研究重点将尽可能通过使用统一的出血定义,结合患者的基因型和/或表型特征为抗凝药物制定个体化方案,从而探索抗凝药物的最佳方案。