编译:肿瘤资讯编辑部
来源:肿瘤资讯
2018年7月5-8日,中国临床肿瘤学会(CSCO)联合美国临床肿瘤学会(ASCO)在合肥成功举办了“临床肿瘤学新进展学术研讨会——Best of ASCO(BOA)2018 China”。2天的时间,解读了39项研究摘要,12场专家点评,4个研究进展述评。来自全国各地2000余名专家学者,汇聚合肥,回顾研究进展,共同探讨和交流这些研究对我国临床实践的影响。值得一提的是,本次BOA会议全程网络直播,线上将近1万名学者观看会议的精彩内容。为快速方便地分享国际最前沿研究信息,【肿瘤资讯】带来系列深度报道,以下分享乳腺癌专场精彩内容。
乳腺癌专场1
本专场由安徽省立医院潘跃银教授和福建省肿瘤医院刘健教授担任主持。广东省人民医院廖宁教授解读三项研究进展,南京医科大学附属第一医院殷咏梅教授进行专家述评。
GeparNuevo试验:随机II新辅助研究评估在蒽环紫杉醇类方案的基础上联合Durvalumab用于TNBC
背景:免疫检查点*制剂抑**联合化疗用于转移性三阴性乳腺癌(TNBC)患者,取得了较高的缓解率。因此,本研究旨在原发性TNBC患者中,标准新辅助化疗的基础上联合抗PD-L1单抗durvalumab的疗效。GeparNuevo研究随机将患者分配接受durvalumab (D) 1.5 g 或安慰剂治疗,q4w,患者先在前两周接受D或安慰剂单药治疗(窗口期),然后进行活检,再接受D或安慰剂联合白蛋白紫杉醇125 mg/m²,qw,连用12周,序贯D或安慰剂联合表阿霉素/环磷酰胺(EC),q2w) q2,连用4个周期。分层因素包括间质肿瘤浸润淋巴细胞(sTILs) 的多少[低(≤10%)、中等(11-59%)、高(≥60%)]。研究入组了原发肿瘤病灶为cT1b-cT4a-d,中心实验室确认的TNBC,以及sTILs状态已知的患者。主要研究终点为比较两组的pCR率 (ypT0 ypN0) 。次要研究终点包括各亚组患者的pCR率以及其他定义的pCRv 了,客观缓解率,保乳率,毒性,耐受性和总生存。根据GeparSepto 研究的结果,假定安慰剂组的pCR率为48%,D组的pCR率为66%(临床有意义的获益),需要纳入158例患者 (双侧 α=0.2, 80%的检验效能)。假设临床试验脱落率为10%,计划随机174例患者。
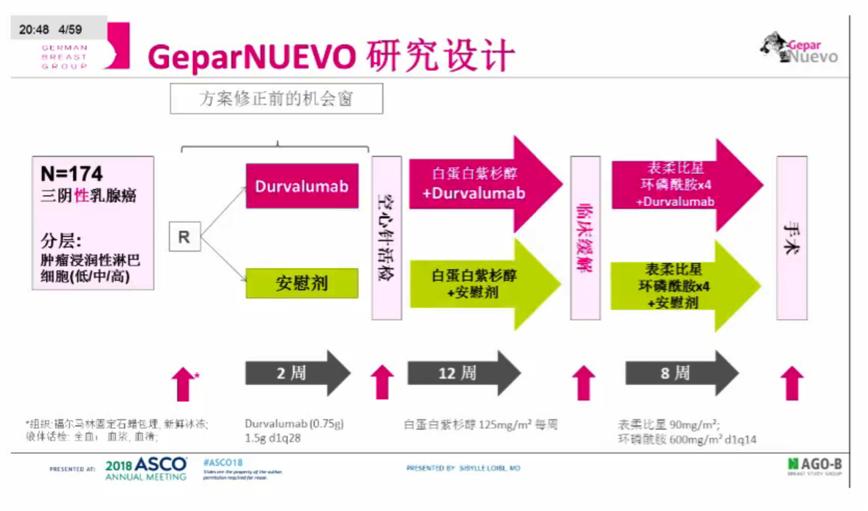
2016年6月至2017年9月,研究共入组了174例患者,所有入组患者均完成了治疗。入组患者的中位年龄为49.5岁(范围23 -76)。cT1,cT2,cT3和cT4的患者比例分别为44.5%,49.7%,3.5%和2.3% cT4。83.3%的患者病理分级为3级,31.4% 临床淋巴结阳性的患者采用了超声波评估。sTILs分类:低、中等和高的患者比例分别为37.9%、47.7%和14.4%。Ki67的中位值为49.0%(范围:3.0%-96.0%)。研究显示,Durvalumab组和安慰剂组的pCR率分别为53.4%和44.2%。亚组分析显示机会窗组治疗的患者(n=117),接受Durvalumab治疗的pCR率显著高于未接受机会窗治疗的患者,此外IIA期以及更高分期和小于40岁的患者,pCR率更高。
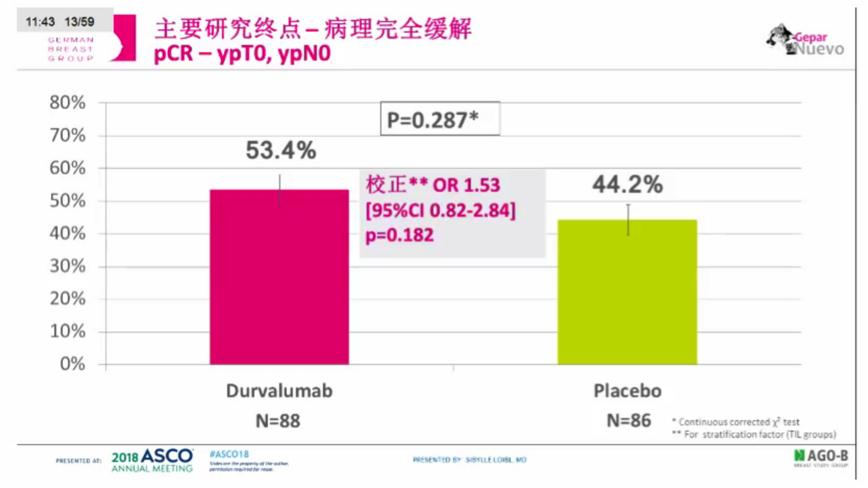
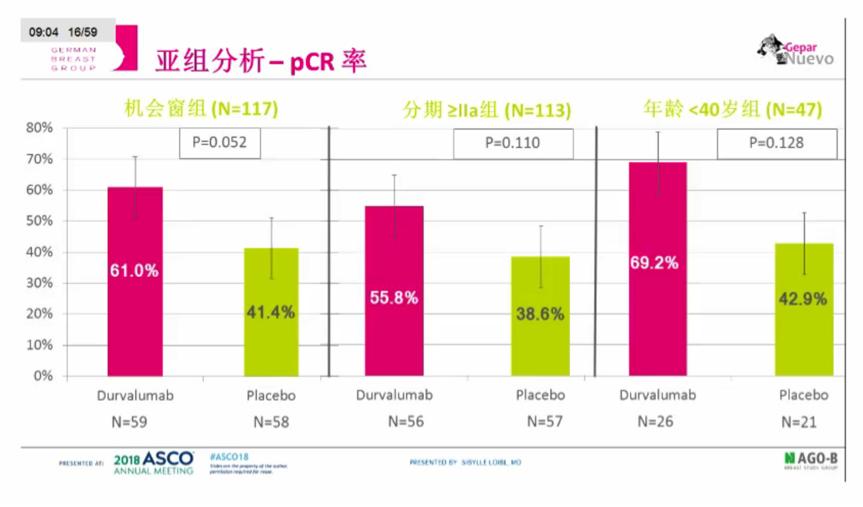
共报道了86个严重不良事件(SAE)和65个irAE。34.5% 的患者至少经历过1个SAE,27.6%的患者至少经历过1个irAE。总体而言,174例患者中,84例子患者取得了pCR (48.3%,95%CI [40.7-56.0]) 。
小结:在原发性TNBC患者中,乳腺癌新辅助治疗中增加durvalumab可以在数值上提高pCR率(53% vs 44%),但是pCR率在以下预设的亚组中显著较高:在化疗前起始运用durvalumab治疗的患者,IIa期以及更高分期的患者和小于40岁的患者,增加Durvalumab治疗耐受性较好。Durvalumab应该进一步在TNBC患者中进行相关研究,加入Durvalumab的新辅助治疗可能会带来获益,进一步的探索和转化性研究正在进行。
殷咏梅教授述评
TNBC乳腺癌是一类异质性较大的肿瘤,其中IM亚型的患者与免疫应答通路相关基因,如CTLA4、IL2、APC等有关。GeparNuevo试验和其他一些免疫治疗的研究给了我们一些初步的结果,但是对于年已治疗如何精准筛选能够获益的患者仍需要进一步的探索,可能的预测标志物包括:TIL浸润?GeparNuevo研究未提示预后作用;PD-L1表达?有待进一步研究。此外,仍需要关注并妥善处理免疫治疗的不良反应。
PERSEPHONE:6个月对比12个月曲妥珠单抗辅助治疗HER2阳性早期乳腺癌:随机III期非劣效临床研究及4年DFS结果
背景:曲妥珠单抗在HER2阳性早期乳腺癌中进行了很多研究,如2005年HERA研究,NSABP-B31临床研究和N9831临床研究,以及后来的BCIRG 006临床研究。系统性荟萃分析显示,曲妥珠单抗辅助治疗能够降低40%的肿瘤复发和34%的死亡风险。基于经验,曲妥珠单抗的关键性注册试验时长为12个月。2006年的FinHer研究结果显示,曲妥珠单抗辅助治疗9周相比于不用曲妥珠单抗能够降低58%的肿瘤相关复发。HERA临床研究显示延长曲妥珠单抗治疗至2年并未带来更多获益。PERSEPHONE研究假设曲妥珠单抗辅助治疗6个月与12个月相比疗效相当,但毒性更小,医疗费用更低。旨在比较6个月和12个月曲妥珠单抗辅助治疗乳腺癌的非劣效性研究,是目前为止国际上最大型的缩短疗程的非劣效性试验。主要入组标准为:HER2阳性早期浸润性乳腺癌(IHC3+或2+且FISH阳性),无远处转移,激素受体状态已知,术后辅助化疗指征明确。假定曲妥珠单抗辅助治疗12个月的4年DFS率为80%,非劣效性检验不低于3%,dance检验显著性水平为5%,检验效能85%,样本量需要4000例受试者。首要终点为诊断以来的DFS(首次复发或全因死亡)。
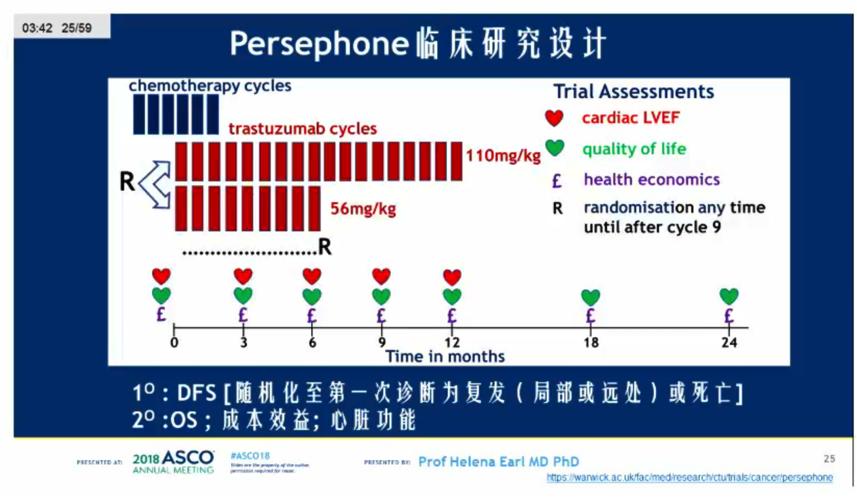
来自于英国152个地区的4089例患者随机分组(2007年10月~2015年7月),1例患者重复随机,分析集共4088例患者。总体人群中,ER+的患者69%;基于蒽环类药物(A)化疗的患者占41%,基于A+紫杉烷(T)的患者49%,基于T方案的患者10%。2018年4月数据更新并重新进行分析,中位随访时间5.4年时,335例(8%)患者死亡,512例(13%)患者复发或死亡。两组的DFS对比, 4年DFS分别为89.8% vs 89.4%, HR为1.07(95% CI,0.93~1.24;P=0.01),证实6个月曲妥珠单抗的非劣效性。预设的亚组分析显示,ER-,接受紫衫类+/-蒽环类,接受新辅助化疗,化疗与曲妥珠单抗同步治疗的患者接受12个月的曲妥珠单抗辅助治疗可能更优。总生存率结果一致,两组的4年OS率分别94.8% vs 93.8%,HR为1.14(90%CI:0.95-1.37,P=0.0006)。毒性分析显示,20%的患者在接受曲妥珠单抗治疗中出现3-4级毒性(6个月组和12个月组的发生率分别为23%和18%,P =0.001)。
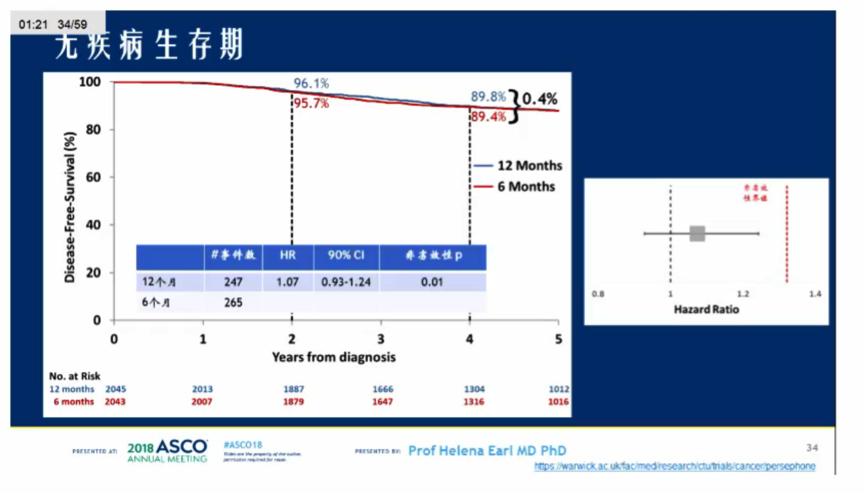
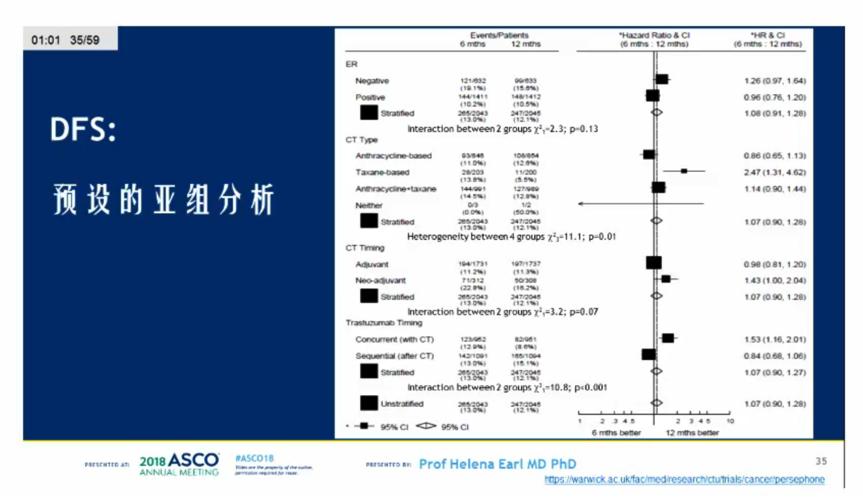
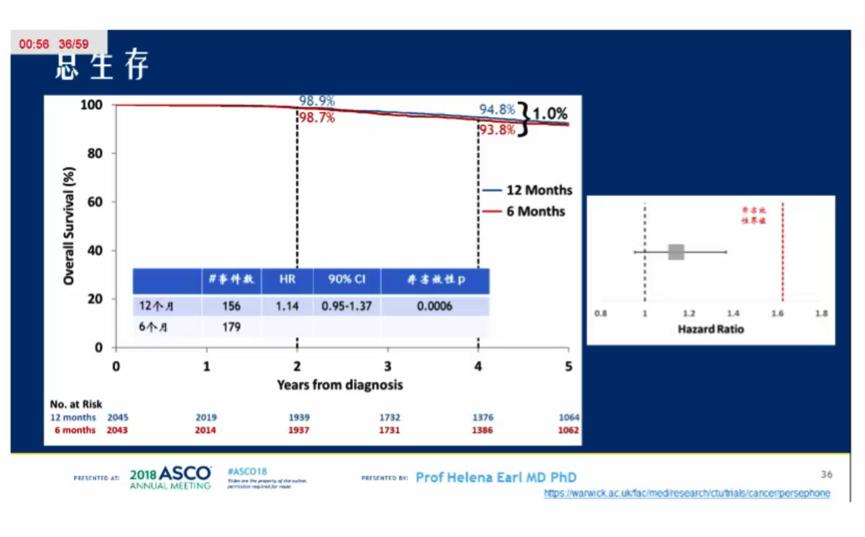
小结:PERSEPHONE临床研究显示6个月曲妥珠单抗辅助治疗并不劣于12个月,与12个月曲妥珠单抗治疗相比,6个月曲妥珠单抗治疗的心*毒脏**性和其他毒性更小,医疗费用更低,该研究结果标志着HER2阳性乳腺癌患者向治疗时间缩短迈进了一步。
专家述评
殷教授回顾了既往在HER2阳性乳腺癌进行降级治疗(缩短疗程)的研究,PHARE和HORG也对比了曲妥珠单抗辅助治疗6个月 vs 1年,但这两个研究均未达到非劣效性终点。这可能与PHARE和Persephone研究非劣效界值的选择有关,PHARE研究专注于风险比和可接受的DFS时间上升的相对风险;而Persephone研究专注于可接受的4年DFS绝对差异,设置的绝对值差异最大为3%,这样HR非劣效界值的估算就得考虑实际观察到的DFS%。进一步回顾这3项研究的心*毒脏**性,所有的研究都显示短疗程治疗带来更少的心*毒脏**性。
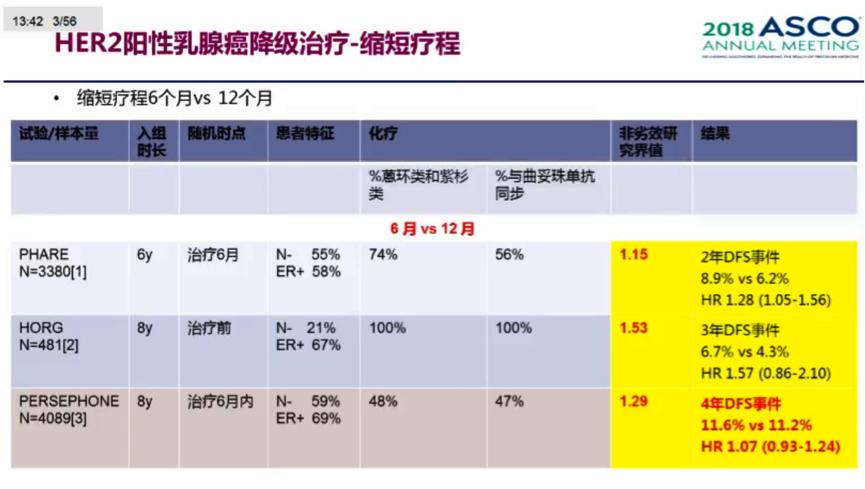
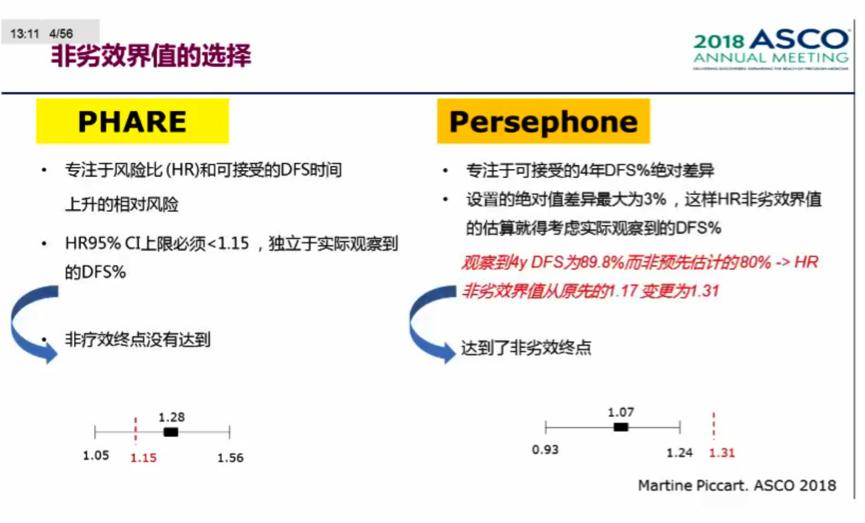
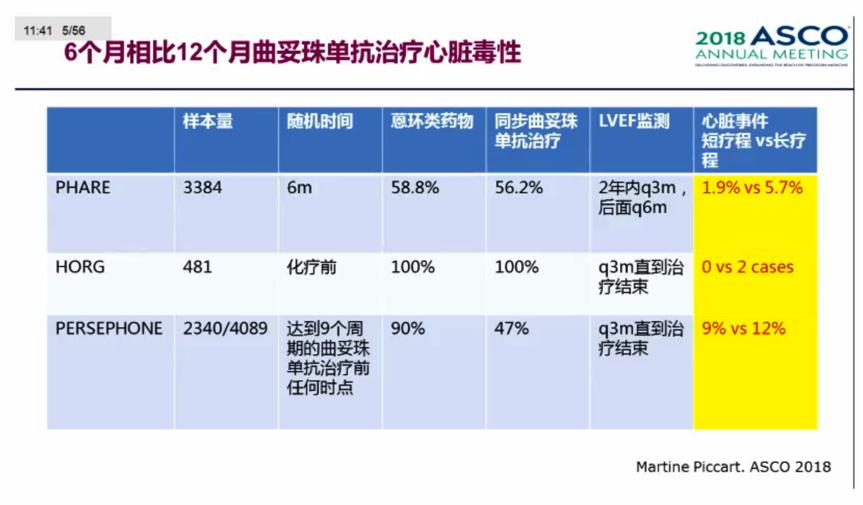
今天来进一步回顾Persephone研究,有一些优势,但也存在不足,总结如下。亚组分析但结果显示这些患者12个月的曲妥珠单抗辅助治疗可能更优:ER-,接受紫衫类+/-蒽环类,接受新辅助化疗,化疗与曲妥珠单抗同步治疗。

关于Persephone研究研究是否可能改变临床实践,我们需要从以下两个方面思考:第一,今天我们更关注于HER2+患者的化疗降级而非抗HER2降级;第二,对于HER2+早期乳腺癌,我们仍需要探索进一步提高治疗疗效。因此,关于HER2阳性乳腺癌辅助治疗有如下总结:HER2阳性早期乳腺癌患者的治疗目标是为每位患者提供治愈机会;曲妥珠单抗1年方案是国内外指南推荐的HER2阳性乳腺癌的标准治疗且安全性得到广泛证实。多项研究均未能证实曲妥珠单抗短疗程的疗效,Persephone研究和既往研究结果不一致,如ASCO大会专家讨论,目前不能改变临床实践。关于HER2阳性低危人群的辅助治疗更关注于如何减少化疗的应用。
TAILORx研究:化疗+内分泌治疗对比内分泌治疗在HR+/HER2-,淋巴结阴性以及21基因复发评分中危乳腺癌患者中的III期临床研究
背景:在HR+/HER2-,腋窝淋巴结阴性的乳腺癌患者中,21基因检测可以预测远处复发风险,对于低危风险(RS评分0-10分)的患者,接受单纯内分泌治疗的复发风险很低;对于高危风险(RS评分>=26分)的患者,可以从化疗中获益;但对于评分中等(11-25分)的患者,是否需要接受辅助化疗,尚未明确。这一前瞻性随机研究,在RS评分中等(11-25分)的患者中对比单纯内分泌治疗和内分泌联合化疗。
研究入组了年龄18-75岁,HR+/HER2-,腋窝淋巴结阴性的乳腺癌,肿瘤大小为1.1-5.0cm(或0.6-1.0cm但病理分级为中等或高级别的患者),且同意分配接受化疗或根据RS评分随机分配的患者。RS评分中等(11-25分)的患者随机分配至单纯内分泌治疗或化疗联合内分泌治疗。主要研究终点为无侵袭性疾病生存率(iDFS),本研究是一个非劣效性研究,即单纯内分泌治疗不差于化疗联合内分泌治疗,但也不拒绝等效性(HR边界:免于化疗组最高HR为1.322,单侧I类错误发生率为10%,II类错误发生率为5%)。研究在计算样本量时考虑到患者可能不遵循随机分配,方案特定的最后分析时间为出现835个iDFS事件。

2006年7月4日至2010年6月10日,研究共入组了10253例合格的患者,RS评分为11-25分。在中位随访90个月后,进行最终分析,共出现了836个iDFS事件。在意向性人群中,单纯内分泌治疗组的iDFS不劣于化疗联合内分泌治疗组(HR 1.08, 95% CI 0.94, 1.24, p=0.26)。此外,在远处无复发转移间期DRFI(HR 1.03, p=0.80),无复发间期RFI(RFI; HR 1.12, p=0.28)和OS(HR 0.97, p=0.80)评估上,单纯内分泌治疗组也不劣于化疗联合内分泌治疗组。此外,2个治疗组的9年iDFS率(83.3% vs 84.3%),DRFI率(94.5% vs. 95.0%),RFI率(92.2% vs. 92.9%)和OS率(93.9% vs. 93.8%)均相似。在第一次iDFS事件中,复发的患者有338例(41.6%),其中199例(23.8%)为远处复发。治疗交互检验显示年龄是重要影响因素(iDFS p=0.03; RFI p= 0.02),而绝经状态,肿瘤大小,肿瘤分级或RS评分(连续评估或RS评分分组11-15,16-20,21-25)均不是影响因素。
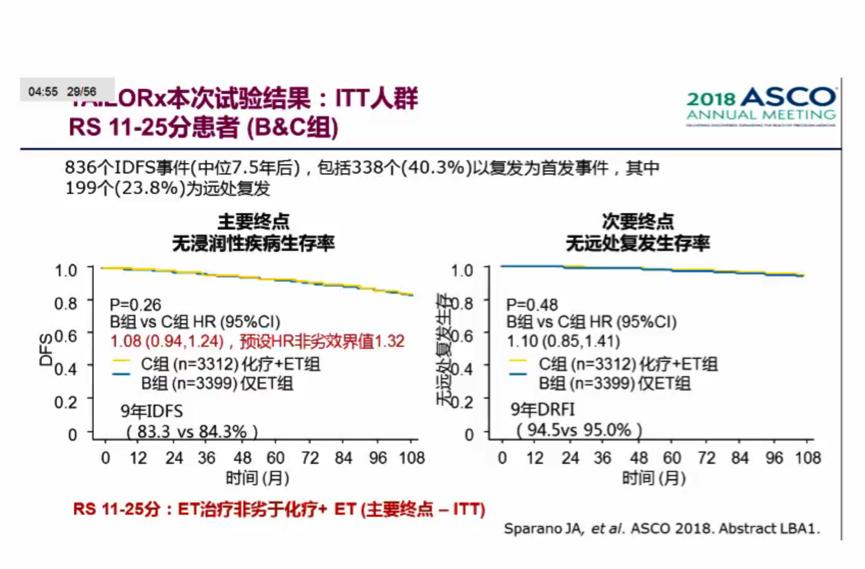
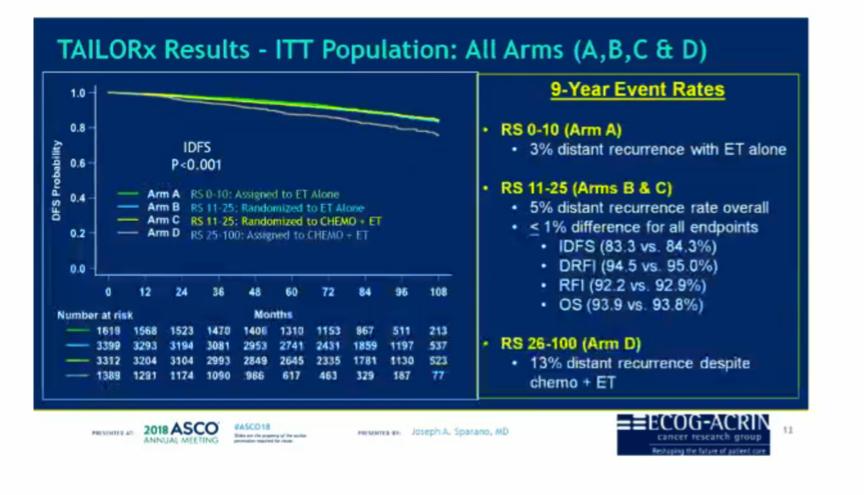
小结:TAILORx研究的主要结果证实,对于在HR+/HER2-,腋窝淋巴结阴性且RS 11-25分的患者,内分泌治疗不劣与化疗+内分泌治疗。RS 0-10分的患者,接受单纯内分泌治疗的远处复发率非常低,9年远处复发率为2-3%。RS 25-100分的患者,即使接受了辅助化疗+内分泌治疗,已有很高的复发率。
专家述评
过去,对于淋巴结阴性的HR+/HER2-乳腺癌一直存在过度治疗,目前已经有多个基因分析工具预测HR+/HER2-乳腺癌的预后,如Oncotype,mammaprint,EndoPredict,Breast cancer Index,Prosigna等。2017年更新的ASCO指南也推荐对这类患者进行多基因检测,与其他临床病理因素结合指导LN阴性,ER+/HER2-乳腺癌的治疗决策。既往的研究显示,Oncotype评分<11分的患者,接受单纯内分泌治疗的预后良好,9年随访数据显示97%的患者无远处转移。TAILORx研究达到主要终点,对于RS 11-25分的患者,内分泌治疗非劣于化疗联合内分泌治疗。探索性分析显示年龄<=50岁,RS 15-25分的女性患者,有一定的化疗获益。但TAILORx研究也存在未解决的问题,参与随机的患者多数为小肿瘤,中位肿瘤大小为1.5cm,中等分级的低危患者(57%的患者为2级),采用MINDACT评估74%的患者为临床低危患者。因此对于II/III期患者,如何决策?尚无答案。最后,殷教授总结道,TAILORx研究对临床实践的影响可总结如下:

乳腺癌专场2
本专场由军事医学科学院附属医院江泽飞教授和河北医科大学第四医院耿翠芝教授担任主持。中山大学附属肿瘤医院王树森教授解读三项研究进展,浙江省肿瘤医院王晓稼教授进行专家述评。
依维莫司(EVE) + 依西美坦(EXE) vs 依维莫司单药或卡培他滨(CAP)治疗ER+,HER2-的晚期乳腺癌:BOLERO-6, 随机,开放的II期研究
背景:EVE是口服雷帕霉素衍生物,通过变构结合mTORC1受体,抑制PI3K–mTOR通路。在BOLERO-2研究中, EVE + EXE vs EXE单药治疗既往接受过NSAI进展的HR+, HER2−ABC,显著延长mPFS (7.8 vs 3.2个月; HR 0.45; 95% CI 0.38–0.54)。CAP是口服抗肿瘤化疗药,与EVE 和 EXE的安全性不同,既往研究显示,用于HER2– 的晚期乳腺癌,mPFS为4.1–7.9个月。EVE单药也有抗肿瘤活性 (mPFS 3.5 个月,虽然目前数据有限。 BOLERO-6研究旨在补充FDA和EMA批准上市后的管制承诺,在既往接受过NSAI进展的HR+, HER2−ABC患者中,评估EVE + EXE vs EXE或CAP的疗效优势。BOLERO-6研究随机了309例患者接受EVE + EXE (n = 104), EVE单药(n = 103), 或 CAP (n = 102),主要终点为研究者评估EVE + EXE vs EVE单药预估的PFS HR;重要次要终点为EVE + EXE vs CAP预估的PFS HR。
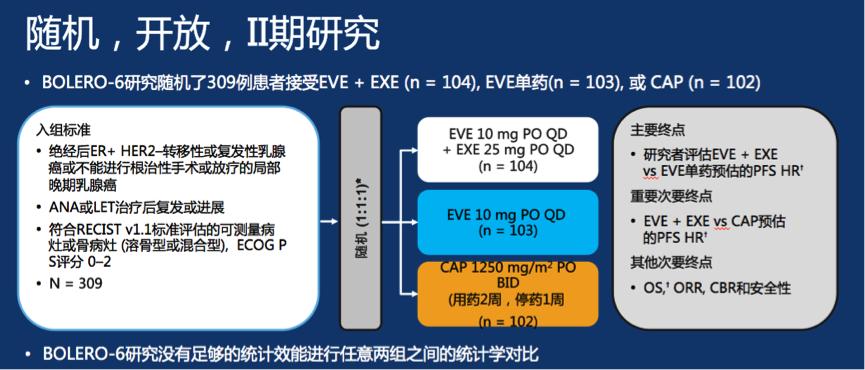
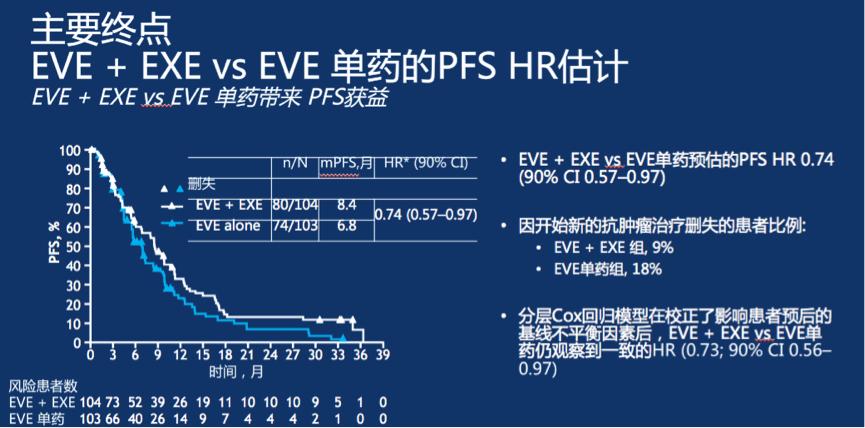
三组患者的基线特征比较,相比于含EVE方案组,CAP组下列患者更多:年龄<65岁、高加索人、完全自主活动 (ECOG PS 0)和仅合并骨转移。相比于含EVE方案组,CAP组≥3个转移灶的患者更少。主要研究终点分析显示EVE + EXE vs EVE 单药带来 PFS获益,PFS HR 0.74 (90% CI 0.57–0.97)。
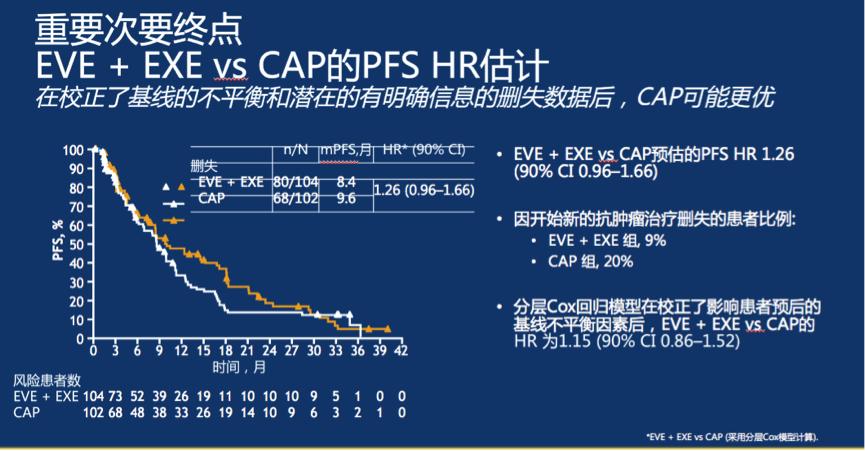
重要次要终点分析显示,在校正了基线的不平衡和潜在的有明确信息的删失数据后,CAP可能更优,EVE + EXE vs CAP预估的PFS HR 1.26 (90% CI 0.96–1.66)。OS分析显示,在Cox回归模型在校正了影响患者预后的基线不平衡因素后,EVE + EXE vs EVE 的 HR为1.27 (90% CI 0.94–1.70) ,EVE + EXE vs CAP的HR 为1.19 (90% CI 0.88–1.62)。安全性分析显示,最常见的任意级别的AE:含EVE方案组口腔炎,CAP组为PPE症状和腹泻。EVE + EXE 组 vs EVE单药组,3-4 级AEs 的发生率更高, EVE + EXE组和 CAP组,3-4级AEs发生率相当。
小结:本研究中,EVE + EXE组的mPFS (8.4 个月)与 BOLERO-2 (7.8个月)研究一致,对比EVE单药 (6.8个月), 预计可以降低26%的疾病进展或死亡风险 (HR 0.74);EVE单药治疗的mPFS组数值上长于既往小型II期研究的结果 (3.5个月)。CAP 对比 EVE + EXE组,mPFS在数值上有差异 (9.6 vs 8.4 个月), 这可能是因为CAP组患者基因特征上的优势以及潜在已知的删失数据;CAP组的mPFS与既往研究也不一致 (4.1–7.9个月)。在解读BOLERO-6研究时,必须考虑到本研究样本量较小以及开放性的设计。然而,研究结果提示EVE + EXE vs EVE单药,可以带来PFS的获益,支持既往的研究结果,对这类患者可以继续使用这一联合治疗模式。本研究中 EVE + EXE治疗的获益风险谱与 BOLERO-2研究结果相当。
SANDPIPER研究: 在ER+,PIK3CA突变的局部晚期或转移性乳腺癌中评估taselisib (GDC-0032) + 氟维司群v 氟维司群单药治疗
PI3K通路参与肿瘤的生长,增殖和生存,PIK3CA基因的激活突变和/或扩增均可以导致PI3K通路的活化。在实体瘤中PI3K通路异常活化的发生率较高,其中,在 ER+/HER2-的乳腺癌中,PIK3CA基因突变的发生率约为40%。ER和PI3K信号通路存在广泛的交叉,抑制PI3K可以导致ER通路的反应性上调。Taselisib是一个突变选择性的新一代 PI3K*制剂抑**,体外研究显示,相比于野生型PI3Kα亚型,其对突变PI3Kα亚型选择性更强。II期研究结果显示,PIK3CA突变的乳腺癌接受 taselisib联合氟维司群治疗,缓解率显著高于PIK3CA野生型肿瘤,ORR分别为38.5% vs 10.5%。
SANDPIPER研究入组了绝经后ER+/HER2-局部晚期或转移性乳腺癌,患者在接受芳香化酶治疗过程中或治疗后复发或进展。要求MBC患者至多接受过一线挽救性化疗,既往未接受过氟维司群,PI3K或 mTOR*制剂抑**治疗。研究分为2个队列,队列1计划入组PIK3CA突变的患者480例,队列2计划入组无PIK3CA突变的患者120例,两个队列的患者均随机2:1分配接受Taselisib+氟维司群或氟维司群单药治疗直至疾病进展或不可耐受的毒性。分层因素包括:内脏转移、内分泌治疗敏感性和入组地区。由中心实验室采用罗氏cobas® 检测 PIK3CA基因突变状态,主要研究终点为PIK3CA突变患者的PFS(研究者评估,INV-PFS);次要终点包括PIK3CA突变患者的ORR,OS,CBR,DoR,独立评估委员会评估的PFS(BICR-PFS)和安全性,探索性终点包括无PIK3CA突变患者的疗效。主要疗效分析人群包括所有参与随机的PIK3CA-突变的肿瘤患者。
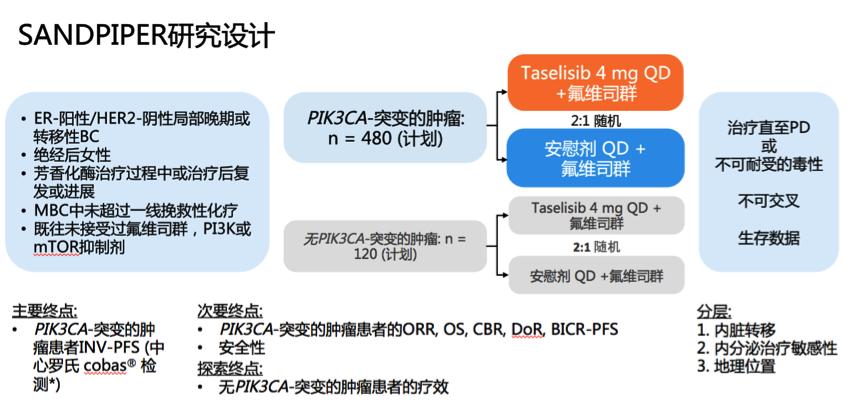
2015-4-9至2017-9-4,研究从全球28个国家149个地区共随机入组631例患者,其中PIK3CA突变患者516例。在突变人群中,分别有340例和176例患者接受Taselisib+氟维司群或氟维司群单药治疗,两组患者的基线特征均衡。研究达到主要终点,Taselisib+氟维司群对比氟维司群单药治疗,显著延长PFS,INV-mPFS分别为7.4 vs 5.4个月(分层HR 0.70,95%CI:0.56-0.89;P=0.0037)。BICR评估的PFS(9.0 vs 5.4个月)进一步确认了INV-PFS。亚组分析显示,各个亚组患者均从Taselisib+氟维司群治疗中获益。进一步根据入组患者的地理位置进行分析,亚洲患者中从Taselisib+氟维司群治疗中获益更为显著(INV-mPFS分别为7.3 vs 3.7个月,HR 0.38;95%CI:0.19-0.75;P=0.0047)。
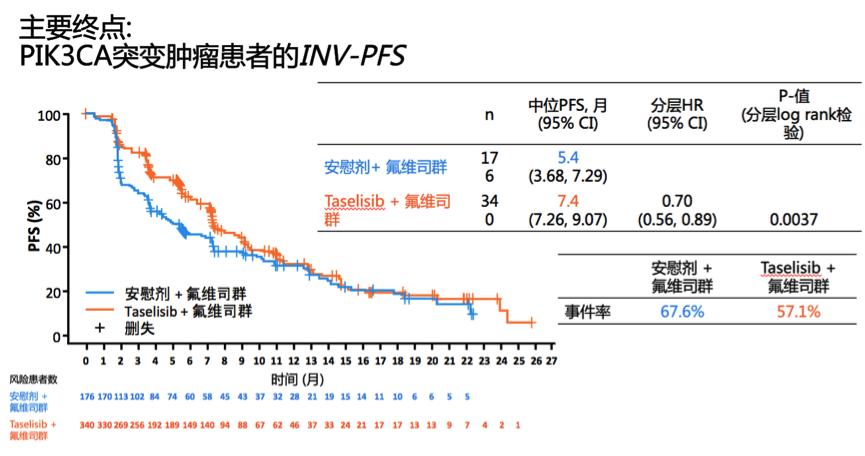
在次要研究终点评估上,Taselisib+氟维司群对比氟维司群单药治疗,显著改善ORR(28.0% vs 11.9%),CBR(51.5% vs 37.3%)和DoR(8.7 vs 7.2个月),目前,OS数据尚未成熟。探索性终点分析显示,在无PIK3CA突变患者,Taselisib+氟维司群(n=61)对比氟维司群单药(n=35)治疗的PFS和ORR均无显著差异。安全性分析显示,taselisib联合组因不良事件(AEs)永久停药的患者比例更高(20.5% vs 2.5%),但AEs停止氟维司群治疗的患者,两组相当(3.6 % vs 2.4 %)。在≥3级的AE对比上,taselisib联合组显著高于氟维司群单药组(49.5% vs 16.4%)。总体而言,Taselisib+氟维司群联合方案的安全性与预期一致,胃肠道毒性和高血糖是最常见的AEs。
小结:SANDPIPER研究达到主要终点,在氟维司群基础上联合Taselisib显著延长PIK3CA突变患者的PFS(INV-mPFS 5.4à7.4个月),此外次要终点包括ORR, CBR,DoR和BICR-PFS,联合治疗也显示出一致的优势。联合方案的耐受性较差,导致患者需要中止治疗,这可能会影响患者的临床获益。
一线AZD5363联合紫杉醇对照安慰剂联合紫杉醇治疗转移性TNBC的PAKT研究:一项随机,双盲,安慰剂对照的II期研究
背景:在TNBC患者中,PI3K/AKT信号通路常因PIK3CA或AKT1突变和PENT1-3的改变而激活;此外,TNBC常伴有PTEN的缺失,且与AKT通路激活高度相关。Capivasertib(AZD5363)是一种高选择性的口服小分子AKT*制剂抑**。在TNBC临床前模型中,无论有无PIK3CA突变,Capivasertib 均显示出其抗肿瘤活性,但敏感性与PI3K或AKT的激活和/或PTEN的缺失有关。PAKT研究旨在确定AKT*制剂抑**Capivasertib(AZD5363)联合紫杉醇治疗TNBC可改善PFS和其他疗效指标,并探索在PIK3CA/AKT1/PTEN突变亚组中,Capivasertib(AZD5363)联合紫杉醇有增强抗肿瘤活性的依据。PAKT的设计如下,统计假设PFS由研究者评估的HR为0.67,有80%的检验效能,计划在出现111例PFS实践时进行分析。

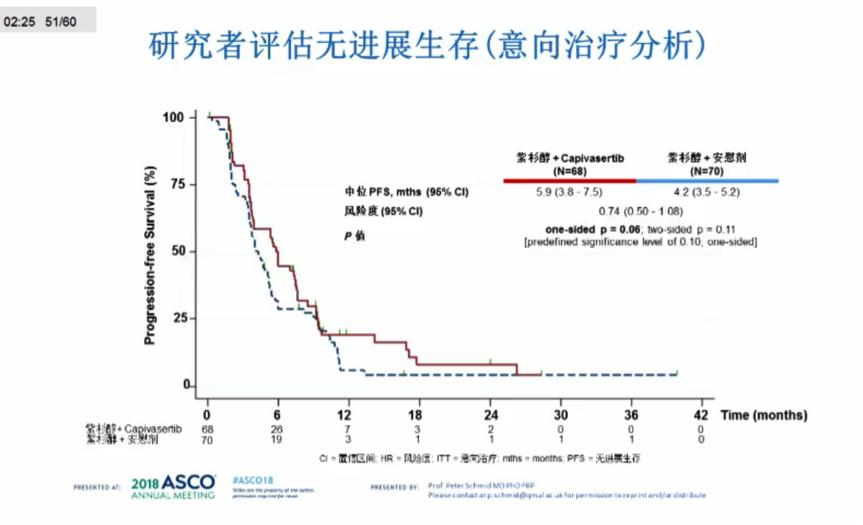
Capivasertib+紫杉醇组和安慰剂+紫杉醇组分别入组了68例和70例患者,两组患者的基线特征均衡。安全性分析显示,Capivasertib+紫杉醇组在腹泻、乏力、皮疹和口腔炎等AE的发生率上高于安慰剂组。在ITT人群中,研究者评估的两组的PFS分别为5.9和4.2个月,HR 0.74(0.50-1.08),P=0.11.
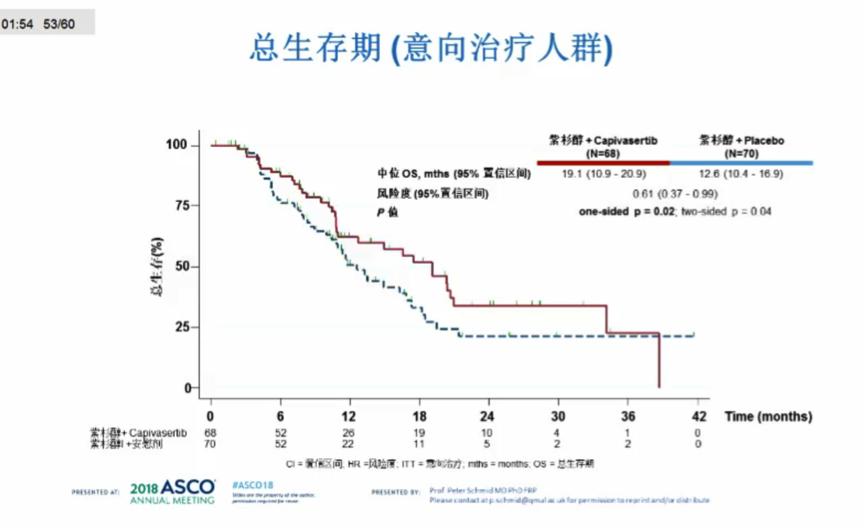
ITT人群中的OS分析显示,Capivasertib+紫杉醇组和安慰剂+紫杉醇组的mOS分别为19.1和12.6个月,HR 0.61(95%CI:0.37-0.99),P=0.04;次要中国内地分析显示,两组的ORR分别为35.4% vs 28.8%。
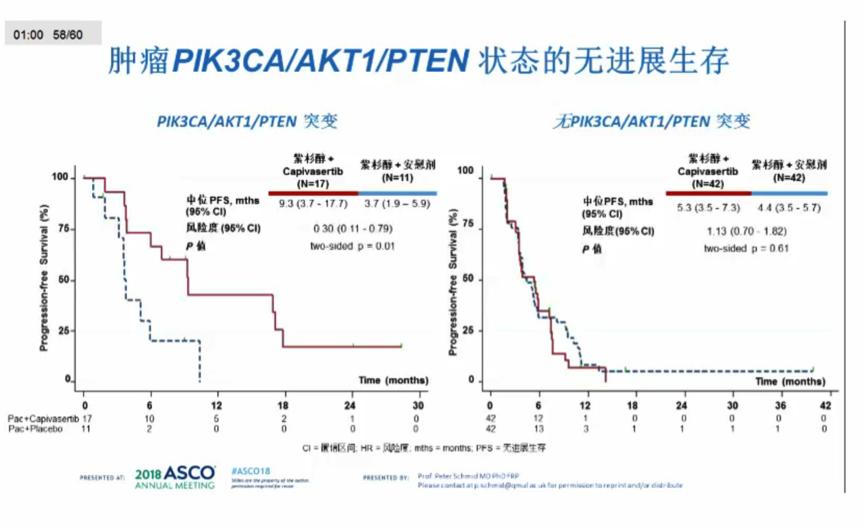
进一步根据患者的PIK3CA/AKT1/PTEN状态进行分析,结果显示在PIK3CA/AKT1/PTEN突变的患者中,Capivasertib+紫杉醇组和安慰剂+紫杉醇组的mPFS分别为9.3 vs 3.7个月,HR 0.30(0.11-0.79),P=0.01;在无PIK3CA/AKT1/PTEN突变的患者中,两组的PFS无显著差异。
小结:在TNBC患者中,一线紫杉醇治疗加入AKT*制剂抑**Capivasertib可以娴熟延长PFS和OS,PIK3CA/AKT1/PTEN突变的患者中获益更明显。最常见的3级或更严重的AE是腹泻、感染、中性粒细胞减少症、皮疹和疲劳。
专家述评
王教授总结道,上述3项研究均是针对PI3K-AKT-mTOR通路的研究,其中mTOR蛋白是一个重要的细胞信号汇集点,在正常细胞中,mTOR的活性是由上游调控信号的正负向调控来调节的。相对于mTOR*制剂抑**,PI3K和AKT*制剂抑**仍处于早期研发阶段,虽然已有3代PI3K*制剂抑**,但到目前为止没有正式批准用于临床。Capivasertib是一个能抑制AKT1/2/3的激酶*制剂抑**,以外用于不加选择的患者,治疗效果不理想。但如果结合基因突变,疗效会增加。此外,今年的ASCO会议上还有类似的研究报导“ipatasertib联合紫杉醇一线治疗局部晚期或转移性TNBC患者的随机双盲II期研究(LOTUS)总生存数据更新”。Ipatasertib组的OS显著高于紫杉醇组23.1 vs 18.4个月,支持正在进行的III期研究。
在本次的BOA会议上,特邀江泽飞教授进行了“乳腺癌治疗——精准指导下的个体化治疗”的主题演讲。在精准医学时代,主要关注乳腺癌治疗的加减法。其中加法包括:内分泌治疗(AI+mTOR,+CDK4/6,氟维司群+mTOR),靶向治疗(曲妥珠单抗+帕妥珠单抗,曲妥珠单抗+帕妥珠单抗+拉帕替尼)和免疫治疗(如联合化疗、靶向或免疫)。
1. 乳腺癌内分泌治疗的进展
ER作为内分泌治疗靶点使部分乳腺癌已经成为慢性病,内分泌治疗从追求最强单药,如TAM,AI或氟维司群向AI+或氟维司群+发展。此外,新的靶向联合已经成为标准治疗,如联合CDK4/6*制剂抑**,HDCA*制剂抑**和PI3K/AKT/mTOR*制剂抑**;而ER以外的预测指标正在研究中,有待进一步证实。其中,CDK4/6*制剂抑**的应用是近年来ER+乳腺癌最主要的研究进展,但关于CDK4/6*制剂抑**,我们仍然面临很多未知,如最佳但治疗时机和联合方案?转移性乳腺癌总生存是否改善?那种生物学类型的肿瘤疗效更好?治疗耐药的机制是什么?疾病进展后,如何治疗?关于CDK4/6*制剂抑**未来仍需要进一步的研究随访,可以尝试综合以往的临床研究结果进行荟萃分析和生物标志物研究,同时开发新的联合方案,基于良好的临床前和转化医学研究,优化患者选择和疾病进展后续治疗。此外,还应该尝试扩展HER2+乳腺癌及其早期辅助治疗。
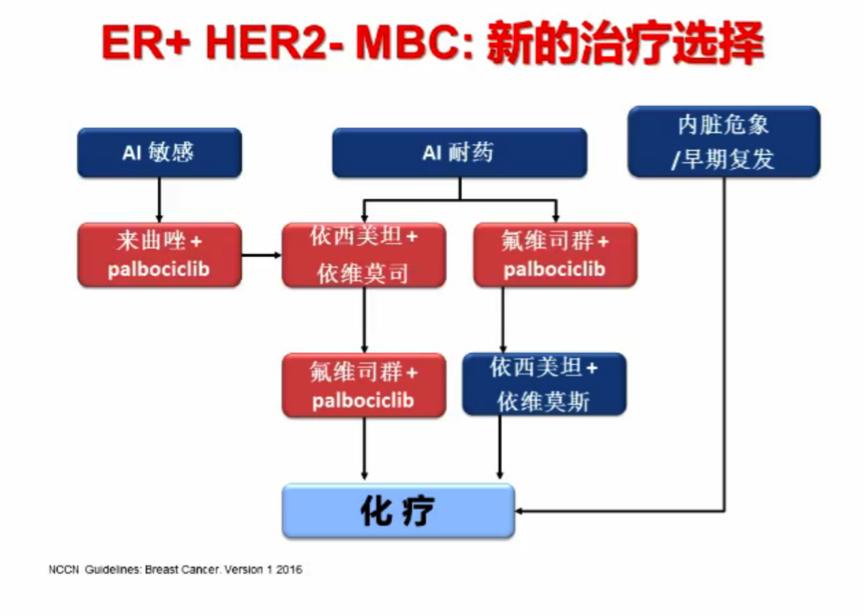
2. 乳腺癌靶向治疗进展
针对HER2基因的靶向治疗成为把握驱动持续抑制的成功范例,目前转移性乳腺癌的抗HER2治疗已经进入二线(TKIs/TDM1),EBC的新辅助/辅助治疗疗效有待进一步提高(可考虑曲妥珠单抗+帕妥珠单抗),辅助治疗需要更具其他危险因素进行加减法,HER2突变、通路活化成为克服耐药的新靶点。对于HER2阳性早期乳腺癌的个体化治疗:1年曲妥珠单抗还是HER2阳性早期乳腺癌的标准治疗,部分HER2阳性患者(LNM+/HR-)需要双靶向联合治疗(曲妥珠单抗+帕妥珠单抗),期待后续辅助抗HER2治疗进入临床(曲妥珠单抗àTKIs),相对低危患者可以考虑半年疗程(HR+/LNM-/不能耐受),术前新辅助治疗为HRE2阳性早期乳腺癌个体化治疗提供平台。
3. 乳腺癌化疗进展
激素依赖性乳腺癌化疗地位开始下降,但还有地位。HER2阳性患者靶向药物需要联合化疗。三阴性乳腺癌治疗目前还是化疗为主,免疫治疗也需要与化疗联合,此外,新靶点药物与化疗也正在进行联合研究。此外,很多乳腺癌的新药正在开发,如在今年ASCO大会上报道的来自中国的新药Utidelone,未来关于转移性乳腺癌的药物研发模式总结如下:
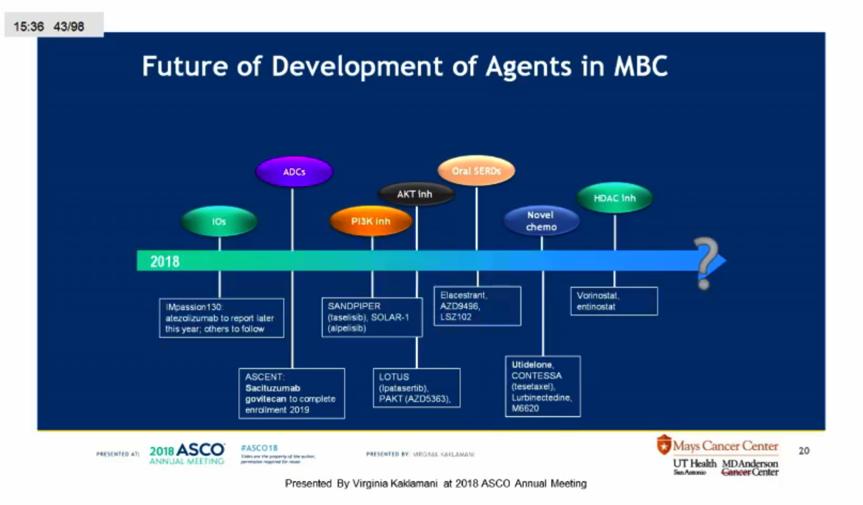
会上,江教授同时对TAILORx研究进行重点点评,这一研究结果的公布,一石激起千层浪,很多的媒体或专家迅速报道“70%的早期乳腺癌患者可以摆脱化疗”,江教授呼吁在热潮中我们需要冷思考,应该认真聆听研究解读。用21基因数字化标定早期乳腺癌患者的不同预后,从而展出那些不需要化疗效果也挺好的患者是大家一直追求的理想。目前共识认为,对于那些低风险患者,即同时符合肿瘤不大、淋巴结阴性、ER阳性、HER2阴性的患者,如RS评分低(<11),可以不化疗,单用内分泌治疗即可;如果RS评分高(>30),还是需要化疗。因此,这绝对不是70%的早期乳腺癌患者可以免除化疗!目前国内外指南关于辅助化疗的标准为:大部分HER2阳性、三阴性、腋窝阳性的早期乳腺癌需要术后辅助化疗,还有部分年轻、分化指数(Ki67)高的患者应考虑化疗,以上患者在我国临床实践中占比应在50-70%,某些地区可能更高,所哟u 符合国际研究TAILORx可免除化疗的早期乳腺癌患者,在我国应该不到30%。CSCO BC数据库中此类患者仅10%。
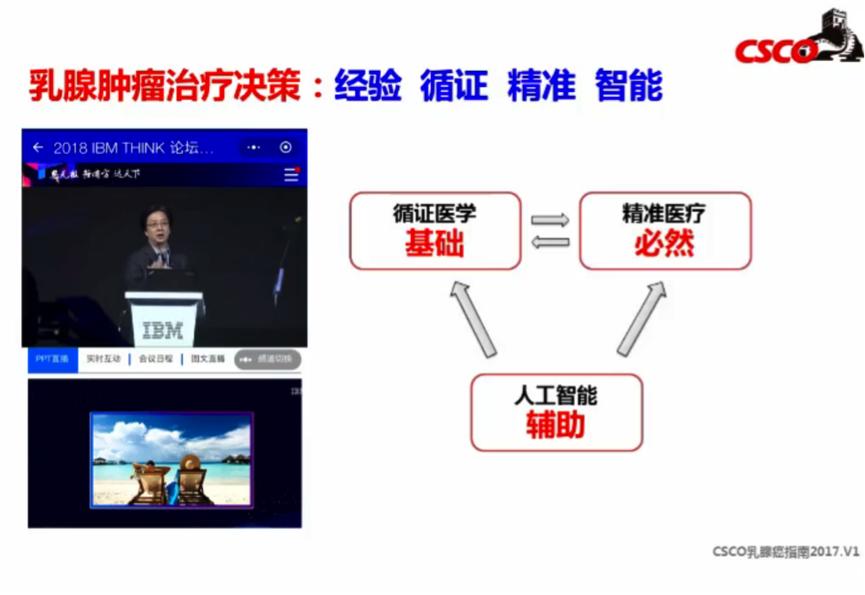
会议最后,江教授对CSCO乳腺癌诊疗指南(2018. V1)的更新要点进行解读,并结合具体病例总结道,乳腺肿瘤治疗的决策应该基于“经验、循证、精准、智能”综合决策。
相关阅读:
【Best of ASCO 2018 China】肺癌专场精彩回顾
http://www.liangyihui.net/doc/44725
【Best of ASCO 2018 China】胃肠肿瘤专场精彩回顾
http://www.liangyihui.net/doc/44734
【2018 ASCO】重磅研究!TAILORx试验显示:七成早期乳腺癌女性不会从化疗中获益
http://www.liangyihui.net/doc/43005
【2018ASCO】聚焦“晚期乳腺癌”专场,这些研究不容错过!
http://www.liangyihui.net/doc/42788
【2018ASCO】聚焦“早期乳腺癌”专场,热点研究一网打尽
http://www.liangyihui.net/doc/42762
责任编辑:肿瘤资讯-贾老师
版权声明
版权属肿瘤资讯所有。欢迎个人转发分享,其他任何媒体、网站如需转载或引用本网版权所有内容,须获得授权,且在醒目位置处注明“转自:良医汇-肿瘤医生APP”。