胰腺纤维化是慢性胰腺炎和胰腺癌的主要病理特征;肝脏纤维化是病毒性肝炎、脂肪性肝病、酒精肝向肝硬化发展过程中的关键步骤和影响预后的重要环节。若上述慢性损伤与器官纤维化持续存在,可能加速胰腺癌或肝硬化/肝癌进展,造成严重危害。近年来,纳米制剂在临床药物研发领域崭露头角,基于其优异的靶向递药特性和良好的生物相容性,在纤维化疾病、肿瘤与糖尿病防治中显示出巨大的潜能。
东南大学附属中大医院院长助理、内分泌科主任李玲教授与国内外知名学者深度合作,医工交叉、医药融通,2022年在国际主流期刊Biomaterials(Q1,IF:15.304)[1]和ACS Nano(Q1,IF:18.027)[2]期刊发表两项最新研究,通过构建胰腺、肝脏靶向治疗平台,抑制星状细胞活化,重塑纤维化失衡的细胞外基质,逆转胰腺与肝脏纤维化,为维持糖脂代谢稳态提供了创新平台,研究工作得到国家自然科学基金项目、江苏省重点研发计划(临床前沿技术)项目支持。该研究与美国加州大学Stephen J. Pandol教授及中国药科大学姜虎林教授合作,博士生祁靓和硕士生张凌烽分别为文章的第一作者。

研究一
重塑失衡的细胞外基质以逆转胰腺纤维化[1]
要点概览
基于纳米递送技术构建胰腺靶向药物递送平台,AT-CC具有良好的胶原靶向消融特性,显著增强药物在胰腺纤维化区域的蓄积和深层渗透。
AT-CC到达胰腺后可释放全反式维甲酸(ATRA)以及四硫代钼酸铵(TM),一方面抑制胰腺星状细胞(PSC)激活,减少胶原等细胞外基质的产生;另一方面抑制其交联沉积,促进基质金属蛋白酶对其逐步降解。
AT-CC具有良好的生物相容性和安全性,为重塑纤维化失衡的细胞外基质,有效逆转胰腺纤维化提供创新平台。
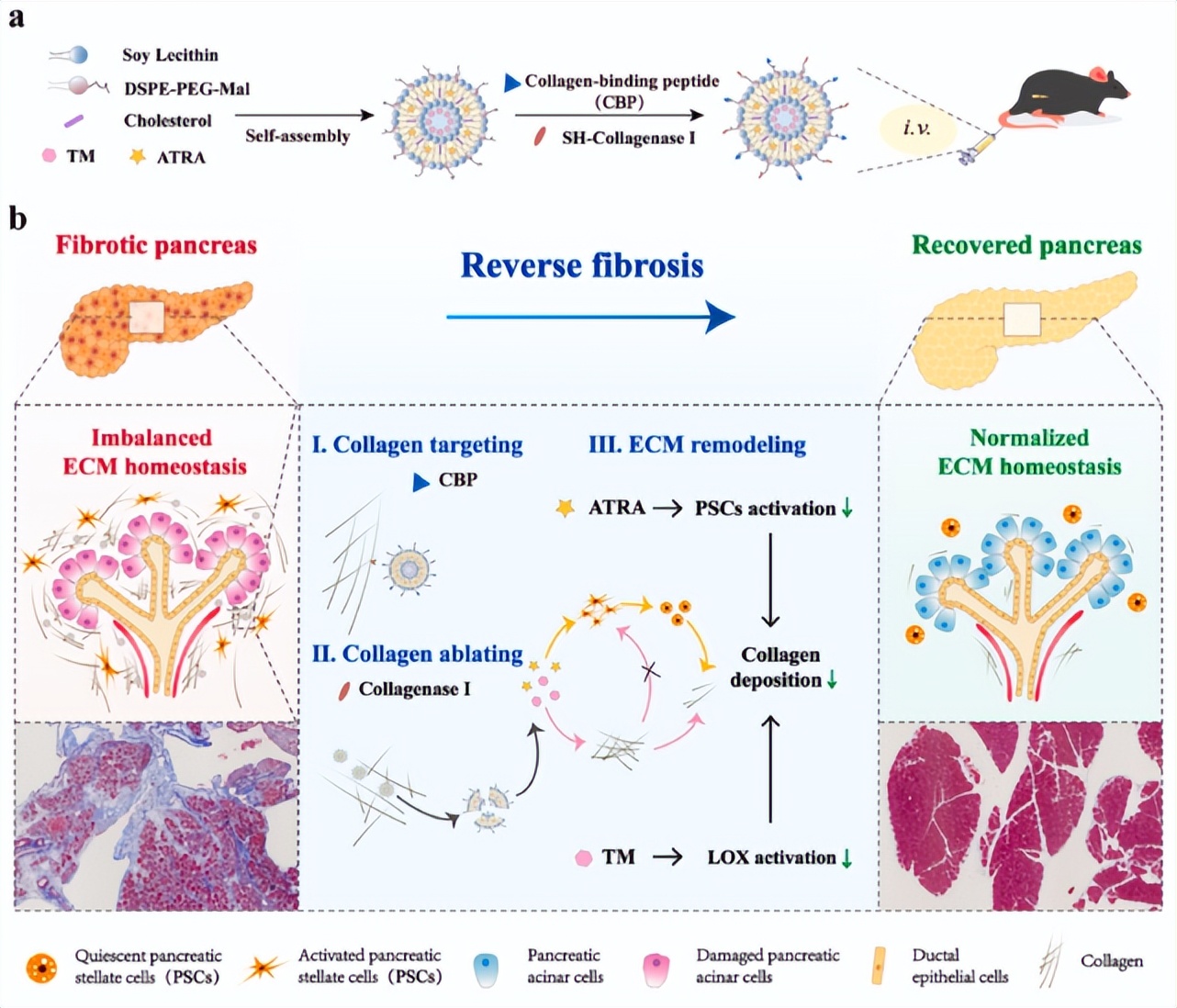
图1.(a)AT-CC制备流程;(b)AT-CC通过尾静脉注射后,在靶向片段CBP作用下蓄积在胶原沉积的胰腺纤维化区域,随着细胞外基质逐步被胶原酶消融,AT-CC深层渗透,释放药物ATRA和TM,二者共同作用,重塑失衡的细胞外基质,促进胰腺组织再生。
研究二
双纳米穿透剂重塑毛细血管化肝窦和细胞外基质屏障用于肝纤维化治疗[2]
要点概览
针对肝纤维化病理条件下毛细血管化的肝窦和沉积的细胞外基质阻碍药物蓄积的病理特点,设计了双纳米穿透剂调节肝窦内皮细胞,恢复肝窦窗孔,消融过度生成的细胞外基质并使活化的肝星状细胞(HSC)转变为静息态,最终成功逆转肝纤维化病理微环境,实现靶向治疗。
通过顺序递送肝窦内皮细胞(LSEC)靶向和窗孔修复纳米制剂(HA-NPs/SMV),以及HSC靶向及胶原消融纳米制剂(CV-NPs/siCol1α1),修复肝纤维化时的病理屏障。
双纳米靶向治疗平台具有良好的生物相容性和安全性,为重塑毛细血管化的肝窦窗孔和沉积的细胞外基质,有效逆转肝纤维化提供创新平台。
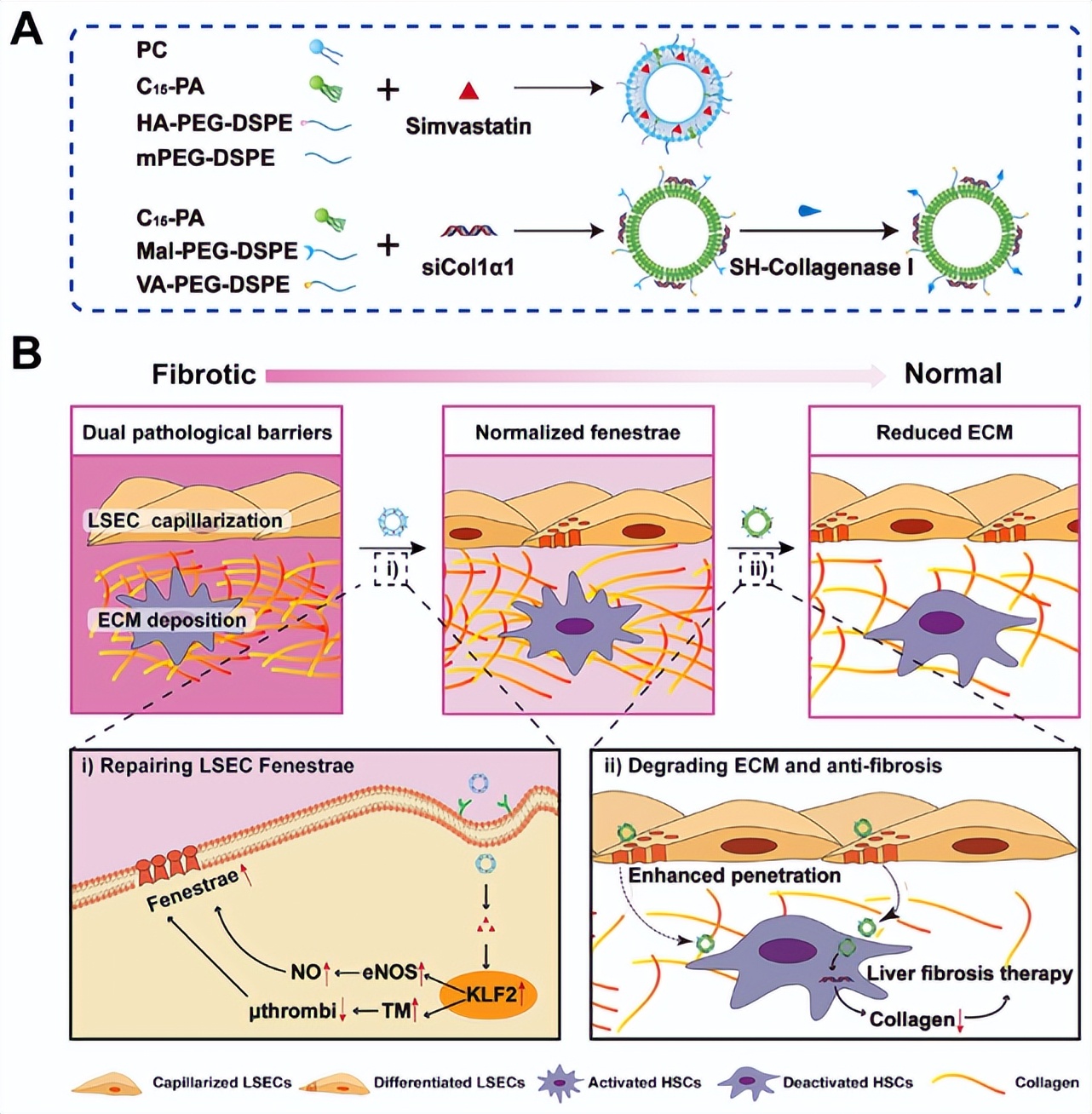
图2.(a)双纳米制剂制备流程;(b)HA-NPs/SMV靶向LSEC,释放辛伐他汀(SMV)以修复窗口;CV-NPs/siCol1α1靶向HSC,穿透胶原屏障,释放siCol1α1,二者协同通过调节肝纤维化病理屏障,推动肝纤维化微环境的逆转。
总结
本研究以“医工交叉融合”的理念,集成临床医学、药剂学和基础医学多学科优势,基于纳米靶向递送技术,实现胰腺纤维化与肝脏纤维化的靶向治疗,为逆转器官纤维化及糖脂代谢稳态失衡提供了新策略,为慢性纤维化性炎性疾病的临床治疗和新药的研发提供平台。

专家简介
李玲 教授
东南大学附属中大医院
德国医学博士、美国UCLA博士后
主任医师、教授、博士生导师
东南大学胰腺研究所所长
东南大学糖脂代谢研究中心主任
东南大学附属中大医院院长助理、内分泌科主任
中华医学会糖尿病学分会青委
江苏省医学会糖尿病分会副主委
江苏省中青年领军人才、江苏省“青年科技奖”获得者
国家工信部5G+健康医疗课题负责人,国家科技部重点研发计划干细胞子课题负责人,主持国家自然科学基金5项、江苏省重点研发计划项目2项(临床前沿技术、新型临床诊疗技术)
以通讯作者在Nature子刊等发表SCI论文50余篇,IF>10分国际主流期刊论文10余篇。申报/授权国家发明专利7项,获国家教育部科技进步二等奖,江苏医学科技奖、江苏省新技术引进一等奖(均排名第1)
参考文献:
1. Qi L, Han H, Han MM, Sun Y, Xing L, Jiang HL, Pandol SJ, Li L. Remodeling of imbalanced extracellular matrix homeostasis for reversal of pancreatic fibrosis. Biomaterials. 2023 Jan; 292: 121945. doi: 10.1016/j.biomaterials.2022.121945.
2. Zhang LF, Wang XH, Zhang CL, Lee J, Duan BW, Xing L, Li L, Oh YK, Jiang HL. Sequential Nano-Penetrators of Capillarized Liver Sinusoids and Extracellular Matrix Barriers for Liver Fibrosis Therapy. ACS Nano. 2022 Sep 27; 16(9): 14029-14042. doi: 10.1021/acsnano.2c03858.