文|斯文Talk
编辑|斯文Talk

前言
线粒体载体(MCs)是真核生物核编码的膜蛋白,可将二羧酸和三羧酸、酮酸、氨基酸、核苷酸、辅酶辅因子、硫酸盐和磷酸盐转运穿过线粒体内膜一。
它们构成一个蛋白质家族,包含排列在约100个氨基酸的三个同源串联序列重复序列中的独特和保守的序列特征,每个重复序列包含两个疏水跨膜片段,由一个特征序列基序PX[D/E]XX[K/R]X[K/R][D/E]GXXXX[W/Y/F][K/R]G。
这些序列特征已被用于识别各种生物基因组中编码MCs的基因,结果,人类中的53个成员,35个在酿酒酵母和58英寸拟南芥已被检测到。
大多数MC基因编码的蛋白质几乎完全由这三个重复序列组成,但有些编码更长的MC,在其N-末端有一个额外的延伸结构域。根据底物特异性和独特的三联体,MC家族成员可分为超过25个亚家族。

碱性氨基酸的线粒体载体
人鸟氨酸携带者ORC1 (SLC25A15)和ORC2 (SLC25A2)是两种同种型,在其MC结构域中具有88%相同的蛋白质序列。
它们在酵母中的*亲近**是Ort1p,其接触点上具有与ORC1相同的带电荷残余物,这将在之后详细讨论。
Ort1p是第一个被鉴定为鸟氨酸转运蛋白的MC,事实上,重组Ort1p被证明转运鸟氨酸以交换质子、精氨酸或赖氨酸。
在EPRA方法表征中,5-磷酸吡哆醛和红菲咯啉用作*制剂抑**,但是N-乙基马来酰亚胺、对羟基苯甲酸汞、对氯汞苯磺酸和水杨酸甲酯也是Ort1p的有效*制剂抑**。
它的主要生理作用被认为是将线粒体鸟氨酸输出到胞质溶胶中,其中鸟氨酸用于精氨酸的生物合成,这一建议与先前的意见一致,即南酿酒酵母具有Ort1p基因突变的菌株依赖于精氨酸的补充才能正常生长。
在肝脏、胰腺、肺、*丸睾**、小肠、脾、肾、脑和心脏中发现了人ORC1和ORC2 mRNAs,其中前一种载体总是以较高水平表达。
这两种亚型都转运带正电荷的氨基酸鸟氨酸、赖氨酸和精氨酸,以及中性氨基酸瓜氨酸。
此外,ORC2转运碱性氨基酸组氨酸、高精氨酸、单甲基精氨酸和不对称二甲基精氨酸(ADMA),以及D-型赖氨酸、精氨酸、鸟氨酸和组氨酸,国王mORC1和ORC2的鸟氨酸值分别约为0.2和0.4 mM最大鸟氨酸鸟氨酸同源交换的值分别为3和1.2毫摩尔/分钟/克蛋白质。
最大赖氨酸和精氨酸同源交换蛋白的值与鸟氨酸同源交换蛋白的值在相同的范围内,而Km赖氨酸和精氨酸的ORC1值分别为约0.8和1.6 mM,ORC2值分别为0.3和0.7 mM。
磷酸吡哆醛被用作ORC1和ORC2的*制剂抑**,但是它们的活性也被汞和N-乙基马来酰亚胺显著抑制。
决定ORC1和ORC2不同底物特异性的残基已经通过接触点残基的定点诱变和它们对转运特性影响的表征进行了彻底研究,虽然ORC1在接触点II具有典型的RE基序,但ORC2具有QE。
当ORC1接触点II的精氨酸与谷氨酰胺交换时(如ORC2 ),底物特异性变得与ORC2和V最大鸟氨酸的同型交换减少了13倍。
反之亦然当ORC2的接触点II中的谷氨酰胺变为精氨酸时,底物特异性转化为ORC1和V的底物特异性最大增加了33倍。
这些实验表明ORC1和ORC2接触点II的残基结合Cα羧基和氨基,因为与该位置被谷氨酰胺占据的蛋白质相比,该接触点的第一个位置上精氨酸的存在赋予蛋白质更严格的底物特异性,具有更高的立体选择性和更高的转换数。
此外,其他结果提供了证据,即接触点I中的谷氨酸是最有可能与底物侧链的末端氨基相互作用的候选者。
假设跨膜α-螺旋四(ORC1和ORC2中的W224)上的色氨酸介导接触点II和III之间的相互作用,从而涉及构象变化中的所有三个接触点。
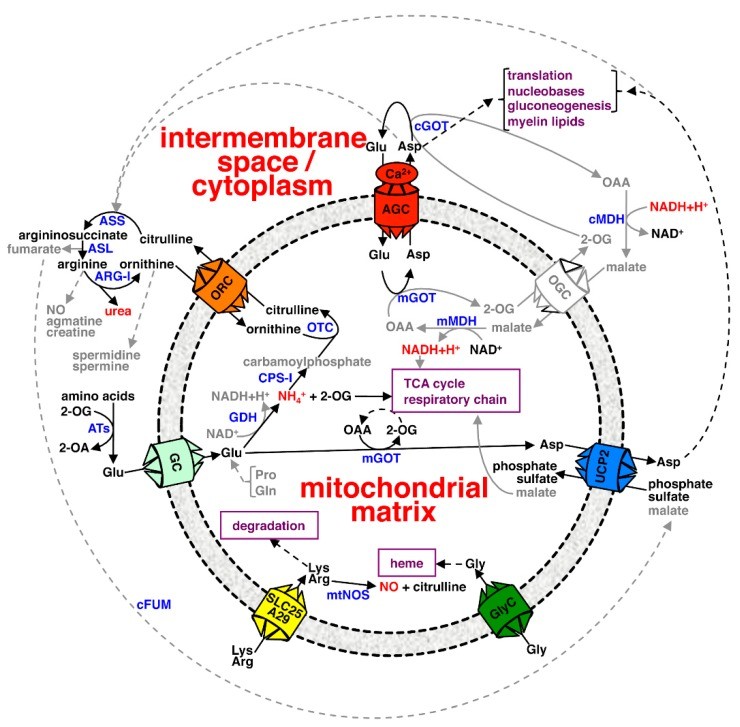
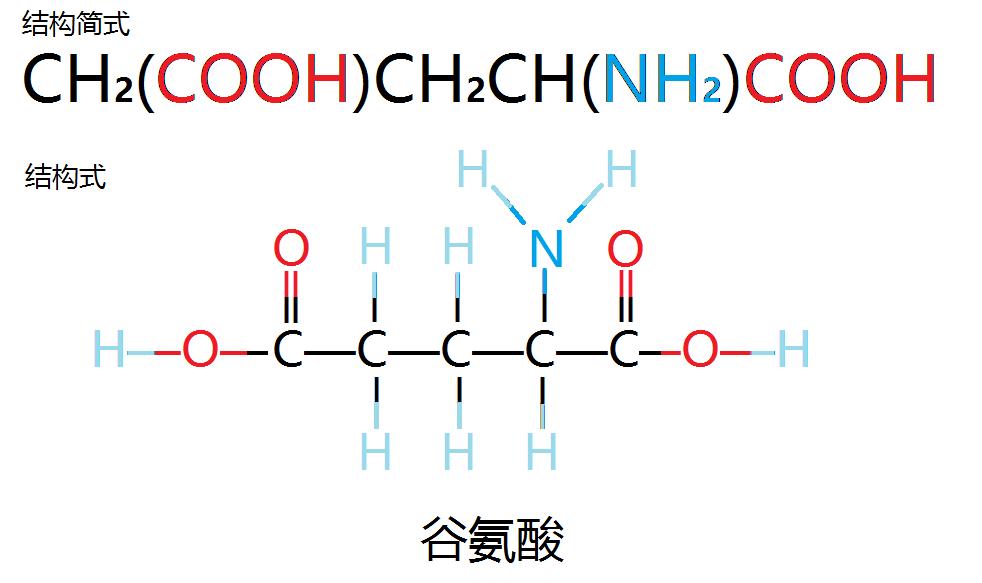
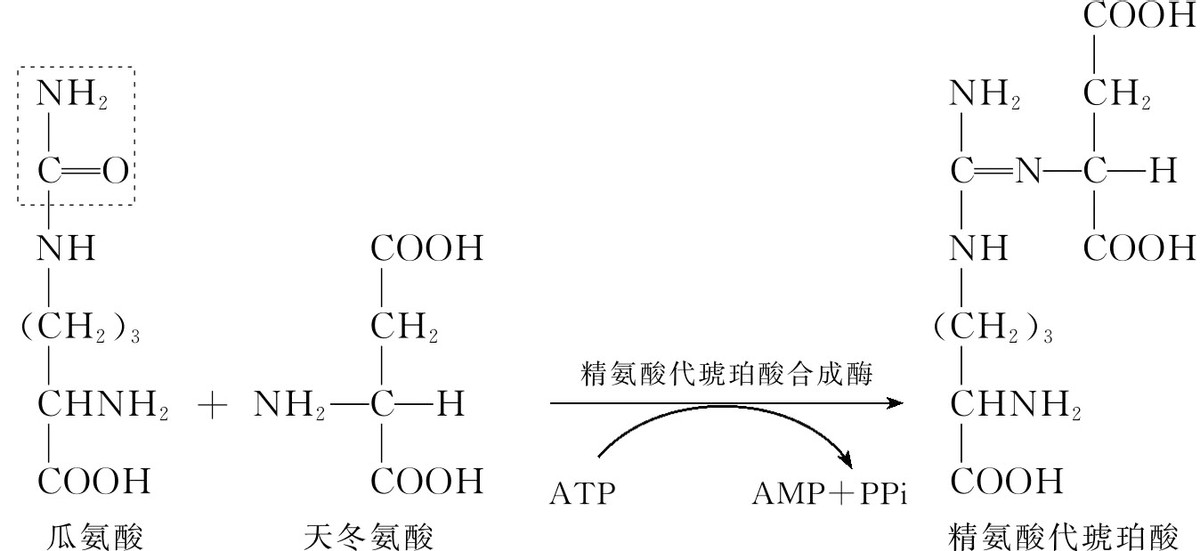
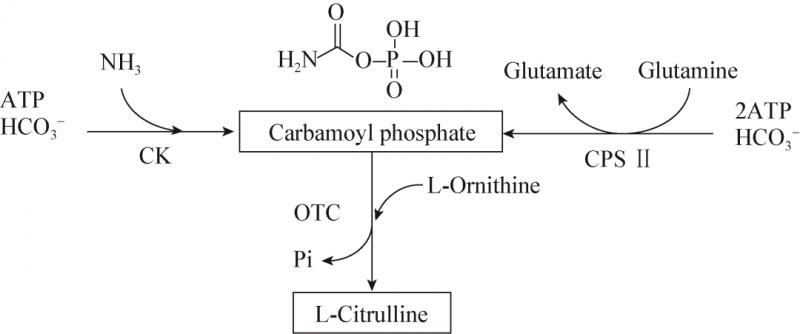
ORC1在主要发生在肝脏,过量的氨穿梭进入线粒体,通常以谷氨酸的形式被GCs,与来自ATP的碳酸盐和磷酸盐缩合,通过氨甲酰磷酸合成酶I形成氨甲酰磷酸。
随后,氨甲酰磷酸用于通过鸟氨酸氨甲酰转移酶将鸟氨酸转化为瓜氨酸,鸟氨酸氨甲酰转移酶是尿素循环中唯一的基质定位酶。
ORC1参与胞质鸟氨酸的输入,以交换线粒体内的瓜氨酸,在胞质溶胶中,尿素循环的其余三种酶将瓜氨酸转化为鸟氨酸和无毒的尿素,然后排出体外。
肝脏ORC1的表达水平受激素调节,并与尿素循环的其他酶协调。
此外,在小肠中,ORC1和ORC2被认为参与了线粒体内瓜氨酸(来源于谷氨酸、谷氨酰胺和脯氨酸)的输出,该瓜氨酸用于肾脏和肝脏中精氨酸的生物合成。

除了结合到蛋白质中,特定细胞类型中的精氨酸还被用作产生胍丁胺、肌酸、精胺、亚精胺和一氧化氮的前体,并被再转化为谷氨酸、谷氨酰胺和脯氨酸。
多胺精胺和亚精胺抑制这两种人类ORC亚型,这可能表明反馈抑制调节机制。
此外,ORC2介导的ADMA跨线粒体膜转运可发挥两种功能:将线粒体蛋白水解产生的ADMA输出到细胞质中,用于二甲基精氨酸二甲基氨基水解酶(DDAH)降解胞质,或通过质膜转运蛋白从细胞中输出,以及将ADMA吸收到线粒体中,使胞质ADMA能够被线粒体丙氨酸-乙醛酸氨基转移酶2降解。
值得注意的是,在呼吸的线粒体中,与线粒体的单向流出相比,带正电荷的ADMA的单向摄取受到质子动力的电分量(内部为负)的支持。
然而,ADMA可以通过电中*交性**换机制由ORC2输出(以及输入)以交换阳离子氨基酸赖氨酸和精氨酸。ORC2也转运单甲基精氨酸,高精氨酸以及可能的二-和三-甲基精氨酸。
鉴于线粒体基质中存在甲基化各种蛋白质的酶,很可能线粒体内的单甲基、二甲基和三甲基精氨酸从线粒体输出到细胞质。
相比之下,高精氨酸在体内跨线粒体膜转运的方向还不清楚,因为各种间接线索表明高精氨酸的生物合成或分解代谢发生在线粒体基质中。
事实上,ORC2催化赖氨酸、精氨酸、鸟氨酸和组氨酸的D-型转运,以及它们的L-型转运,证明它不能区分这些对映异构体,可以解释为表明ORC2参与了由各种食物提供的这些阳离子氨基酸形式的代谢。
由编码ORC1的SLC25A15基因突变引起的HHH综合征强调了ORC1转运功能在人类代谢中的重要性。
有缺陷的ORC1降低了尿素循环的速率,导致高氨血症和胞质溶胶中鸟氨酸的积累,这导致高鸟氨酸血症、多胺水平增加和继发性肌酸缺乏。
有缺陷的ORC1还诱导氨甲酰磷酸增加,氨甲酰磷酸部分与赖氨酸缩合,通过鸟氨酸氨基转移酶的作用形成高瓜氨酸,部分进入嘧啶途径,解释了高瓜氨酸尿和尿中乳清酸排泄增加。
该综合征的临床特征通常始于新生儿期至儿童期,较少见于成年期,为嗜睡、意识模糊发作、凝血异常、肝炎样发作、以锥体束征为特征的渐进性神经功能障碍、小脑征、认知缺陷、异常行为和食用高蛋白饮食后经常出现的昏迷。
处方治疗包括低蛋白饮食和补充精氨酸和氨清除剂,这允许几乎正常的预期寿命。有趣的是,ORC2可能仅部分弥补了HHH综合征患者*功中**能性ORC1的缺乏,因为它在肝脏中的表达少得多,并且对鸟氨酸的亲和力比ORC1低。

中性氨基酸的线粒体载体
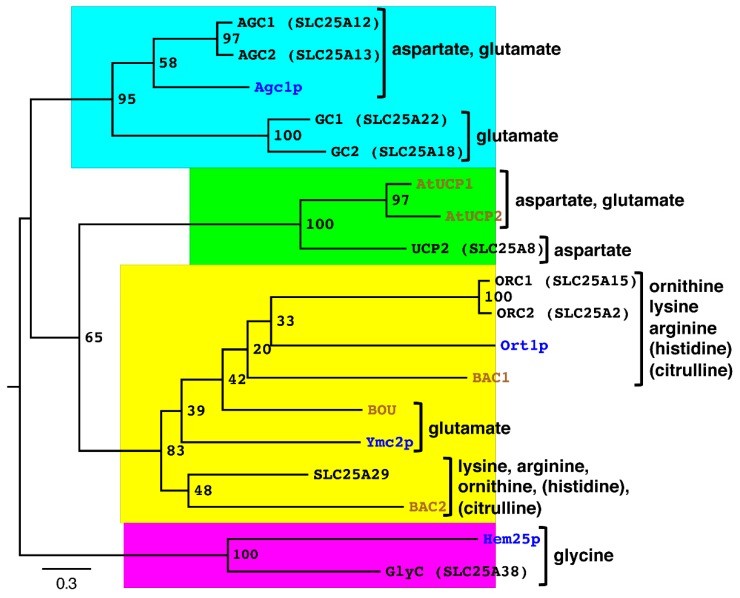
甘氨酸、人GlyC (SLC25A38)和酵母Hem25p (YDL119cp)的MCs被发现存在于一个系统发育聚类中,与所有其他转运上述氨基酸的MCs。
GlyC和Hem25p在它们的MC结构域*共中**享35%的相同序列,与Agc1p具有第二高的同一性百分比。
虽然证据不足,但这可能表明,与其他MCs相比,GlyC和Hem25p与Agc1p具有更近的共同进化祖先,分别具有18%-26%和21%-27%的同一性。
此外,GlyC和Hem25p在接触点II都具有RD,并且正如人们从底物侧链中不存在电荷所猜测的,在接触点I没有带电的残基。
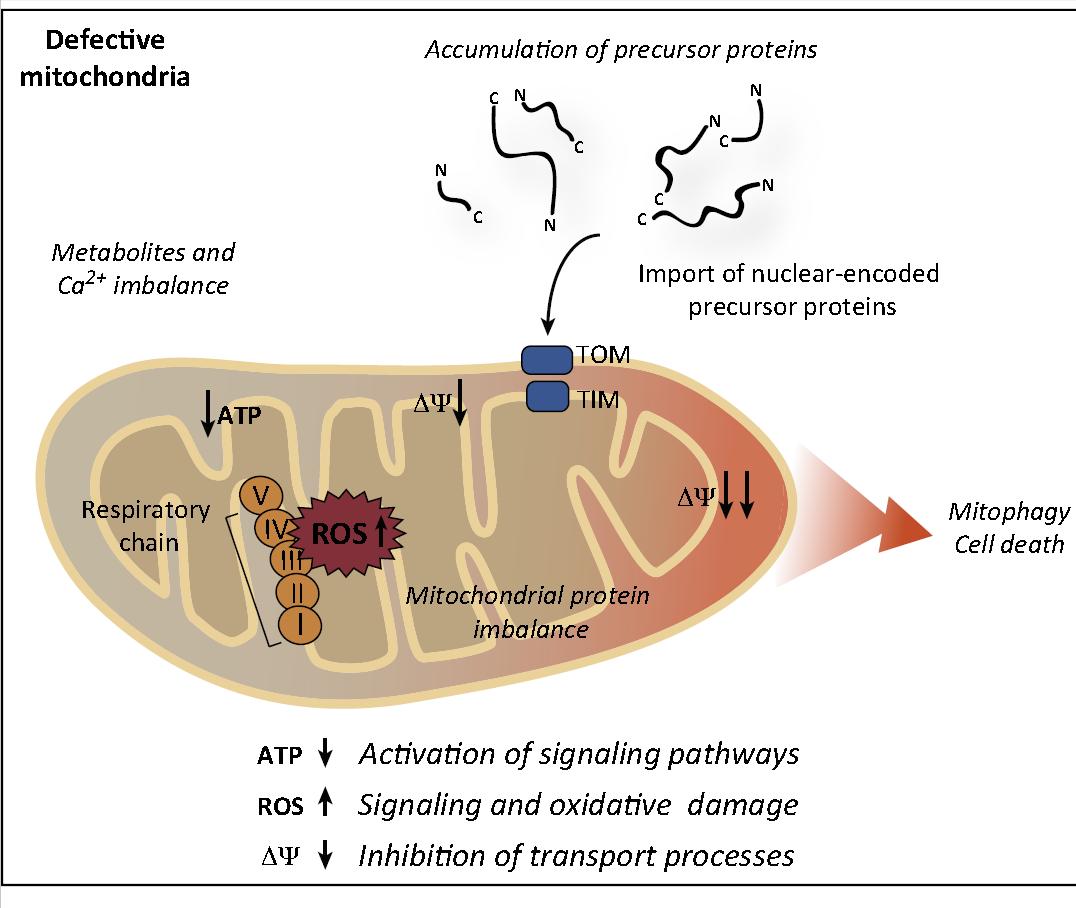
人类基因的突变SLC25A38被发现引起先天性铁粒幼细胞性贫血,这是一种以成红细胞中线粒体铁超载为特征的疾病。
这一发现导致推测MC SLC25A38可能参与血红素和铁-硫簇的生物发生,可能是通过运输甘氨酸,后来,一份基于使用EPRA方法获得的发现的报告提供了GlyC和Hem25p转运甘氨酸的证据。
酵母转运蛋白被更详细地表征;它是Km和V最大甘氨酸甘氨酸反向转运体的值分别为0.75 mM和170 μmol/min/g蛋白质。
甘氨酸反向转运蛋白的初始转运速率比甘氨酸单向转运蛋白高约6倍。
Hem25p转运活性被5’-磷酸吡哆醛、向红菲咯啉、单宁酸和对羟基苯甲酸汞有效抑制,线粒体分离自aHem25缺失菌株显示甘氨酸摄取减少,这通过重新引入缺失基因得以恢复。
此外,该Hem25缺失菌株在不可发酵碳源上表现出生长缺陷,呼吸效率降低,细胞色素bc1复合物、血红素和细胞色素含量减少,这些都可以通过重组表达Hem25p或GlyC。
基于这些实验,Hem25p和GlyC被认为负责将甘氨酸输入线粒体,其中甘氨酸转化为血红素前体δ-氨基乙酰丙酸盐。
随后,δ-氨基乙酰丙酸通过未知的转运蛋白输出到细胞质中,进行进一步的酶转化,形成卟啉中间体,该中间体穿梭回到线粒体基质中,形成血红素基团。在酵母中,由Hem25p引入到基质中的甘氨酸也可用于通过甘氨酸裂解系统合成叶酸衍生物。

结语
许多转运不同氨基酸的MCs的转运特性已经得到很好的表征,并显示出以不同的底物特异性转运天冬氨酸、谷氨酸、鸟氨酸、瓜氨酸、赖氨酸、精氨酸、组氨酸和甘氨酸。
进一步的研究应旨在更好地探索表征的MCs对氨基酸的体外活性如何与它们在体内、各种生物体、组织和细胞类型中的特定生理作用相关联。
此外,考虑到已鉴定的转运氨基酸的人MCs在接触点II具有R(除了ORC2和UCP2分别具有QE和RN),SLC25A39、SLC25A40、SLC25A45、SLC25A47和SLC25A48可能是氨基酸转运的候选者。
到目前为止,已经确定的氨基酸MCs在氨基酸的大量运输中起作用,这些氨基酸是途径中的代谢物或被再循环,例如在苹果酸-天冬氨酸穿梭或尿素循环中。
理论上,氨基酸的MCs也有助于为翻译线粒体DNA编码的蛋白质提供构件。然而,由于所有的氨基酸都可以转化,至少间接转化为TCA循环代谢物,多余的氨基酸可能被氧化并用于能量代谢。