冠状病毒(Coronaviridae, CoV) 是一类严重危害人类及家畜家禽健康的病原微生物,在自然界中广泛存在,其自然宿主包括人、牛、猪、禽及犬、猫、鼠、蝙蝠等,该属病毒的广泛宿主特点以及自身基因组的结构特征使其在进化过程中极易发生基因重组和变异,呈现遗传多样性,新亚型及新的冠状病毒在此过程中不断出现。病毒在电子显微镜下可见如日冕般外围的冠状,因此被称为冠状病毒。严重程度从感冒到重症疾病不等,如中东呼吸综合征(MERS)和重症急性呼吸综合征(SARS)及目前新命名的新型冠状病毒(2019-nCoV)。
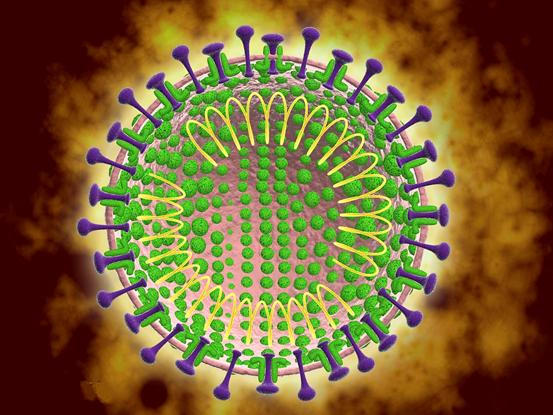
冠状病毒示意图
冠状病毒分类
冠状病毒属于单股正链RNA 病毒,冠状病毒科冠状病毒属,根据病毒的抗原性,大部分研究文献将已知并已定型的冠状病毒分为3 群,其中第1 群和第2 群为哺乳动物病毒,第3 群为禽类病毒。第1 群包括人冠状病毒229E(HCoV-229E) 、猪传染性胃肠炎病毒(TGEV) 、犬冠状病毒( CCoV)和猫传染性支气管炎病毒( FCoV) ;第2 群包括人冠状病毒OC43( HCoV-OC43) 、牛冠状病毒(BCoV) 、火鸡冠状病毒(TCoV) 、鼠肝炎病毒(MHV)、猪血凝性脑脊髓炎病毒( HEV) 和大鼠冠状病毒( RtCoV) ;第3 群包括禽传染性支气管炎病毒( IBV) 和火鸡蓝冠病病毒( TCoV)。非典型肺炎SARS-CoV 病毒基因组与已有的冠状病毒的基因序列同源性都不高,所以被认为是第4 群冠状病毒。
冠状病毒形态结构
冠状病毒为多形态,略呈球形,直径80-160nm。有囊膜,表面覆有长12-24nm 的纤突,纤突末端呈球状,规则地在囊膜表面排列成皇冠状,故得名冠状病毒。病毒粒子囊膜由双层脂质组成,在脂质双层中穿插有两种蛋白:膜蛋白(M)和纤突蛋白(S)。部分冠状病毒,如BCoV、HEV、HCoVOC43和TCoV 的囊膜上还有第三种蛋白,即血凝素糖蛋白(E)。病毒粒子内部由RNA 和核衣壳蛋白(N)组成,呈螺旋式结构,直径9-16nm。
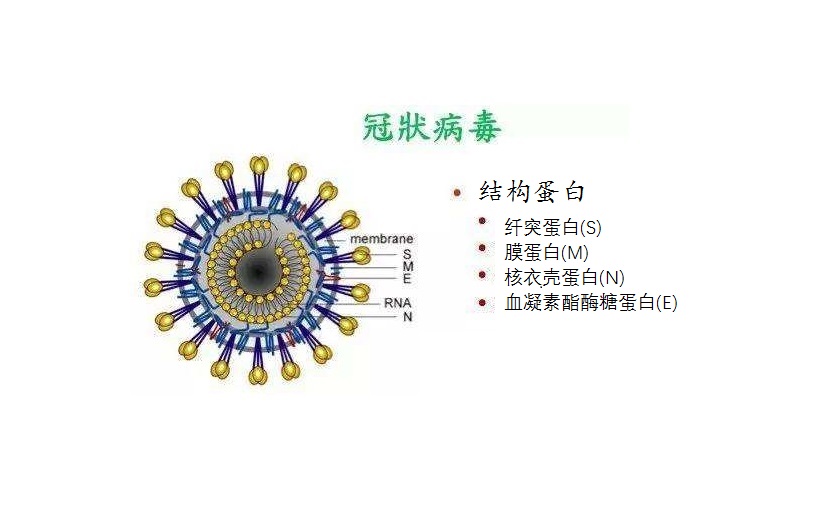
冠状病毒结构示意图
冠状病毒的基因组为单链正股RNA,是目前已知RNA 病毒中最长的。具有mRNA 的功能和感染性,导入真核细胞后能引起感染。
纤突蛋白(S)是伸出囊膜20 nm 的球- 杆形的病毒融合性糖蛋白,是冠状病毒感染细胞的关键蛋白,携带主要的B 淋巴细胞抗原决定簇,是惟一能诱导产生中和抗体和提供免疫保护作用的结构蛋白;含有宿主细胞受体识别位点,在决定宿主细胞亲嗜性方面起关键作用;决定病毒的致病性;具有细胞膜融合作用,使病毒核蛋白进入细胞质。
膜蛋白( M)是病毒跨膜蛋白,大部分位于囊膜内,仅有氨基端糖基化的小部分暴露在囊膜外面。M 蛋白是负责病毒颗粒组装的主要蛋白质,与病毒囊膜形成与出芽有关。M 蛋白同N 蛋白的C 端结合,介导核衣壳装配入病毒体。
核衣壳蛋白(N)是核蛋白,N 蛋白能与病毒RNA 紧密结合,通过螺旋堆积将RNA 封装,从而保护病毒的基因组RNA, IBV 和MHV N 蛋白都可以同核仁中的核仁纤维蛋白和核仁素相互作用,导致细胞生长延迟,使细胞更长时间的停留在分裂间期,此时病毒RNA 可以最大程度的翻译。
血凝素酯酶糖蛋白( E )第二群冠状病毒,如BCV、HEV、HCV、OC43和MHV - DVIM 等存在,分子量120~140 kD ,目前认为HE 蛋白可能与病毒吸附有关,能引起红细胞凝集,且是有乙酰酯酶活性,HE 蛋白目前研究的不多,但其对病毒粒子的形成起着相当重要的作用[8]。其氨基酸序列与丙型流感病毒的HE 蛋白同源,推测是基因组同丙型流感病毒重组而获得的
分离与鉴定
冠状病毒能在多种细胞上增殖,各种冠状病毒适应细胞种类如下:鸡传染性支气管炎病毒适应鸡胚、幼鸡气管环器官培养、原代雏鸡肾细胞;犬冠状病毒适应原代犬肾细胞;猫冠状病毒适应原代幼猫腹膜细胞;猪传染性胃肠炎病毒和猪血凝性脑脊髓炎病毒适应原代猪肾细胞、脾细胞、甲状腺细胞和*丸睾**细胞;猪流行性腹泻病毒适应胎猪肠细胞;犊牛腹泻病毒适应恒河猴肾细胞、胎牛肾细胞;小鼠肝炎病毒适应鼠巨噬细胞、鼠DBT 细胞、鼠17CL-1 细胞、人冠状病毒适应继代人胚肾细胞、WI-38 细胞、HeLa 细胞、有胚气管环器官培养、L132 细胞、人胚肺细胞。
鉴定病毒的最常用方法是病毒中和实验,用已知的特异性抗血清对分离病毒进行中和后,在细胞或组织培养物上进行培养,根据是否出现病变判定是否有中和反应从而对病毒做出鉴定。现在较常用分子基因技术,比病毒分离及中和方法可更快速、灵敏,并且准确做出诊断鉴定,例如,采用RT-PCR和实时荧光RT-PCR 技术直接对病料样品、试子或病毒培养物进行病毒特异基因片段扩增,再进行序列测定比对,从而鉴定病毒。
血清学检测技术包括间接免疫荧光试验(IFA)和酶联免疫分析法(ELISA)、血凝试验和间接血凝实验等,通过检测抗体的有无以确定是否有病毒感染。在病毒的不同感染期应采取不同的检测方法,例如,有报道指出,在SARS 病毒感染后出现发烧症状的前10 天内使用RT - PCR 技术便可检测病人是否感染病毒,但在发病后期使用RT - PCR 技术往往会出现假阴性结果,此时血清学检测技术结果更准确。
冠状病毒感染
冠状病毒的宿主范围与病毒特异的细胞受体直接相关,病毒粒子经受体介导吸附于敏感细胞的细胞膜上,通过HE 或S 蛋白结合于细胞膜上的糖蛋白受体,吸附在敏感细胞膜上的病毒粒子通过膜融合或胞吞作用侵入细胞。病毒经口、鼻感染后,对淋巴细胞、网状内皮细胞、上皮细胞和实质细胞呈现杀细胞作用,从而损害多种器官。冠状病毒急性感染后,还可能发生持续性感染,病毒在细胞与细胞之间慢性传播,引起细胞死亡和器官病理变化。这种现象已在小鼠肝炎病等得到证实。其他冠状病毒,如鸡传染性支气管炎病毒、人冠状病毒也可能发生持续性感染。
就目前所知,冠状病毒只感染脊椎动物,具有胃肠道、呼吸道和神经系统嗜性,分别引起相应症候群。人冠状病毒是引起人类普通感冒和咽炎的病毒之一,感染患者都表现急性上呼吸道感染症状,如鼻炎、鼻塞、喷嚏和咽炎等;严重急性呼吸系统综合症SARS 病毒和中东新型冠状病毒则在肺部引起严重症状;虽然冠状病毒本身有许多独特之处,但其所引起的临床症状,则与由鼻病毒引起的普通感冒或由流感病毒引起的流行性感冒极其相似。冠状病毒亦引起许多动物的疾病,如:鸡传染性支气管炎、猪传染性胃肠炎病、犬冠状病毒病、猫肠道冠状病毒病、猫传染性腹膜炎病、兔冠状病毒病、小鼠肝炎病、大鼠诞泪腺炎病、猪凝血性脑脊髓炎病、牛冠状病毒病、兔肠道冠状病毒病和火鸡兰冠病等
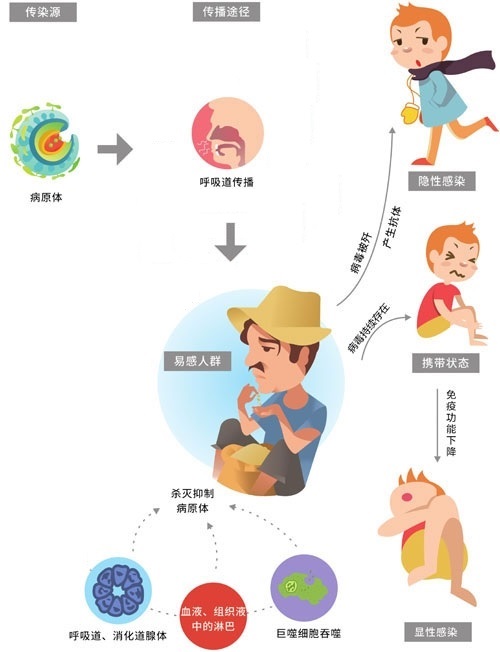
冠状病毒防治
冠状病毒没有特效的药物治疗方法,采用针对病毒的特异性抗体可有效治疗。一些*制剂抑**和蛋白酶制剂,能够减轻或阻断自身免疫损伤。免疫预防和消毒是防治冠状病毒感染传播的有效手段。冠状病毒与流感等呼吸系统感染病毒的传播途径相似,经口液、喷嚏、接触传染,并通过空气飞沫传播,感染高峰在秋冬和早春。病毒对热敏感,紫外线、来苏水、过氧乙酸及等都可在短时间内将病毒杀死。大部分冠状病毒应用1% 的煤酚、1/10000 高锰酸钾、70% 酒精和1% 福尔马林均可在室温条件下几分钟内杀死。
针对新疾病,并无现有可用疫苗。而且开发一种疫苗可能需要若干年时间。目前疫苗可分为四类,即灭活疫苗、弱毒活疫苗、DNA 疫苗和基因工程疫苗。由于冠状病的高变异特点,直接采用流行株或已证明能够完全保护流行株的致弱毒株制备的灭活疫苗免疫效果最好,但疫苗的制备过程可能存在散毒的风险。在实际免疫中,应注意根据毒株流行情况选用合适的疫苗。
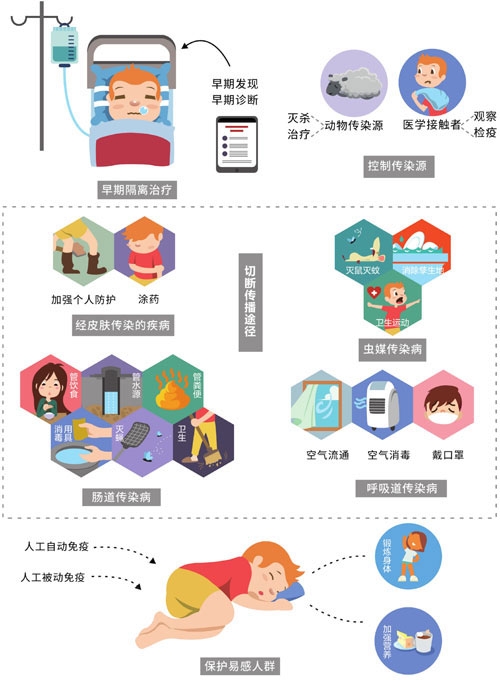
SARS流行特征及病毒特性
传染性非典型肺炎,也称为“重症急性呼吸综合征”(SARS),是一种由SARS冠状病毒引起的急性呼吸道传染病。自SARS流行至今,全世界共有26个国家和地区报告临床病例8098例,其中死亡774例,死亡率约10%。中国内地总发病人数5327例,其中死亡349例,死亡率为6.6%。
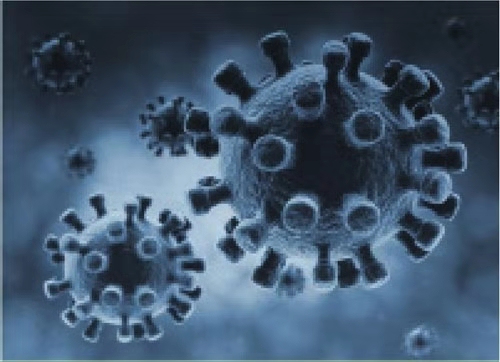
SARS病毒是一种冠状病毒的一个变体,直径60~220纳米,透过电子显微镜,可观察到病毒外膜有明显的棒状粒子突起,有点像“自由女神头顶的帽子”,因此命名为冠状病毒。该病毒在空气中能存活4~5小时,在干燥塑料表面最长可活4天,尿液中至少1天,腹泻病人粪便中至少4天以上。当暴露于常用的消毒剂或固定剂后即失去感染性,对热十分敏感,紫外线、来苏儿和0.1%过氧乙酸等都能将病毒杀死。
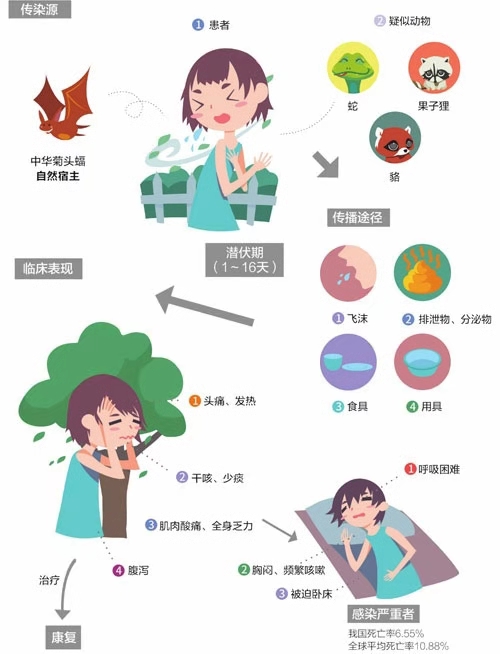
MERS流行特征及病毒特性
中东呼吸综合征(MERS)是由一种新型冠状病毒引起的急性呼吸道传染病。该病最早于2012年出现在中东国家,2013年传入法国,2014年传入菲律宾和马来西亚,2015年5月传入韩国,并由一名韩国籍病人传入我国。韩国MERS疫情不仅未得到控制,反而呈迅速蔓延之势。首尔民众为防止感染MERS,戴口罩出行。截至2015年6月10日,全球共有25个国家累计报告MERS实验室确诊病例1231例,其中死亡451例,病死率36.6%
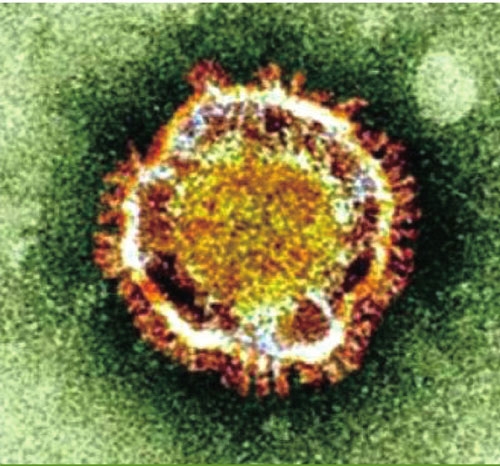
MERS病毒属于冠状病毒科,具有包膜,病毒粒子呈球形,直径为120~160纳米。病毒对理化因子的耐受性较差,56℃10分钟、37℃数小时可使其灭活。对脂溶剂敏感,如*醚乙**、乙醇(70%)、甲醛及紫外线等均可灭活病毒。
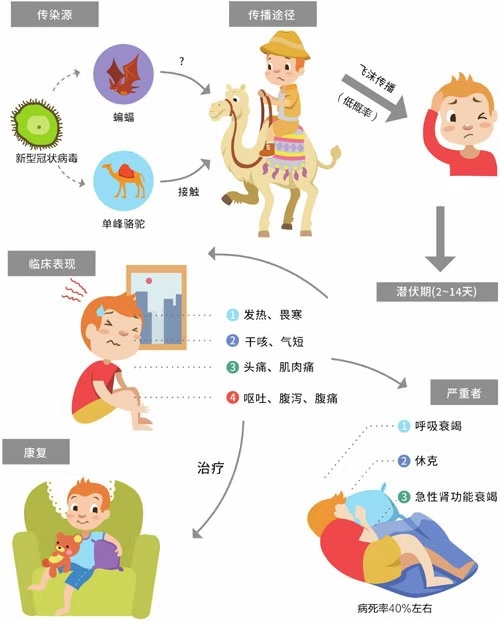
目前新型冠状病毒的宿主、感染源、人体感染途径等问题都未彻底了解清楚。在长时间近距离接触的情况下,这种病毒很可能通过空气和唾液传播。但从疫情持续时间和病例总数来看,新型冠状病毒的传播能力远不及SARS。这种新型冠状病毒目前尚无特异性治疗措施,也没有预防这种病毒的疫苗和特效疗法。有效预防措施是通风、消毒、远离高风险区域和人群,并及早诊断和治疗,由医疗机构对患者进行对症治疗,并借助体外循环技术,对呼吸功能不全的重症患者给予辅助性呼吸循环治疗。