什么是慢性血栓栓塞性肺高血压
慢性血栓栓塞性肺高血压(chronic thromboembolic pulmonary hypertension,CTEPH)是因肺动脉血栓栓塞、血栓机化引起肺动脉狭窄或者闭塞,同时诱发肺血管重构,导致肺血管阻力进行性升高、肺高血压及右心功能不全的一组临床综合征,属于第4大类肺高血压(pulmonary hypertension, PH),也是目前唯一有可能被治愈的一类肺高血压。
未经治疗的CTEPH患者生存率极低,平均肺动脉压(mPAP)>50mmHg的CTEPH患者的5年生存率不足10%,在目前的治疗模式下,患者的生存率已经明显改善。CTEPH治疗手段主要包括肺动脉内膜剥脱术(pulmonary endarterectomy, PEA)、靶向药物治疗以及球囊肺动脉成形术(Balloon pulmonary angioplasty, BPA)。
肺动脉内膜剥脱术(PEA)
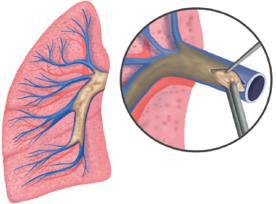
图1:肺动脉内膜剥脱术示意图
肺动脉内膜剥脱术(图1)可明显改善CTEPH患者的血流动力学参数、功能状态以及长期预后,也是指南推荐的首选治疗方案,而且是目前唯一可能治愈CTEPH的手段。
该手术通常需要进行双侧的栓塞肺动脉内膜切除以清除肺动脉内血栓栓塞样物质,恢复肺血管的血流动力学。要做到这一点,必须要进行深低温体外循环,这样才能保证肺动脉手术区没有血流,同时又能保护神经功能。
该手术操作复杂,手术的院内死亡率取决于手术医生的经验,且与该医院每年进行手术的数目呈反比。比如在欧洲,专业中心(>50例PEA/年)的院内病死率≤3.5%,操作手术相对较少的医院(11-50例PEA/年),病死率为4.7%,而在手术病例更少的医院(<11例PEA/年)病死率升高至7.4% [5]。因此,PEA手术应该在操作经验丰富的CTEPH专业中心进行,并且该中心应该有一支包含有经验的PEA手术医生,呼吸科,心血管科,影像科,核医学科,ICU等专科医生的团队。
所有CTEPH患者均应接受专业团队关于PEA手术可行性的评估。研究显示,约有40%的CTEPH患者因为各种原因无法进行PEA手术,如栓塞部位位于外周肺动脉、合并严重的并发症或者术者水平受限等,并且,约1/3的患者在手术后会出现残留或者持续的肺高血压。但在CHEST-1研究中,对于不能进行PEA的患者经第二家中心再次评估后,发现22%患者是可以接受手术治疗的,因此对于首次评估不能进行PEA的患者需要二次评估。
靶向药物治疗
对于不能接受PEA手术治疗或者不能接受PEA手术风险,以及PEA术后PH复发或持续存在PH的CTEPH患者,靶向药物治疗是一种选择。
CTEPH的非堵塞区域的肺小动脉类似PAH的病理变化是靶向药物治疗的病理基础。临床实践中,有手术指征的CTEPH患者靶向药物使用逐年增加。对于有PEA手术指征且存在严重的血流动力学障碍的患者,术前是否需要给予靶向药物治疗目前还缺乏证据。
一项RCT研究和一项回顾性分析发现,PEA术前给予靶向药物治疗对于术后各项结果的改善影响很小,但却显著延缓患者接受手术的时间。目前,还需要进行一些前瞻性的RCT研究来识别哪些患者可以从PEA术前靶向药物治疗中获益。
可溶性鸟苷酸环化酶激动剂(sGCS)
sGCS是第一个被FDA批准用于治疗CTEPH的靶向药物,也是国内目前唯一一种被批准用于治疗无法进行PEA手术或PEA术后持续存在肺高血压的CTEPH的靶向药物。
CHEST-1研究和CHEST-2研究证实CTEPH患者接受sGCS治疗后,运动功能以及血流动力学明显改善,并且耐受性良好。因此,2015 ESC指南推荐推荐对于手术后症状持续/复发的CTEPH患者,或经包括至少一位有经验的PEA手术医生的CTEPH专家团队判断不能手术的CTEPH患者,可接受sGCS治疗(I,B)。
MERIT-1研究为一项随机对照研究,探索了内皮素受体拮抗剂(ERA)马昔腾坦在无法PEA手术的CTEPH患者中的有效性和安全性。研究结果显示治疗4个月时的患者肺血管阻力(PVR)明显降低。一项2008年的小型非对照的研究显示,5型磷酸二酯酶*制剂抑**(PDE5-i) 西地那非治疗12个月后改善了CTEPH患者的运动功能。
球囊肺动脉成形术(BPA)
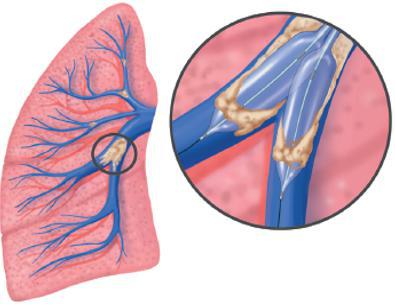
图2:球囊肺动脉成形术示意图
对于不能进行PEA手术的CTEPH患者,球囊肺动脉成形术(图2)也是一种治疗选择。
BPA是在低灌注的肺动脉内通过球囊扩张,重建有效的血流量,从而减少通气-灌注不匹配以及右心室的后负荷。BPA每次在一个肺叶或者最多两个肺叶进行,通过使用比目标血管直径小的球囊持续扩张以最大程度地避免出现血管损伤。
2001年首次报告BPA应用于CTEPH患者(18例)的疗效和安全性,可显著改善血流动力学指标,但并发症很高,且围手术期的死亡率高达10%,致使该技术在近10年时间内并没有得到发展和推广。随着手术方式的改良,技术进步和器械的发展,目前BPA手术的安全性已经大大改善,手术效果良好(图3),近期的报告显示围手术期的并发症已经大幅降低至0%-1%。
BPA后再狭窄和再阻塞是非常少见的,并且肺动脉也不需要植入支架。BPA并发症主要为球囊和导丝引起的肺血管损伤和以及再灌注肺水肿。BPA并发症的发生率除了与技术有关外,主要与选择治疗的病灶类型、治疗中心的既往经验和选择的患者有关。
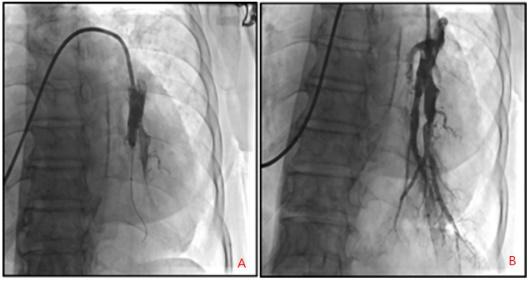
图3:A) BPA前:左肺下叶前、后基底段残根改变;
B) BPA后:血管通畅,远端血管显影
Kawakami等人提出了最有利于接受BPA治疗的病变分类(图4):相对于复杂病变(完全或次全闭塞病变,“扭曲”病变),“环状”病灶和“网状”病灶的治疗更简单也更有效,同时并发症更少(3% vs 5%)。
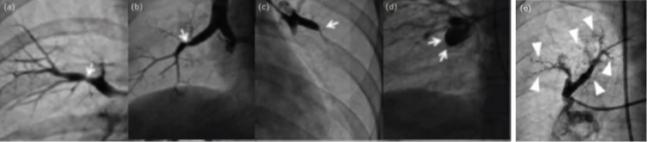
图4. BPA治疗病变分类:(a)环状病变;(b)网状病变;(c)次全闭塞病变;(d)完全闭塞病变;(e)扭曲病变
BPA术后短期和中期的血流动力学和临床功能改善显著。研究显示,接受BPA治疗的队列,短期和中期内血流动力学参数,WHO的心功能分级,6MWD和BNP改善明显,效果不劣于PEA手术和靶向药物治疗。临床经验显示部分患者甚至可以减少靶向药物,生活质量明显改善,在我国目前专业外科中心较少的情况下,是CTEPH患者的一个较好选择,但是目前有关BPA术后的长期的临床效果的研究数据比较少。
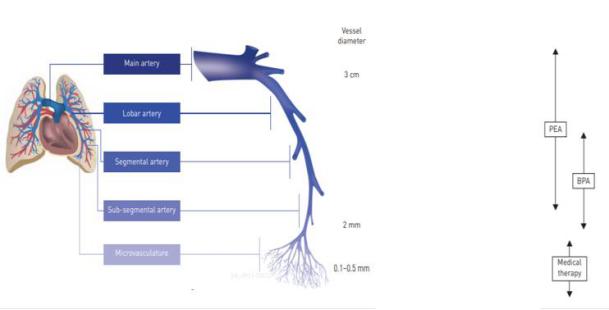
图5. CTEPH不同病变部位治疗选择
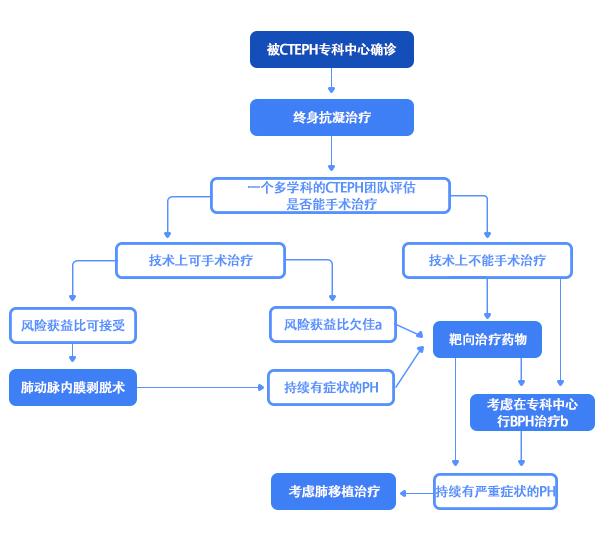
图6. 2015 ESC/ERS 指南:CTEPH 治疗策略
综上所述,CTEPH的治疗是一个综合评估和管理的过程(图5、6)。PEA是指南推荐的首选治疗方案,主要用于清除近端肺动脉主干(直径约3 cm以内)以及叶、段肺动脉中的血栓栓塞性病变。在专科中心,PEA可以清除段、亚段内的病变,甚至直径为2 mm的血管。当PEA不可行,或手术风险/获益比无法接受,或术后仍然存在PH或PH复发时,可选择靶向药物治疗,靶向药物主要作用于直径为0.1-0.5 mm的血管中的微血管病变,包括内膜增厚和纤维肌性增生。BPA是一种新兴的治疗手段,主要针对段和亚段水平肺动脉,直径2-5mm的肺小动脉病变,但该治疗需要多次手术,并且长期疗效需要进一步评估。当上述治疗手段都无效后,可考虑进行肺移植或心肺联合移植治疗。
#暖榜健康超能团#