
肾癌最常见的是肾透明细胞癌(RCC),肾透明细胞癌与黑色素瘤一样被认为是免疫原性肿瘤,对免疫治疗有较好的应答。例如,早期的细胞因子疗法IFN-α方案和高剂量IL-2方案,它们的抗肿瘤作用其实主要就是通过调控免疫相关细胞,上调自身免疫反应来达成。
随着肿瘤免疫逃逸机制研究地不断发展,多类免疫检查点*制剂抑**进入了临床试验当中,其中部分已获批可用于肿瘤的治疗。这些免疫检查点*制剂抑**能有效阻断肿瘤免疫逃逸,使患者自身的抗肿瘤免疫反应重新发挥作用,杀死肿瘤细胞。
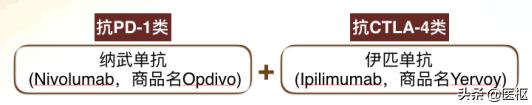
肾癌治疗中获批的免疫检查点*制剂抑**有:抗PD-1类的纳武单抗、派姆单抗(也称帕博利珠单抗)以及抗CTLA-4类的伊匹单抗。在本期内容里我们将为大家介绍,在晚期肾细胞癌患者的一线治疗中,上述免疫检查点*制剂抑**各自的治疗方案、获益人群特点以及对应方案的疗效与安全性。
- 免疫原性:指能引起免疫应答的性能,即抗原能刺激特定的免疫细胞,使免疫细胞活化、 增殖、分化,最终产生免疫效应物质抗体和致敏淋巴细胞的特性。
一、免疫检查点*制剂抑**的联合治疗方案
纳武单抗联合伊匹单抗是首个获批用于晚期肾癌的免疫治疗方案。这两类免疫检查点抑制
剂调控的免疫通路不同,但都能阻断免疫抑制信号,促进T细胞活化,发挥抗肿瘤作用。
代号CheckMate-214的III期临床试验在晚期肾透明细胞癌中,比较了纳武单抗联合伊匹单抗方案和标准一线方案舒尼替尼单药。参与试验的患者根据IMDC预后风险评估分为低危(预后评估较好)、中危(预后评估中等)和高危(预后评估较差)三类。
在中高危患者中,纳武单抗联合伊匹单抗治疗相较舒尼替尼单药治疗,可使患者死亡风险降低37%,且治疗的生存获益不受肿瘤PD-L1表达水平上的影响。该免疫联合方案的客观缓解率为41.6%,较舒尼替尼提高了15%;治疗相关的严重不良反应发生率为49%,较舒尼替尼降低了17%。此外患者免疫联合治疗的生活质量也优于舒尼替尼。
但是在预后风险为低危(预后评估较好)的患者中,该联合治疗方案相较于舒尼替尼方案却未显示出疗效上的优势。
代号CheckMate-214的III期临床试验在晚期肾透明细胞癌中,比较了纳武单抗联合伊匹单抗方案和标准一线方案舒尼替尼单药。参与试验的患者根据IMDC预后风险评估分为低危(预后评估较好)、中危(预后评估中等)和高危(预后评估较差)三类。
在中高危患者中,纳武单抗联合伊匹单抗治疗相较舒尼替尼单药治疗,可使患者死亡风险降低37%,且治疗的生存获益不受肿瘤PD-L1表达水平上的影响。该免疫联合方案的客观缓解率为41.6%,较舒尼替尼提高了15%;治疗相关的严重不良反应发生率为49%,较舒尼替尼降低了17%。此外患者免疫联合治疗的生活质量也优于舒尼替尼。
但是在预后风险为低危(预后评估较好)的患者中,该联合治疗方案相较于舒尼替尼方案却未显示出疗效上的优势。
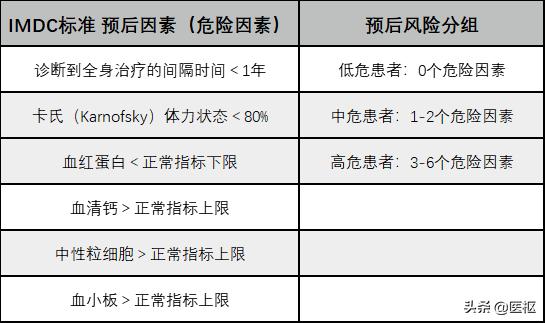
IMDC预后风险评估表
基于此试验的验证结果,纳武单抗联合伊匹单抗方案相继获FDA和欧盟的批准,投放使用于IMDC评分为中高危的晚期肾透明细胞癌(RCC)患者的一线治疗。但目前在中国,伊匹单抗尚未上市,纳武单抗也还未获批用于肾癌的治疗。
二、免疫检查点*制剂抑**联合靶向药物治疗
由上文可知,CheckMate-214的试验结果是令人鼓舞的,使人们对晚期肾癌的免疫治疗有了更多的期望。目前,除了多个免疫单药或联合用药的治疗方案进入了临床试验外,部分免疫检查点*制剂抑**和传统靶向药物的联合治疗也正在研究中。但是这两类抗肿瘤药物的作用机制与疗效特点均有差异,联合使用是否能在肾癌的治疗上获取理想效果,早前还属于未知数。直至2019年初,KEYNOTE-426以及JAVELIN Renal 101这2个大型临床III期试验相继报道的结果给出了肯定的答案,以下进行详细说明:
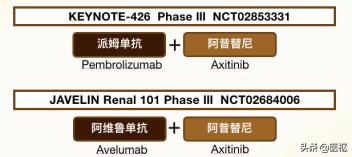
这两个大型试验均是在晚期或复发性肾透明细胞癌患者中开展的,试验组分别是派姆单抗联合阿昔替尼以及阿维鲁单抗(抗PD-1类免疫检查点*制剂抑**)联合阿昔替尼,对照组均是晚期肾癌一线标准疗法舒尼替尼单药方案。
疗效上,这两个联合治疗的客观缓解率均在50%-60%之间,比舒尼替尼单药方案高25%以上;联合治疗的患者肿瘤进展及死亡的风险较舒尼替尼方案降低了31%。两个试验的随访时间均不足以获得成熟的生存数据,但就目前的统计分析来看,派姆单抗联合阿昔替尼方案较舒尼替尼方案,可以显著地延长患者生存期。
安全性上,派姆单抗联合阿昔替尼较对照组发生严重不良反应的频率更高,阿维鲁单抗联合阿昔替尼与对照组相似。
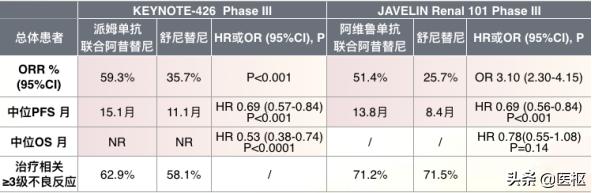
KEYNOTE-426、JAVELIN Renal 101试验结果表
- ORR:客观缓解率,是指肿瘤缩小达到一定量并且保持一定时间的病人的比例 (主要针对实体瘤 ),包含完全缓解 (CR) 部分缓解 (PR) 的病例 。
- 中位PFS:中位无疾病进展生存时间,表示一半的人从随机分组开始到第一次肿瘤进展或死亡时间。
- 中位OS:中位总生存时间,又称半数生存期,表示恰好有50%的个体尚存活的时间。
尽管这两个试验尚需更长的随访时间才能得到联合治疗的生存结果,并进一步观察和管理治疗中出现的不良反应。但目前分析表明这两个新的联合方案均较标准方案舒尼替尼显著提高疗效,派姆单抗联合阿昔替尼已获FDA和欧盟批准用于晚期肾癌一线治疗,而阿维鲁单抗联合阿昔替尼也有望成为新的一线治疗方案。
综上所述,对于肾癌患者而言,免疫治疗以及免疫联合靶向治疗的前景是广阔的。现阶段,众多的免疫单药、免疫联合免疫以及免疫联合靶向药物的方案已处于临床Ⅰ、Ⅱ期试验中,在最终的III期试验里,我们也期待有更多的方案能获得理想的结果。
从细胞因子方案到靶向药物方案,再到免疫检查点*制剂抑**及相关的联合方案,晚期肾癌的内科治疗一直都在不断发展前进。晚期肾癌一线治疗疗效的逐步提高以及不良反应管理手段的日渐成熟,将会为患者带来更多的希望。
参考文献:
[1] Parton M, Gore M, Eisen T. Role of cytokine therapy in 2006 and beyond for metastatic renal cell cancer[J]. Journal of clinical oncology, 2006, 24(35): 5584-5592.
[2] Motzer R J, Tannir N M, McDermott D F, et al. Nivolumab plus ipilimumab versus sunitinib in advanced renal-cell carcinoma[J]. New England Journal of Medicine, 2018, 378(14): 1277-1290.
[3] National Comprehensive Cancer Network. Kidney Cancer. NCCN Clinical Practice Guidelines in Oncology[J].
[4] Rini B I, Plimack E R, Stus V, et al. Pembrolizumab plus axitinib versus sunitinib for advanced renal-cell carcinoma[J]. New England Journal of Medicine, 2019, 380(12): 1116-1127.
[5] Motzer R J, Penkov K, Haanen J, et al. Avelumab plus axitinib versus sunitinib for advanced renal-cell carcinoma[J]. New England Journal of Medicine, 2019, 380(12): 1103-1115.