非酒精性脂肪性肝病(NAFLD)是指除了感染或大量饮酒以外的诱因造成的肝脏脂肪过多累积,如肝脂肪累积5%以上或组织学上就会发生脂肪变性。
因为现代社会的现代化和发展速度过快,所带来的生活习惯的变化,非酒精性脂肪性肝与以前相比越来越多。
虽然大多数的非酒精性脂肪性肝病人只有脂肪变性,但是非酒精性脂肪性肝有可能发展为非酒精性脂肪性肝炎(NASH)、肝纤维化、肝硬化、或肝功能衰竭等病变。
随着非酒精性脂肪性肝的增多,非酒精性脂肪性肝的并发症,也与以前相比增多的趋势,其威胁着全球人民的健康和对社会经济来带多种严重的负担。
病因及相关因素
(1)性别与年龄
有研究发现,非酒精性脂肪性肝发病的平均年龄为50~55岁,而此研究通过调查表明出,在巴基斯坦、南亚地区的平均发病年龄在45岁左右,印度在38岁左右,都比西方国家的年龄低,表明存在着年轻化的趋势。
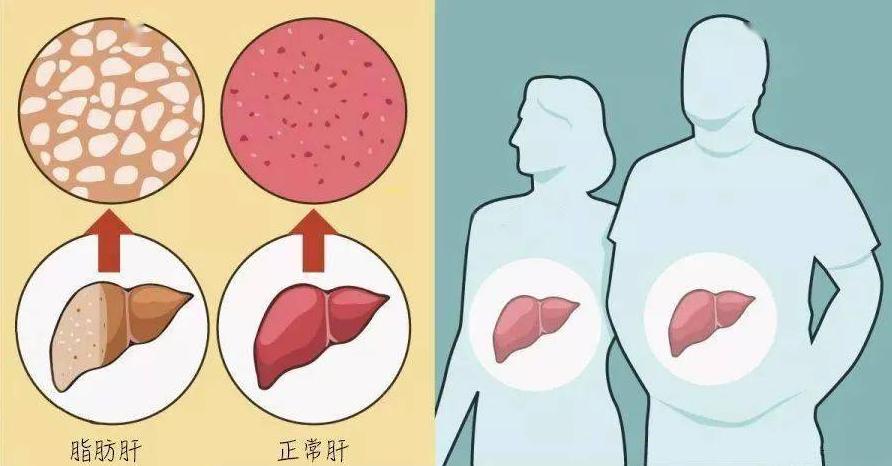
在马来西亚通过一个研究发现,男性的患病率与女性的患病率分别为35.3%、16.3%,男性的患病率明显高于女性。
此研究还发现,南亚地区及西方男女患病率也不同,男性的患病率明显高于女性。
而女性的患病率达到50岁之后,慢慢接近于男性的患病率,甚至可以比男性的患病率高,有学者说此可能性,可能与女性绝经后的激素分泌减少有密切的关系。
(2)肥胖
通过很多研究己发现,肥胖人群与患非酒精性脂肪性肝有很密切的关系。
在三个不同的人群,普通人群、肥胖人群、病态性的肥胖人群,非酒精性脂肪性肝的患病率分别为25%、70%、85%。

2018年在澳大利亚进行了全国性的调查,结果如下:18岁以上的澳大利亚成人当中66.9%属于肥胖或超重,和1995年56.2%相比的话肥胖和超重大量增多。
通过一个进行西方国家的肥胖率和超重率发现:新西兰达到30.7%,英国达27%,而美国达于38.2%,在西方国家为肥胖率最高的国家之一。
在孟加拉地区超重人群的非酒精性脂肪性肝患病率比正常人群高于4.51倍,而肥胖人群甚至达到10.71倍。
因为代谢综合症的最危险因素之一为内脏脂肪过多和肥胖,所以腰围可能成为一个重要的指标,但是腰围与BMI之间哪个与非酒精性脂肪性肝的关系更密切,还不明确,还在论争中。
(3)代谢综合症
由各种原因如肥胖、超重、血脂异常、血糖异常、血压升高等作用起来引起代谢综合征。

非酒精性脂肪性肝患者当中大约90%的患者至少有一种代谢综合征的表现,超过33%的患者有代谢综合征所有的特征。
空腹血糖和低密度脂蛋白是由肝脏生成,但是肥胖患者因为内脏脂肪过多,会引起胰岛素抵抗,而发展为高胰岛素血症,之后会导致肝脏VLDL生成和糖异生性的增加,最终会导致肝脂肪变性的过多。
研究表现,中度脂肪变性和重度脂肪变性会引起空腹血糖过度升高、HDL水平降低。
此外研究发现,在临床能经常遇到非酒精性脂肪性肝合并慢性乙肝患者有胰岛素抵抗,此类患者可能发生的代谢危险的增加,与胰岛素抵抗有密切的关系。
(4)其他因素
除了上面所提到的以外,与非酒精性脂肪性肝密切相关的因素还有人类、环境、生活习惯(如饮食、睡眠、运动、工作等)以及家族史等。

在美国对742例慢性肝病患者进行了统计学及临床学方面特性的分析和研究,发现西班牙裔美国的整个人类当中非酒精性脂肪性肝发病率占28%为最多,非洲裔人的发病率只达于3%,表明不同的人类之间,也明显存在着非酒精性脂肪性肝发病的遗传性不同。
发病机制
(1)二次打击学说
二次打击学说由Day和James在1988年提出,在医学界广为认可,由于肥胖、高血脂等原因,甘油的过量生成聚集在肝脏内,因肝细胞内脂肪堆积而引起的肝脏发生的一系列炎症反应。
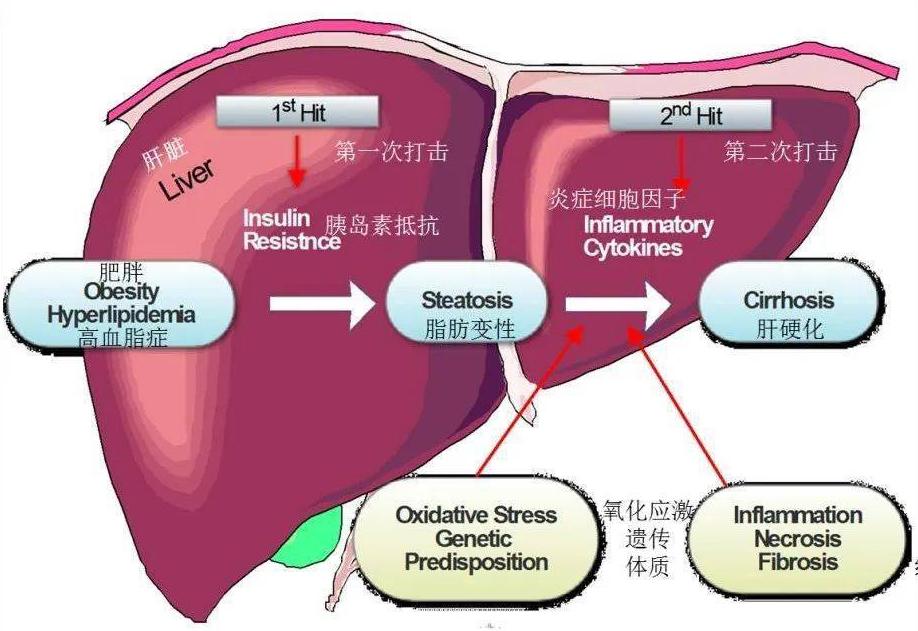
己表明出第一次打击有几个方面:首先超重肥胖和2型糖尿病等会引起胰岛素抵抗,而胰岛素抵抗再引起肝细胞内甘油积累的过多,因此肝脏的耐受力下降,并由此产生了第二次打击。
二次打击由于肝脏内脂肪过度累积,肝脏就会发生氧化应激反应和线粒体功能障碍,导致氧化代谢产物的增加,通过此过程会产生脂质过氧化物,因这些产物的生成就会导致信号通路传达的损伤或障碍,则发生内质网应激反应,再发生炎症因子的过多生成,最后肝细胞就会收到损害,因此会发生炎症坏死或纤维化等的炎症反应。
引起非酒精性脂肪性肝的因素复杂而多种多样,因此第二次打击学说不能完全解释非酒精性脂肪性肝,胰岛素抵抗、线粒体功能障碍、肠内菌群失调、遗传因素等这几个方面共同参与非酒精性脂肪性肝的发生和发展的多重打击学说被提出。
(2)胰岛素抵抗
胰岛素抵抗,因为很多不同的原因引起胰岛素摄取和利用葡萄糖的功能下降,血糖无法维持正常水平,机体能量供给导致脂质合成增加的同时脂肪酸分解抑制作用减弱,结果会导致甘油过多累积于肝脏内,其是非酒精性脂肪性肝发生的主要原因之一。
很多研究表明,非酒精性脂肪性肝与胰岛素抵抗之间的关系很密切,而会相互作用,对胰岛素抵抗引起作用的因素还会对非酒精性脂肪性肝引起一定的作用。
如有胰岛素抵抗,则摄取和利用葡萄糖的能力就会下降,因此机体就会分解脂肪代替能量提供给机体,就会增加脂肪酶的活性,增加脂肪组织甘油三酯的摄取能力,将脂肪储存在肝脏内,引起脂肪肝。
脂质物质积累过多,会加重胰岛素抵抗,它们之间也存在着相互影响、相互促进。
非酒精性脂肪性肝,也会降低脂联素的水平。
脂联素有几方面的作用,如葡萄糖和脂质代谢、抗炎、抗胰岛素抵抗调节等,脂联素是一种脂肪细胞释放的蛋白质。
通过研究可知,如有脂联素的降低,就会加重肝细胞脂肪变性。
Shah等人通过一个研究表明出铁超载和胰岛素抵抗也有密切的关系,铁超载会将胰岛素的敏感性降低,通过此过程就会引起胰岛素抵抗,和非酒精性脂肪性肝的发生有关系。
主要原因是铁可以激活NF-KB信号通道,NF-KB通道引起肝细胞炎症反应,加快非酒精性脂肪性肝形成。
人体有好几种微量元素必须有的,包括铁,但是通过最近几年的研究表明,虽然铁是一种必需的元素,但是过多就会发生铁超载,而铁超载与胰岛素抵抗和非酒精性脂肪性肝有直接的关系。
铁超载会产生活性氧气,引起氧化应激反应,另一方面铁超载会影响脂质代谢和胰岛素敏感性降低等,与非酒精性脂肪性肝的发生有关。
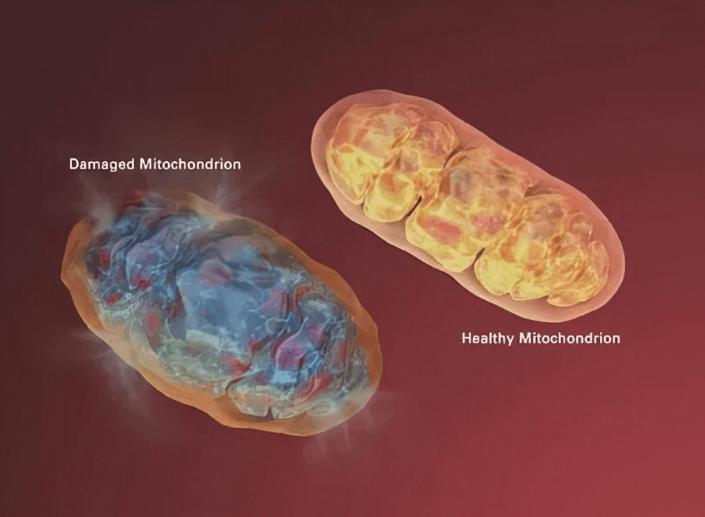
(3)线粒体功能障碍
线粒体能量失调,对非酒精性脂肪性肝的发生产生重要的影响。
非酒精性脂肪性肝患者因肝细胞内的游离脂肪酸过多,导致线粒体微细结构肿胀、线粒体功能失调,导致氧化损伤,改变内质视网膜的透射性,增加活性氧生成,减少ATP生成。
ROS是一种活性度较强的产物,包括氧自由基、氧自由基衍生物,ROS会诱发未折叠的蛋白反应。
UPR可以引导三种信号通道,分别通过IRE1、PERK、ATF6等三种信号通道,导致肝细胞内大量脂质聚集,并生成大量氧化应激反应及TNF-ci、IL-6、IL-8等炎症因子。
增加肝细胞的炎症反应,正常情况下,合成肝细胞的脂肪酸在内质网内首次生成磷脂后,再与载脂蛋白结合,变成极低密度脂蛋白(VLDL)并入血。
肝细胞发生炎症反应时,肝细胞受损而生成的甘油三酯不能释放到血液循环中,从而导致VLDL堆积在肝脏中,产生非酒精性脂肪性肝,导致肝细胞更加坏死。
活性氧的氧化能力较强,一般在生理状态下活性氧可以参与机体的正常代谢,但如果生成过多的过氧化物,就会破坏氧化和抗氧化作用的平衡水平,正常情况下,抗氧化物质会降低过氧化物的毒性,从而避免氧化应激反应损伤细胞,但由于氧化和抗氧化平衡水平的失调,导致抗氧化物质(如谷胱氨肽酶等)减少,引起氧化应激酶反应,大量多不饱和脂肪酸被活性氧等强氧化物质氧化,生成大量的脂质过氧化物,破坏线粒体的结构与功能,激活库普弗细胞,加重肝脏损伤,引发肝纤维化,进而引起肝细胞变性和坏死,导致线粒体微细结构肿胀,氧化受损,进一步加重线粒体的损伤,阻断呼吸链的传达,生成过多的ROS,下降抗氧化能力,肝细胞损伤更加严重,形成一个恶性的循环,加重肝细胞的凋亡,甚至引起肝硬化、肝细胞癌等更严重的后果。
另有研究表明,进食高果糖类食物被认为是引起非酒精性脂肪性肝和肥胖的高危因素之一,进食果糖后可加重脂质在肝细胞内合成增加,氧化受损,肝细胞的脂肪变性会更加严重。
主要是因果糖中含有五元呋喃环,不太稳定,会增加ROS的生成,破坏线粒体的功能,加重氧化反应。
(4)肠道菌群失调
肠道菌群是非酒精性脂肪性肝主要治病因素之一。
机制多与肥胖、炎症、IR等密切关。
有研究表明,在中国的一个队列中,61%的非酒精性脂肪性肝患者检测到生成大量酒精的肺炎克雷伯菌(HiAlc Kpn),用以研究HiAlc细菌与脂肪肝疾病之间的相关性,他们用HiAlc Kpn喂养了无特定的病原体的小鼠,注意的是喂养HiAlc Kpn可引发慢性肝脂肪变,Boursier和同事研究出肠道菌群不平衡与严重的非酒精性脂肪性肝病变的相关性,瘤胃球菌数量的增多与纤维化程度的加重为正相关。
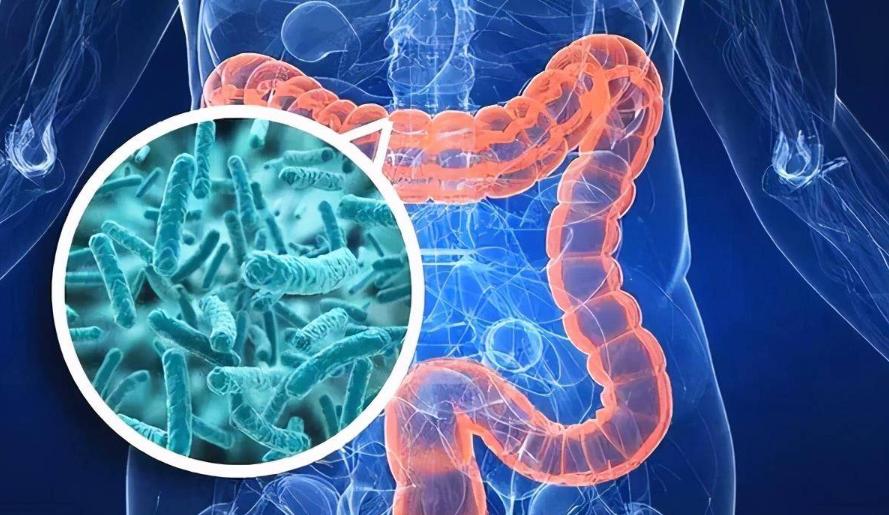
比较非酒精性脂肪性肝患者和健康人的肠道微生物组的一项研究中,相对于健康的非肥胖成人个体水平,非酒精性脂肪性肝患者的革关氏阴性细菌含量更多,拟杆菌含量提高了20%,厚壁菌降低24%。
前肠道菌群主要通过肠-肝轴的作用机制在非酒精性脂肪性肝中发挥作用,细胞壁外膜中的脂多糖通过TRL4作用于脂肪细胞和巨噬细胞,引导释放多种炎症细胞因子,引发IR,且肠道菌群结构和功能失调,改变相关基因表现,促进慢性低度炎症向IR发展,诱发非酒精性脂肪性肝。
肠道菌群的失调也可通过其他机制促进NASH,如乙醇生产和阻扰胆碱代谢。
整体上肠道菌群及其有害代谢物(乙醇、多胺、硫化氢、饱和脂肪酸、等)可能是肝损伤的驱动因素。