*仅供医学专业人士阅读参考
点击右上方“关注”, 准时接收每日精彩内容推送。
类风湿性关节炎 (RA) 通过引起关节炎症、肿胀和疼痛,并导致持续性滑膜炎和不可逆的关节破坏,严重威胁人类健康。在RA的发展过程中,促炎 M1 巨噬细胞表达高水平活性氧 (ROS) 和一氧化氮 (NO) 的诱导滑膜炎症和骨侵蚀。消除病变关节中的 ROS 和 NO 是一种潜在的 RA 方法,它可以驱动促炎 M1 巨噬细胞向抗炎 M2 表型转变。
近日来自 *京大南**学生命科学分析化学国家重点实验室的李喆教授团队 利用 DNA 分子固有的 ROS 和 NO 清除能力,设计了一种 叶酸修饰的三角形 DNA 折纸纳米结构 (FA-tDONs),FA-tDONs可以有效清除 ROS 和 NO 并主动靶向 M1 巨噬细胞,促进 M1 向 M2 转化并减轻炎症,并在RA小鼠模型中发现FA-tDONs 能有效减轻滑膜浸润和软骨损伤,减缓疾病进展 。这项研究证明了 DNA 折纸结构在 RA 治疗中的应用价值,并显示了了它在其他抗氧化疗法中的潜力。相关工作以题为“DNA Origami as a Nanomedicine for Targeted Rheumatoid Arthritis Therapy through Reactive Oxygen Species and Nitric Oxide Scavenging”于2022年8月2号发表在《ACS Nano》上。
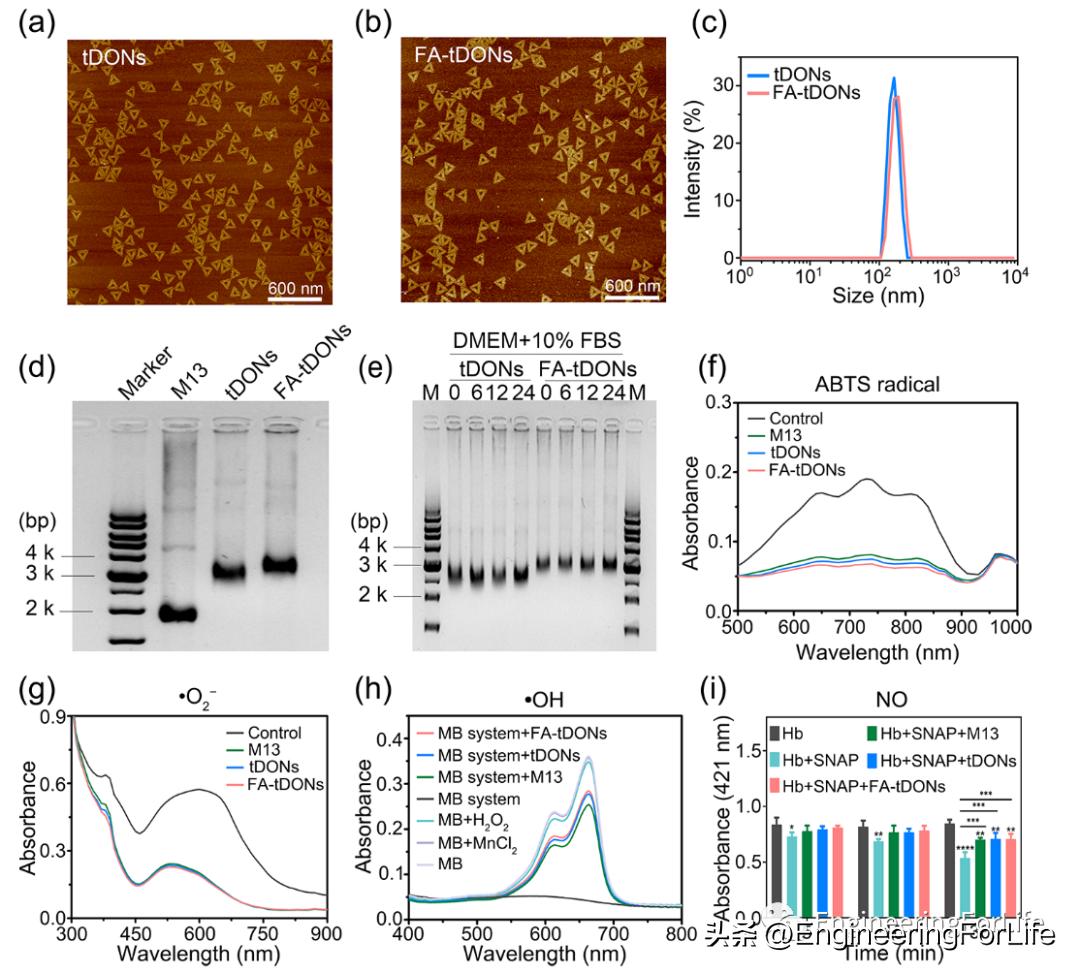
图1 tDONs 和 FA-tDONs 的表征
1. FA-tDONs 的制备和表征
首先,研究团队通过数百条短 DNA 链作为订书钉折叠 7249 个核苷酸的环状单链支架 DNA (M13),制备大小为120nm的三角形 DNA 折纸纳米结构 (tDON)。随后用叶酸 (FA) 修饰 tDON 以主动靶向病理环境中M1 巨噬细胞上过度表达的叶酸受体 β (FR-β)。原子力学显微镜观察 tDONs 和 FA-tDONs 的形态为边长为120 nm 的三角形,动态光散射 (DLS) 表明 tDON 和 FA-tDON 在大小上没有显着差异,并且凝胶电泳上显示tDON 的迁移速度略快于 FA-tDON,表明纳米结构的组装成功。随后研究团队验证了M13、tDON 和 FA-tDON具有良好的ROS及NO清除能力。
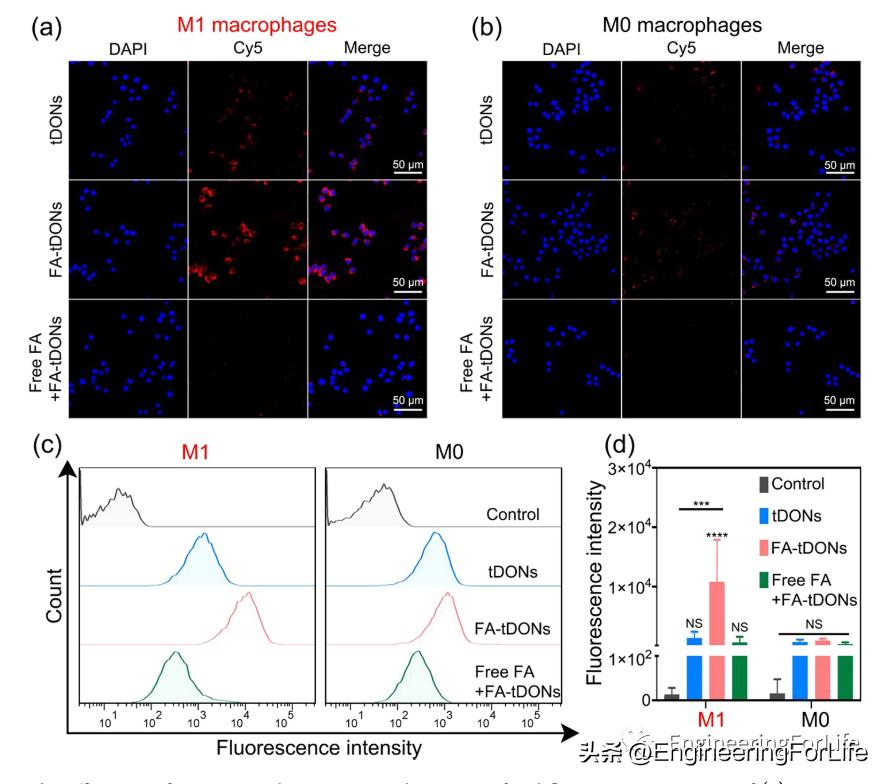
图2 M1 巨噬细胞对 FA-tDON 的细胞摄取效率
2. FA-tDONs 的细胞摄取和细胞内自由基清除能力
研究团队通过cy5标记FA-tDONs 和 tDONs,共聚焦图像显示,M0细胞不结合DNA纳米颗粒,而用 FA-tDON处理比用 tDON 处理的 M1 巨噬细胞表现出更高的荧光,并且可以被游离FA阻断。流式数据显示FA-tDONs的摄取比tDONs高4.4倍,这说明FA 修饰促进了DNA纳米结构的细胞内化,可以在体外主动靶向 M1 巨噬细胞。
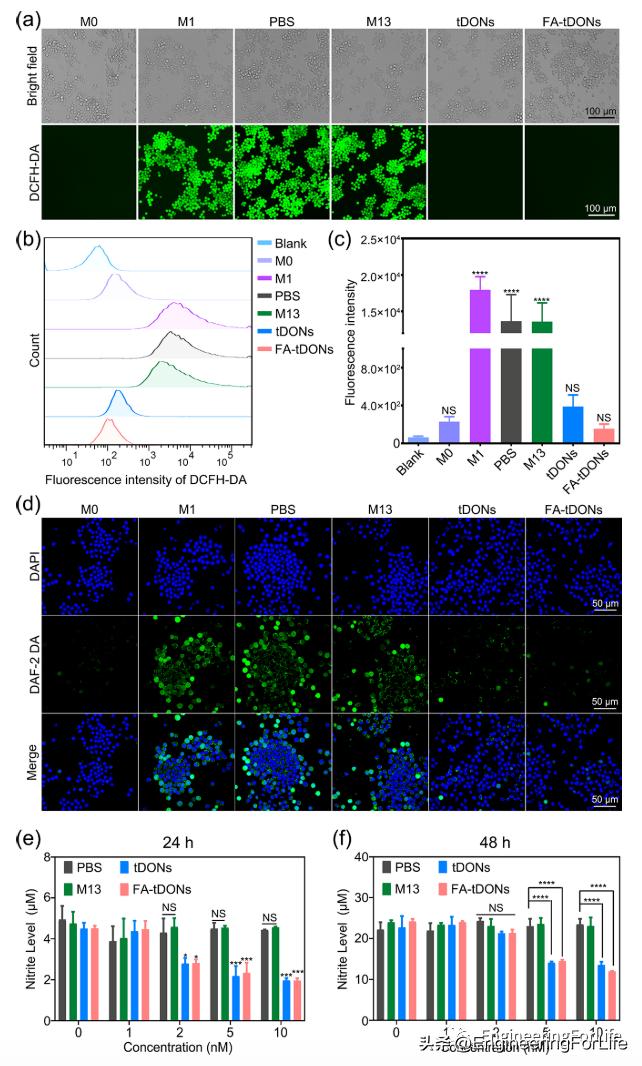
图3 FA-tDONs 在 M1 巨噬细胞中的 ROS 和内源性 NO 清除能力
研究团队通过ROS 探针发现tDON 和 FA-tDON 有效清除 M1 巨噬细胞中的细胞内 ROS 并使 DCFH-DA 的信号下降到M0 巨噬细胞水平,流式显示 tDON 和 FA-tDON 处理 24 小时后荧光分别降低了 40 倍和 80 倍。FAtDONs 更强的 ROS 清除能力可归因于更好的能被细摄取。同样,用 tDON 和 FATDON 处理后显着降低细胞内的DAF-2 DA信号,表明这两种纳米结构能有效清除NO。通过 Griess 测定法在细胞上清液中测量了 NO 的氧化产物亚硝酸盐。tDON 及FA-tDON在处理24小时后将亚硝酸盐浓度降低约50%,并持续48 小时。
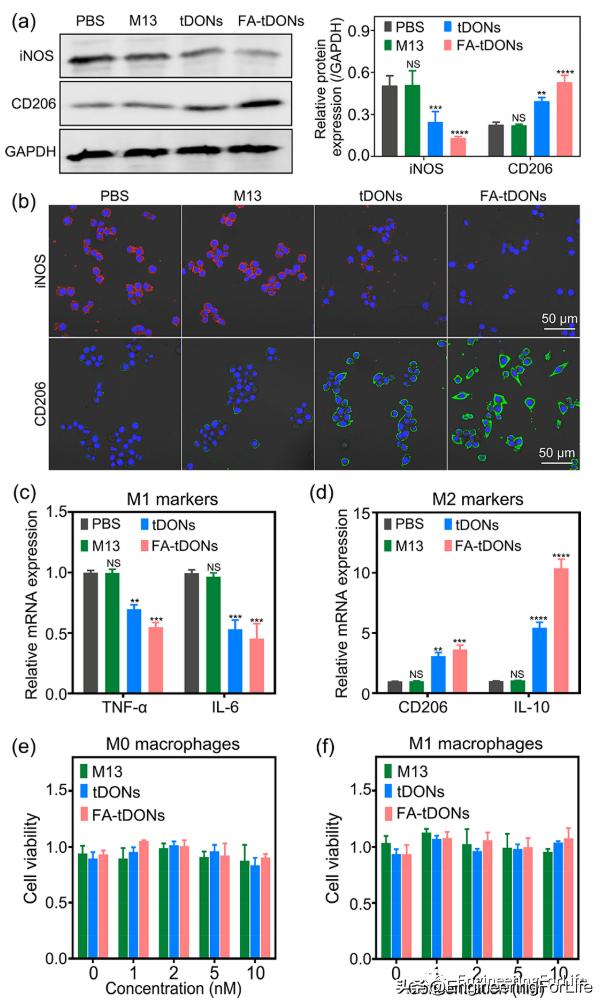
图4 不同 DNA 材料处理的巨噬细胞活力及表型转换能力
3. FA-tDONs 诱导的巨噬细胞的体外的表型转变
在确认 FA-tDONs 在 M1 巨噬细胞中有效的 ROS 和 NO 清除能力后,研究团队评估了它们是否可以诱导 M1 到 M2 表型转变。Western blot分析显示,tDONs 和 FA-tDONs 将 iNOS(代表性 M1 标记)的表达降低 52% 和 74%,同时将 CD206(代表性 M2 标记)的表达增加 ~1.8 和 ~2.8 倍。相反,由于细胞摄取效率低下,M13 处理组几乎没有观察到巨噬细胞极化。并且纳米材料的生物毒性可以忽略不计。
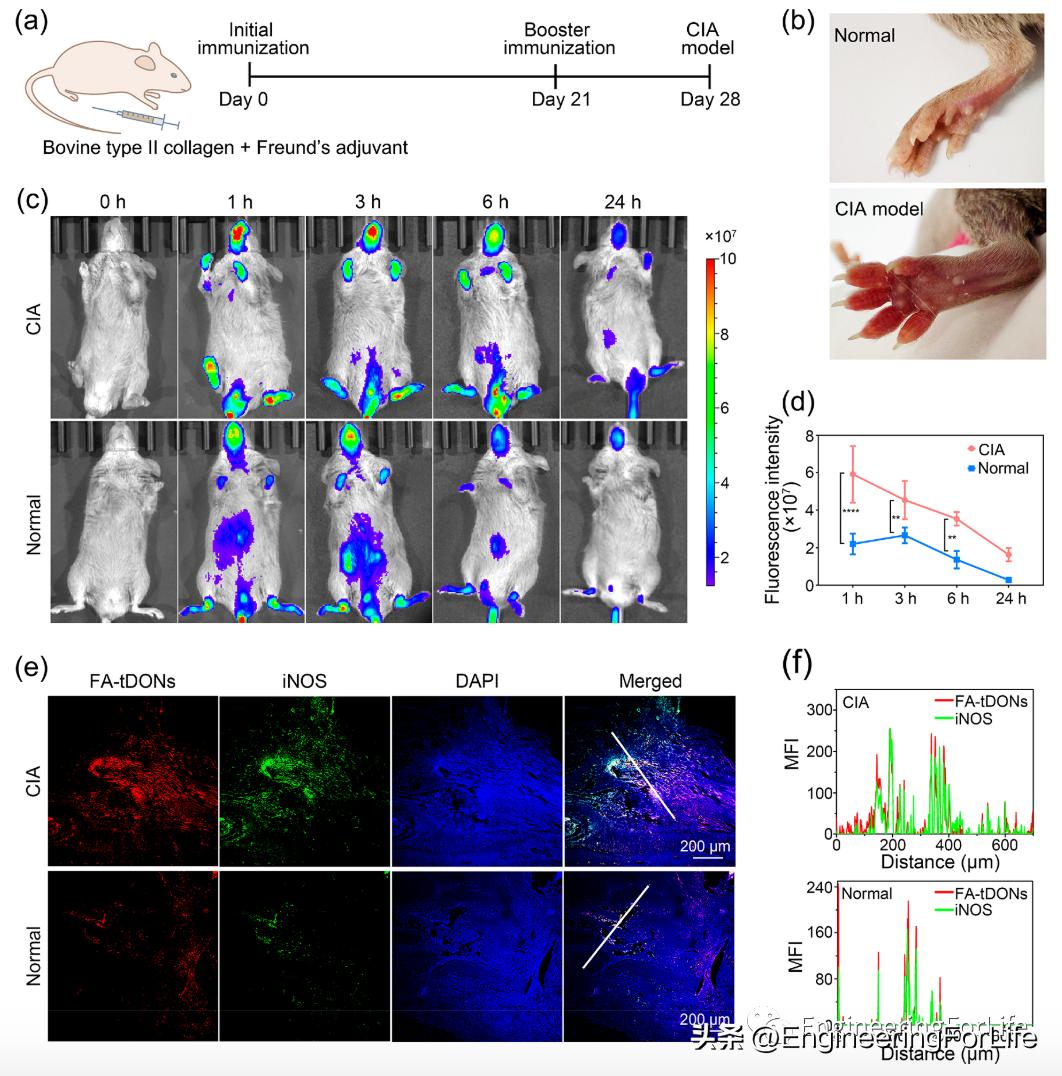
图5 FA-tDONs 的体内靶向效应
4. CIA 小鼠模型中 FA-tDON 的 RA靶向、体内分布及治疗效力
研究团队随即评估了DNA纳米颗粒在体内的治疗效果。FA-tDONs 用 Cy5.5标记并静脉注射到 CIA 和正常小鼠中。注射后 1 小时在 CIA 小鼠的病变关节中可以观察到荧光信号并持续 24 小时(图 5c)。相比之下,正常小鼠非炎症关节中的荧光信号在注射后 1 小时仅为 CIA 小鼠的三分之一,在 24 小时后几乎检测不到(图 5c,d)。通过注射cy5标记的FA-tDONs,CIA 小鼠的爪子中观察到更高水平的 iNOS 表达,此外,FAtDONs 和 iNOS 的荧光信号表现出相似的分布模式,表明 FA-tDONs 在体内主动靶向 M1 巨噬细胞。
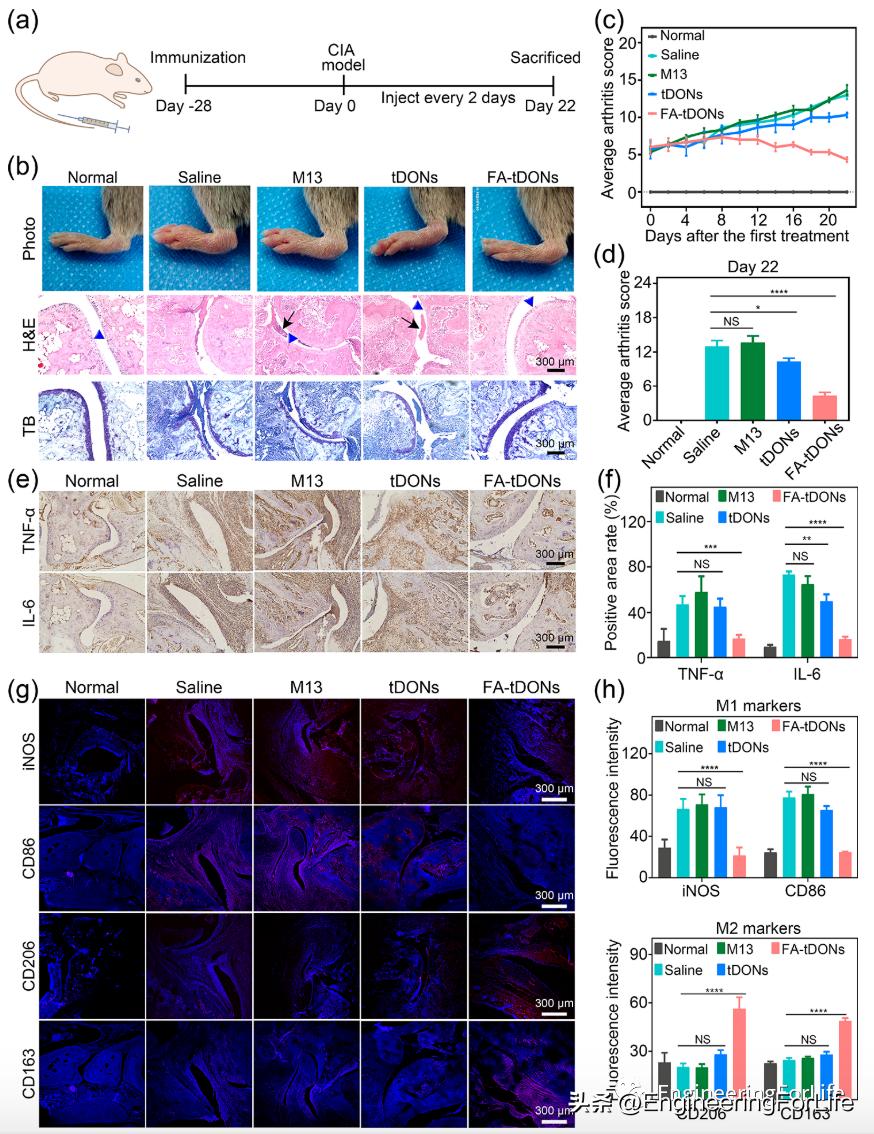
图6 FA-tDONs 通过促进巨噬细胞表型转化来缓解 RA
研究团队进一步通过组织学检查评估了关节的病变变化。苏木精和伊红 (H&E) 染色显示FA-tDONs 治疗组的关节面平滑,滑膜增生少。相比之下,其他三组关节腔滑膜增生和间质炎症细胞浸润明显。甲苯胺蓝 (TB) 染色的提示,FA-tDON 处理组的关节软骨保持完整,而在其他三组中观察到局部软骨破坏。还使用临床关节炎评分在整个治疗过程中评估 RA 的严重程度。FA-tDONs 治疗组的临床评分更低,临床预后更好。免疫荧光染色表明, FA-tDONs 治疗使 iNOS 和 CD86(M1 生物标志物)接近正常,伴随着 CD163 和 CD206(M2 生物标志物)的上调, TNF-α、IL-6表达明显下降。
综上所述,该研究探索了 DNA 纳米结构在 RA 治疗中的效用。表现出高效的细胞摄取和 ROS 和 NO 清除的能力,促进促炎巨噬细胞向抗炎表型的转变,并在 CIA 小鼠模型中验证了它们的靶向特异性、功效和生物安全性。该纳米药物还具有尺寸均匀、结构明确、易于合成和修饰等特点。 作者表示,既往研究主要利用 DNA 折纸纳米结构来用作药物输送的载体,但本项工作表明它们本身具有作为纳米药物治疗 RA 的潜力,而且通过改变靶向模块,DNA 折纸纳米结构有望成为治疗各种疾病的候选方法之一 。
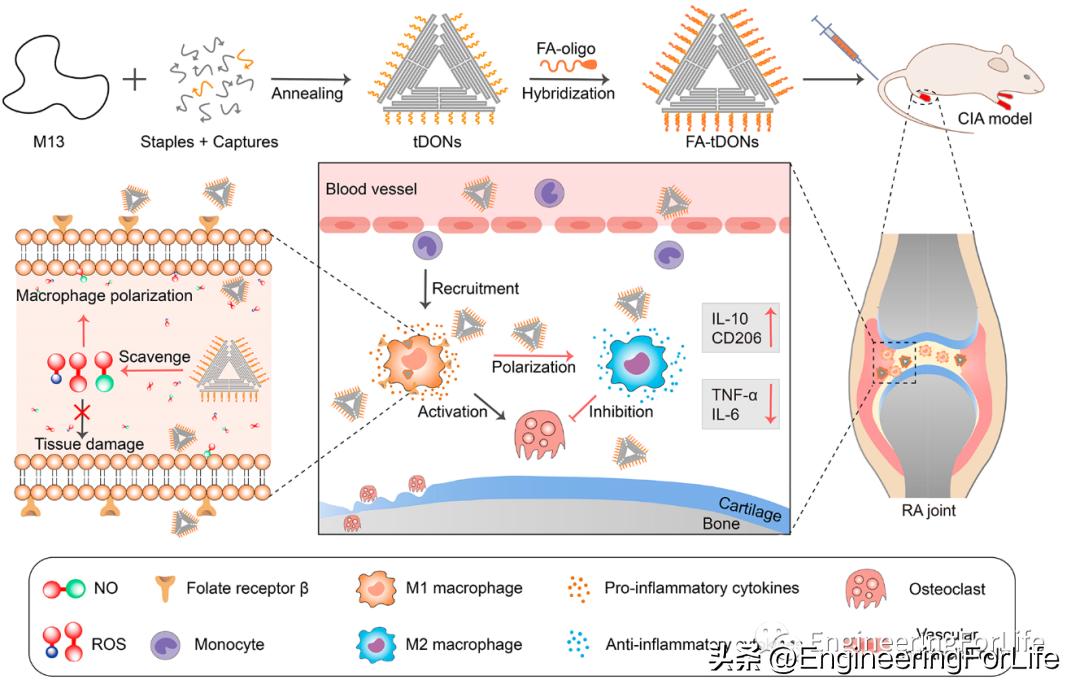
图7 FA-tDONs 纳米药物的设计和RA的治疗机制
了解更多
关注“EngineeringForLife”,了解更多前沿科研资讯~
