文/子非鱼(上海某肿瘤医院 医生)
虽然在过去的几年里,抗癌新药不断涌现,新型化疗药、分子靶向药、免疫检查点*制剂抑**,层出不穷。然而,具体到某一种特定的恶性肿瘤,能用的有效抗癌药,依然有限。对于晚期实体瘤而言,管用的抗癌药平均在四五类左右;病人的身体条件依然还不错,但是已经被证实有效的抗癌药已经穷尽的窘境,屡屡发生。
因此,一直以来,学术界都在研究一种被称为“再挑战”(rechallenge)的治疗策略:原来用过的、曾经起效过的药物,经过一段时间以后(这段时间内,病友大概率接受了其他方案的治疗),如果条件允许,可以尝试再次使用。
这样做的理论基础,其实也非常简单:一种治疗方案,曾经治疗有效,证明病人身体里肯定存在对该方案敏感的癌细胞;而持续使用一段时间后,敏感的癌细胞不断被杀灭,对该方案耐药的癌细胞不断繁殖、富集起来,大体上就会表现为肿瘤增大, 疾病耐药(但是,这个时候,几乎可以肯定的是,原来对该方案敏感的癌细胞并没有100%被消灭,只是比例明显下降,肿瘤组织中已经是耐药的癌细胞占了大多数,甚至是绝大多数)。接下来,病友换了另外一种治疗方案,或者单纯是随着时间流逝,对原方案耐药的癌细胞被杀灭或者比例逐步下降,对原方案敏感的癌细胞可能又会重新长起来,比例上也获得增长。这个时候,再一次使用原来的老方案,可能有机会再一次控制病情。病友们把这种情况称之为“复敏”,也就是恢复了对老方案的敏感性。
那么,上面这套理论假设以及抗癌策略,到底有没有临床数据支持呢,到底是不是管用呢?近期,几大权威期刊,给出了不少有趣的数据。
实证研究+数学模型:初步证实“复敏”理论
来自美国安德森癌症中心的Christine Parseghian教授,开展了一项有趣的实证研究,他们关注的是EGFR单抗(爱必妥、帕尼单抗等)治疗的肠癌患者。RAS、BRAF基因野生型的晚期肠癌患者,尤其是左半肠癌患者,EGFR单抗联合化疗,是世界各国推荐的首选治疗。治疗一段时间后,由于出现RAS突变、EGFR胞外段突变等原因,会出现对EGFR单抗的耐药。然而,RAS突变、EGFR胞外段突变的肠癌细胞,在EGFR单抗停止使用后,相比于RAS野生型、EGFR野生型的癌细胞,并没有生存优势;因此,理论预测,在EGFR单抗停止使用后,这些耐药的癌细胞的比例,应该会逐步下降。
Christine Parseghian教授首先选取了135例患者,对他们在EGFR单抗治疗前、耐药后各个时间段的外周血标本,进行了连续的基因分析,看看野生型和耐药型的癌细胞比例变化规律。果然如下图所示,在EGFR单抗治疗耐药后,医生们停止给患者使用EGFR单抗,患者外周血中耐药型癌细胞的比例,随着时间推移,是指数级下降的,其半衰期大约是4.4个月。随后,该研究小组利用另外73例独立的病例资料和外周血检测结果,验证了这个结果,在这个73例独立样本中,停止使用EGFR单抗后,耐药的癌细胞指数级下降,半衰期是4.3个月。
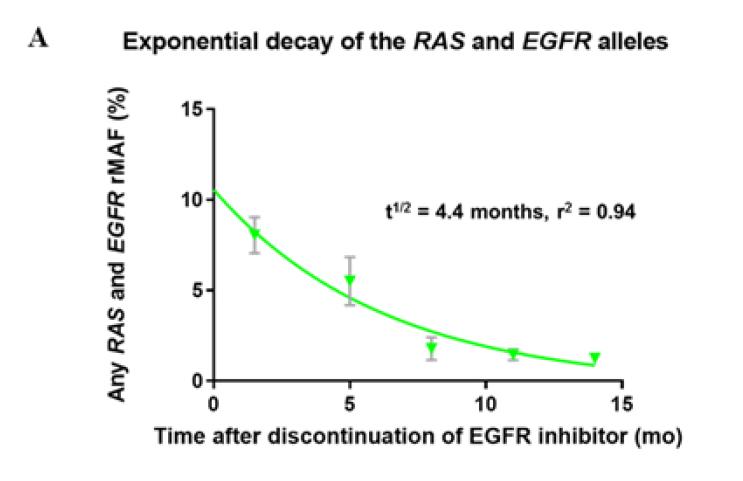
既然,EGFRA单抗停药后,耐药的癌细胞会指数级衰减,且半衰期是4-5个月左右。因此,间隔一段时间后,再次使用EGFR单抗,很可能会再次有效。因此,该研究团队又从另外一个地方,找来独立的80名接受了“再挑战”治疗的回顾性队列。这组病人,从EGFR单抗第一次使用耐药而停药,到再次使用,中间中位间隔的时间是5.1个月,差不多正好是耐药癌细胞衰减一半的时间,再次使用EGFR单抗后,客观有效率为23%——那些时间间隔超过2个半衰期的病友,再次使用EGFR单抗后,有效率为32%;而那些时间间隔短于1个半衰期的病友,再次使用EGFR单抗后,有效率只有16%。时间间隔越长,原来的耐药癌细胞衰减地越彻底,再次用药后有效率越高。
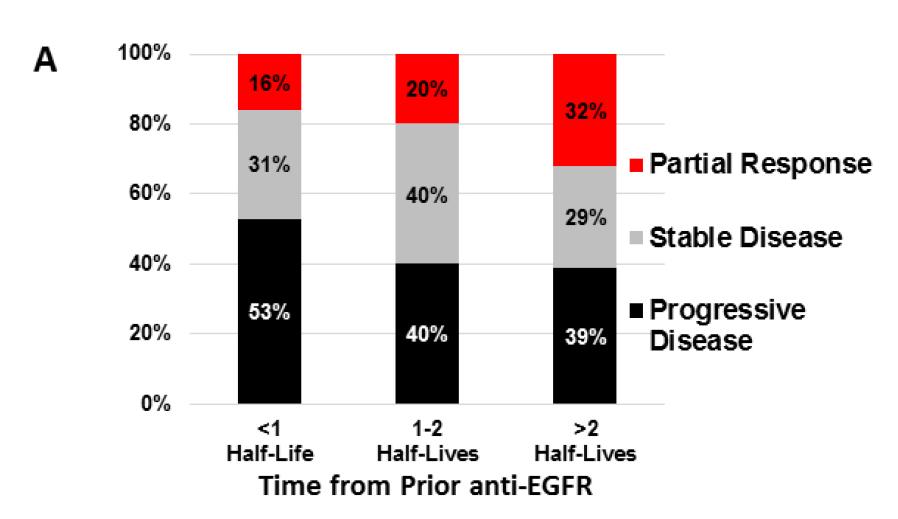
前瞻性临床试验:动态基因检测,助力成功“再挑战”
上面提到的是回顾性研究,不少病友认为说服力不强。接下来,笔者再介绍一个类似的前瞻性研究。来自意大利比萨大学的Alfredo Falcone从2015年1月到2017年6月,就开展了一项这样的二期临床试验。
他们纳入的是一线接受爱比妥+伊立替康治疗,治疗后肿瘤客观缓解,且无疾病进展生存时间大于6个月(满足这几个条件,说明病友一开始对这套方案,还是较为敏感的),二线接受了贝伐联合奥沙立铂治疗的晚期肠癌患者。这批患者二线治疗失败后,入组该前瞻性二期临床试验,三线给的方案是重新启用一线方案:爱必妥+伊立替康。
28名患者入组,结果显示:6名患者再次获得可观缓解,9名患者疾病稳定。再挑战治疗的有效率为21%,疾病控制率为54%。这样一个数字,在三线治疗的肠癌里,已经相当不错了。
除此之外,该研究小组还对入组的患者,进行了全面深入的外周血基因分析。他们发现,在接受爱必妥+伊立替康方案“再挑战”前夕,如果患者外周血中依然可以检测到RAS突变(意味着耐药的癌细胞,浓度相对还比较高),那么再挑战大概率会失败;反之,成功的概率就比较高。6位“再挑战”获得可观缓解的病友,在用药前夕的外周血中均已检测不到RAS突变;而在剩下的疗效没有那么好的病友里,57%的病友均检测到了RAS突变。
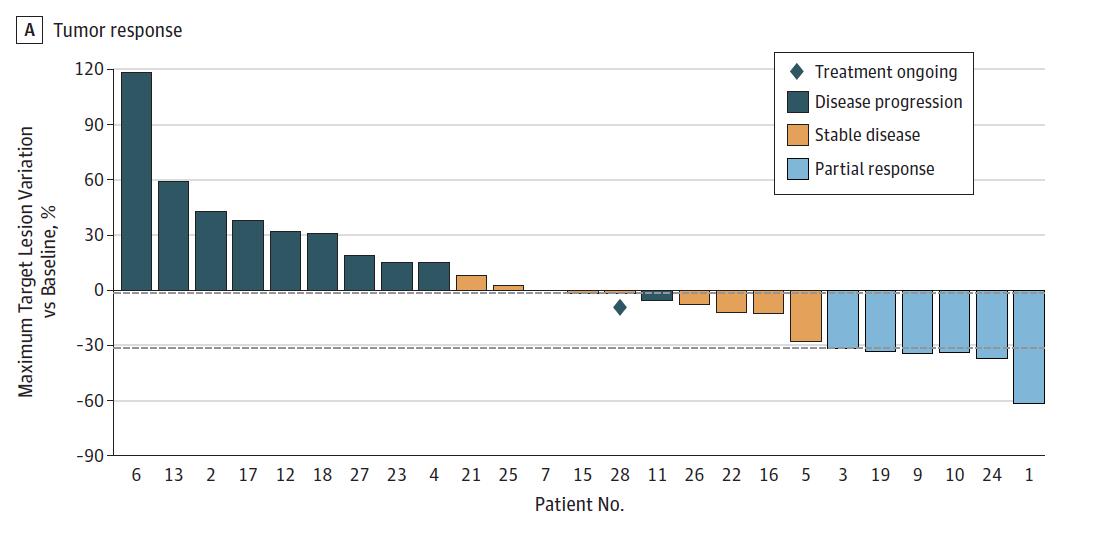
因此,综合这项前瞻性临床试验数据,以及上面提到的安德森癌症中心开展的实证研究,我们可以发现:对于EGFR单抗治疗后一度起效的晚期肠癌患者,在经过其他治疗方案干预后,间隔超过一定时间(最好是超过8-10个月)或者外周血中已经检测不到耐药突变后,可以酌情再次启用EGFR单抗。
免疫治疗时代:“再挑战”成功案例不多,机制复杂
既然靶向药可以考虑“再挑战”策略,其他药物是否也可以呢?事实上,在化疗药物治疗时代,国内外的专家通过多年的临床观察和相关的临床试验,已经积累了丰富的经验。如果某种化疗方案,曾经一度起效,且间隔时间已经超过半年,那么在其他标准治疗都失败的情况下,可以考虑再次启用。当然,如果某病友经历过很多化疗方案治疗,好几种老方案都符合这个标准,那么自然是优先选择,间隔时间更长、第一次使用时肿瘤缩小幅度更大、第一次使用时疗效维持时间更长的那种老方案。
化疗、靶向药都可以考虑“再挑战”策略,PD-1抗体等免疫治疗是抗癌原理截然不同的抗癌新药,是否也有类似的成功经验呢?日本同行在这个方案,走在了世界前列。
日本岗山大学附属医院的Toshio Kubo教授汇总了一组相关的回顾性研究数据。从2015年12月到2017年12月,日本7大著名的癌症中心,一共有434名晚期非小细胞肺癌患者接受过PD-1抗体治疗。截止目前,已经有317名患者因为疾病进展而停止PD-1抗体治疗;这317名患者中,有14人后续再次使用了PD-1抗体。有趣的是,这14名患者第一次使用PD-1抗体的时候,只有3名患者是客观有效的,5人是疾病稳定的,另外6人压根就是无效的(用药后疾病是进展的)——因此,严格意义上讲,这组病人并不是符合常规的“再挑战“,估计大多数是由于其他标准治疗均失败、”山穷水尽“了,再一次抓起PD-1抗体这根近年来被媒体和学术界热捧的救命稻草。
结果显示:3名第一次用药时客观缓解的病友,“再挑战“时均无效;5名第一次用药时疾病稳定的病友,”再挑战“时同样均无效。反倒是,6名第一次用药时原发耐药的病友,经过其他传统治疗的干预后,第二次使用PD-1抗体,有1名患者客观缓解、2名患者疾病稳定——有效率达到了16.7%,控制率达到了50%。有趣的是,那名”再挑战“获得客观缓解的病友,已经其中1名”再挑战“获得疾病稳定的病友,在两次使用PD-1抗体的间隔里,接受过放疗。因此,有专家推测是否中间安排的放射治疗,起到了一定的增敏作用。
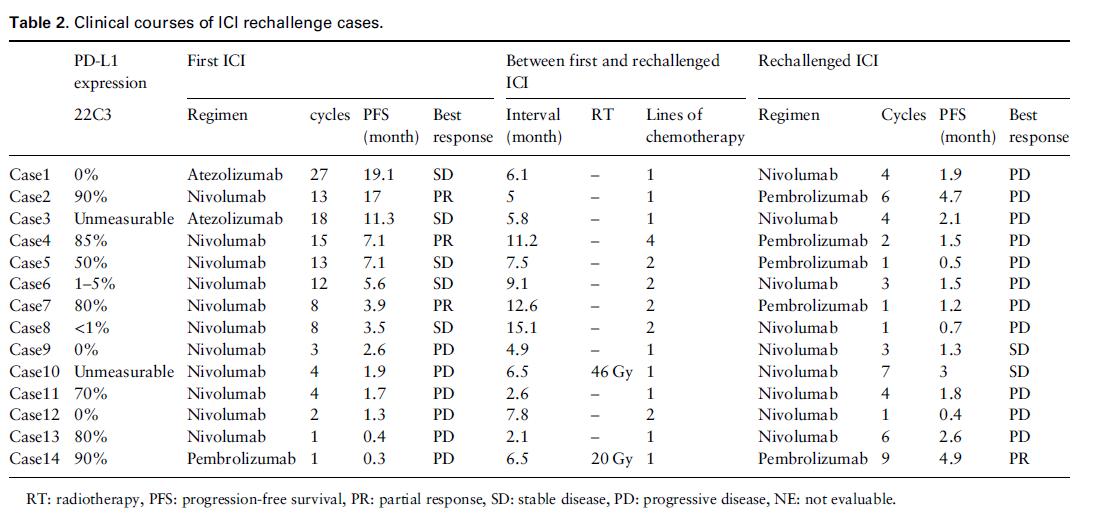
免疫治疗抗癌机理很特别,耐药的机制很复杂,且本身抗癌过程中又存在着诸如假进展、混合反应、爆发进展等诸多“怪事“,目前学术界对其研究还很不透彻。从上述小规模数据提示,对于PD-1抗体等免疫治疗的”再挑战“,目前学术界还有很多未解之谜,尚缺乏有效的手段和理论,可以提前预判到底哪些病人适合接受免疫治疗“再挑战”,因此对于绝大多数病友不做推荐。
参考文献
1. Anti-EGFR Resistant Clones Decay Exponentially After Progression: Implications for Anti-EGFR Re-challenge.
2. Rechallenge for Patients With RAS and BRAF Wild-Type Metastatic Colorectal Cancer With Acquired Resistance to First-line Cetuximab and Irinotecan A Phase 2 Single-Arm Clinical Trial. JAMA Oncol. doi:10.1001/jamaoncol.2018.5080
3. The effect and safety of immune checkpoint inhibitor rechallenge in non-small cell lung cancer. Japanese Journal of Clinical Oncology, 2019, 1–4