作者介绍:冰球,美国耶鲁大学临床医学博士(MD)和工商管理硕士(MBA)。现在美国排名前三的教学医院做内科医生和医院管理。
记得在医学院时,上有关乳腺癌的课,老师是这样开头的:
“班里在座的女生,你们每8个人中就会有一个人得乳腺癌。”
我们当时互相做个鬼脸,不以为然。
乳腺癌的数据早已烂熟于耳:最常见的女性癌症,2012年全球乳腺癌新发病率为1700万人;乳腺癌高发于北美和欧洲, 美国女性每8人里就有一人得乳腺癌。
近年来中国乳腺癌的发病率也在不断增加:每年中国乳腺癌新发数量和死亡数量分别占全世界的 12.2% 和 9.6%。预计到2021年,中国乳腺癌患者将高达250万。
但数据是冷冰冰的,在心中惊不起波澜。
直到临床实习时在乳腺外科轮转,看到一个个活生生的病人经历,直到年龄比我大不了几岁的年轻导师得了乳腺癌,直到专做乳腺癌手术的外科教授自己也得了乳腺癌,我才真切地感受到了乳腺癌的阴影无处不在。
令人欣慰的是,近几年乳腺癌的治疗手段和存活率都有很大突破,大多数乳腺癌只要发现治疗的及时,治愈的可能性很高。

下面我和大家聊聊近年来乳腺癌科研及临床的几大突破性进展。准备好了吗?都是满满的干货哦,需要一点耐心看完。
咱们先来学习几个乳腺癌和临床试验的概念(对这些概念有所了解的读者可以直接跳过这部分):
乳腺癌分子标记:对预测病情发展和治疗有指向标的作用。
ER, 雌激素受体;PR, 孕激素受体。两个合在一起又统称为激素受体( HR)。
HER2, 人类表皮生长因子第二型受体
这三个重要的标记在肿瘤细胞中可以有表达(即为阳性,通常用“+”表示) 或无表达(即为阴性,通常用“-”表示)
比如一个病人的乳腺癌为 ER+/PR+/HER2-, 意思就是说这个乳腺癌细胞有雌激素和孕激素受体的表达(为阳性,“+”),但没有人类表皮生长因子第二型受体的表达(为阴性, “-”)。
乳腺癌分期:乳腺癌分期和大部分癌症分期一样用的是TNM系统。
T 代表肿瘤大小,N代表受癌细胞侵袭的淋巴数量,M 代表有无其它器官扩散,分为1-4期。这里为了简便起见,我把第4期,也就是已有其它器官扩散的乳腺癌叫晚期, 1-3期统称为早期。
名词解释:
-总生存率(Overall survival:OS): 不用解释,就是一个人群中还活着的个体占人群的比例
-无疾病生存率 (Disease free survival:DFS): 一个人群中没有指定的疾病(如乳腺癌)的生存率
-无恶化生存率(Progression-free survival:PFS): 一个人群中有稳定疾病,没有恶化的生存率。
-术前的辅助疗法 (Neoadjuvant therapy): 在手术前进行的化疗、靶向疗法或放疗等手段。
-术后的辅助疗法 (Adjuvant therapy):在手术后进行的化疗、靶向疗法或放疗等手段。
-病理完全缓解 (Pathological Complete Response:pCR):指在术前辅助疗法后,乳房和/或淋巴里没有残留癌症 。(不同临床试验对此定义稍有区别,有些包括淋巴,有些不包括)
-靶向疗法 (Targeted therapy):和传统化疗的“一锅端”不同, 针对某个分子标记物的特定药物。如最早的靶向疗法就是用于HER2+ 乳腺癌的曲妥珠单抗(又叫赫赛汀)。
-美国的临床试验登记网www.Clinicaltrials.gov:在那儿能找到美国所有的临床试验, 每个试验有独一无二的标码,以 NCT带头。如NCT0000231
- 药品核准标示外使用 (Off-label use): 肿瘤医生可以通过这个渠道给病人用有些还没有正式通过FDA核准的药物,当然必须要有科研数据支持。
常见乳腺癌药物中英文对照:
Palbociclib (帕博西尼)
Letrozole (来曲唑)
Trastuzumab (曲妥珠单抗,赫赛汀)
Pertuzumab (帕妥珠单抗)
Lapatinib (拉帕替尼)
好了,学习完以上这些内容,你已经具备了解乳腺癌最前沿信息的能力了。下面我们一起来了解最新的科研临床进展吧!
黑体部分为某种疗法的概述,有兴趣的同学可以进一步阅读背景和临床试验部分,相关论文也都列于文末。
1. CDK 4 /6 *制剂抑**。
一类新型药物, 成为绝经后妇女晚期激素受体阳性 (HR+)乳腺癌 的新治疗标准。
目前通过美国FDA批准上市的有palbociclib (帕博西尼) (Ibrance) , 另外两个同类药物也都获得了FDA的“突破*药性**物疗法认证”,在上市的快车道上。它们分别是ribociclib 和 abemaciclib 。
背景:
长期以来,绝经后妇女如果有晚期激素受体阳性乳腺癌,唯一的一线药物是letrozole (来曲唑),一种aromatase inhibitor (芳香环*制剂抑**),效果差强人意。
CDK ( cyclin-dependent kinases) 有个很拗口的中文名字:周期蛋白依赖性激酶。在细胞分裂周期中起激活作用,抑制CDK4/6 导致细胞停留在G1阶段,无法正常完成分裂周期。由于这个特性,CDK4/6 *制剂抑**被选做了可行的药物。在早期细胞试验中, CDK被发现对 激素受体阳性乳腺癌细胞有抑制作用。
临床试验:
Palbociclib 是第一个研发上市的CDK4/6 *制剂抑**,在针对晚期激素受体阳性乳腺癌的二期临床试验中效果惊人:它和letrozole 联合,与只用letrozole相比,使病人的无恶化生存期延长了一倍 (从10.2月增加到了20.2月)。[1]
这个结果在三期试验中也得到证实:letrozole 单独用,无恶化生存期为14.5月,palbociclib+letrozole,无恶化生存期延长到24.8月。[2]
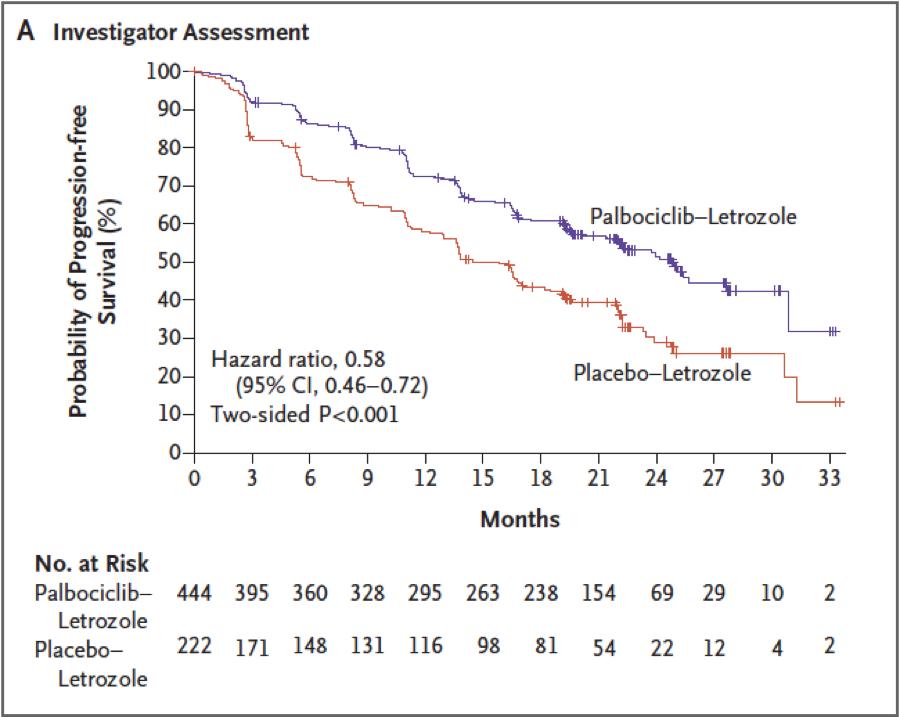
三期试验中Palbociclib+letrozole 对比letrozole +安慰剂的
当然,最有说服力的是总生存率的增加,目前数据还在随访中。
这里有一个小插曲: Palbociclib 的最早研发人和全球临床试验的领头人就是我住院医第一年在肿瘤内科住院部轮转时带队主治医师。那时palbocilicb 刚刚在二期试验结果基础上被FDA批准上市,大家都很激动。
Ribociclib,另一种CDK4/6 *制剂抑**,在陆续的临床试验中也被证实了很好的临床效果。[3]
第3 个CDK4/6 *制剂抑** Abemaciclib 的临床试验正在进行中,包括NCT02107703 和 NCT02246621。
目前使用palbociclib +letrozole 已成为绝经后晚期激素受体阳性乳腺癌患者的一线治疗方案。
2. 针对HER2+乳腺癌的靶向药物。
除了老牌的 trastuzumab ( 曲妥珠单抗, 赫赛汀 ), 不断有新药问世:pertuzumab (帕妥珠单抗),lapatinib (拉帕替尼),和 trastuzumab emtansine (T-DM1) 。
在临床应用中,trastuzumab 和pertuzumab 这两个靶向药物已联合使用(特别是用于术前辅助疗法和晚期已扩散的HER2+乳腺癌),同化疗一起,进一步增强了疗效。
Lapatinib 也已在临床中用于二线药物或在 药品核准标示外使用。
T-DM1 被批准用于晚期乳腺癌的二线或三线药物。
这些药物都还在十分活跃的进行临床试验中,未来可能用的范围会更广。
背景:
以前HER2+乳腺癌的病人生存率是比较差的,但自从第一个针对HER2 的靶向药物,单克隆抗体trastuzumab(曲妥珠单抗,赫赛汀)于1998年被批准应用于临床以来,HER2 +乳腺癌病人的存活率大大提高。
Pertuzumab也是一个针对HER2 的单克隆抗体,它还是第一个被称作 “HER二聚化*制剂抑**”的单克隆抗体(HER dimerization inihitor)。(这里省略100字解释……)
Lapatinib (拉帕替尼)是一种被称为Tyrosine Kinase Inhibitor (酪胺酸激酶*制剂抑**)类型的药物, 同时抑制 EGFR 和HER2 两个受体。
Trastuzumab emtansine (T-DM1) 是trastuzumab 和细胞毒类药物emtansine的组合药物。这个聪明的药物组合从理论上来说使药物先通过trastuzumab 攀附在表达HER2受体的细胞上,然后让emtansine 这个毒药继续把癌细胞杀死。
临床试验:
Pertuzumab:在晚期已扩散HER2+乳腺癌中,一个叫CLEOPATRA 的三期临床试验显示了pertuzumab 和 trastuzumab 合用大大增加了无恶化生存率和总生存率。[4]
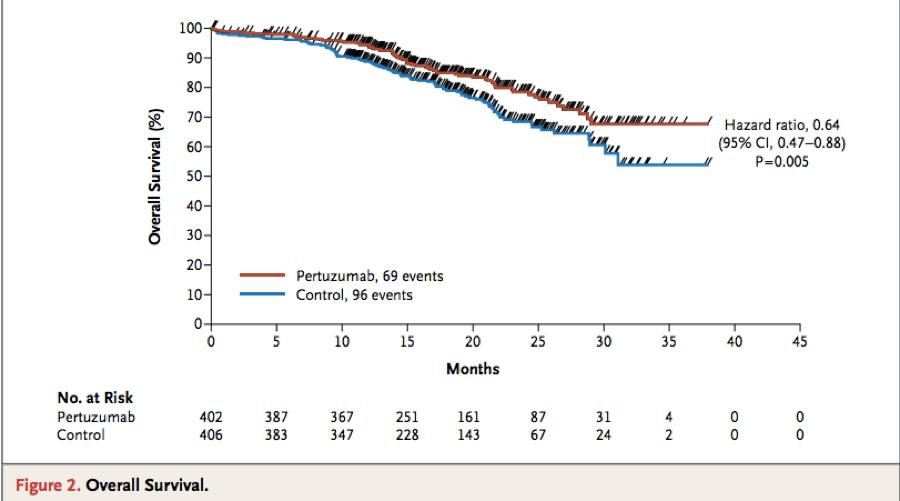
图:pertuzumab + trastuzumab +化疗药物Docetaxel 对比 安慰剂+trastuzumab+化疗药物Docetaxel的总生存率
在术前辅助疗法中,两个二期临床试验(简称为TRYPHAENA 和 NeoSphere)显示了明显提高的pCR( 病理完全缓解)率。近期公布的NeoSphere 的5年随访数据显示了领先的无恶化生存率。[5-7]
Laptinib: 一个叫NeoALTTO 的三期临床试验显示了在术前辅助疗法中lapatinib 和trastuzumab合用与trastuzuma单用相比,病理完全缓解(pCR)率有大大提高: 46.8% vs. 27.6%。[8]
但也有其他临床试验(如NSABP41)得出相反结果,表明这两组没有差别。[9]其中原因可能是 除了HER2受体的表达外,HR-和HR+的差别对病人也有影响。现在进一步针对细分HER2+/HR+和HER2+/HR-病人组的研究正在进行中。
T-DM1: 在晚期已扩散HER2+乳腺癌中,一个叫EMILIA的三期临床试验显示T-DM1的应用明显提高了无恶化生存率和总生存率。[10]另一个叫MARIANNE 的三期试验显示T-DM1和trastuzumab相比在晚期已扩散HER2+乳腺癌中效果相当。[11]目前更多关于T-DM1的临床试验进行的热火朝天,这里就不一一列出。
3. 芳香环*制剂抑**(Aromtase inhibitor)治疗绝经后妇女的早期HR+乳腺癌。
治疗时间从5 年增加到10年,进一步增加了无疾病存活率(91% vs. 95%)。[12]
4. 最新研究表明,对于早期HR+乳腺癌, 术前辅助治疗仅用激素疗法与化疗相比效果相当,但副作用大大减少。[13]
这个研究2016年11月刚刚发表,不久的将来,单独激素疗法可能取代化疗用于早期的激素受体阳性乳腺癌的术前辅助治疗。
5. 通过70个基因表达谱测试(70-gene signature profile, MammaPrint)可以成功预测低风险的早期乳腺癌病人,在这个人群中或可避免化疗。[14-15]
在这个叫MINDACT 的三期临床试验中,6693位患有早期乳腺癌的妇女,通过70个基因表达谱测试确定了她们基因组风险,同时通过Adjuvent!Online(一个临床评估风险工具)确定她们的临床风险。
按照标准,低风险基因表达和低风险临床特征的妇女没有接受化疗;高风险基因表达和高风险临床特征的妇女自动接受化疗。
另外共有1550名患者具有低风险基因表达和高风险临床特征,她们被随机分组到化疗或无化疗组。其中没有做化疗的患者的5年无扩散生存率为94.7%,而做化疗的5年无扩散生存率为96.2%。绝对差异只有1.5%。
所以文章得出结论,对于通过70个基因表达谱测试为低风险基因表达的早期乳腺癌病人(即使有高风险临床特征),可以避免化疗。
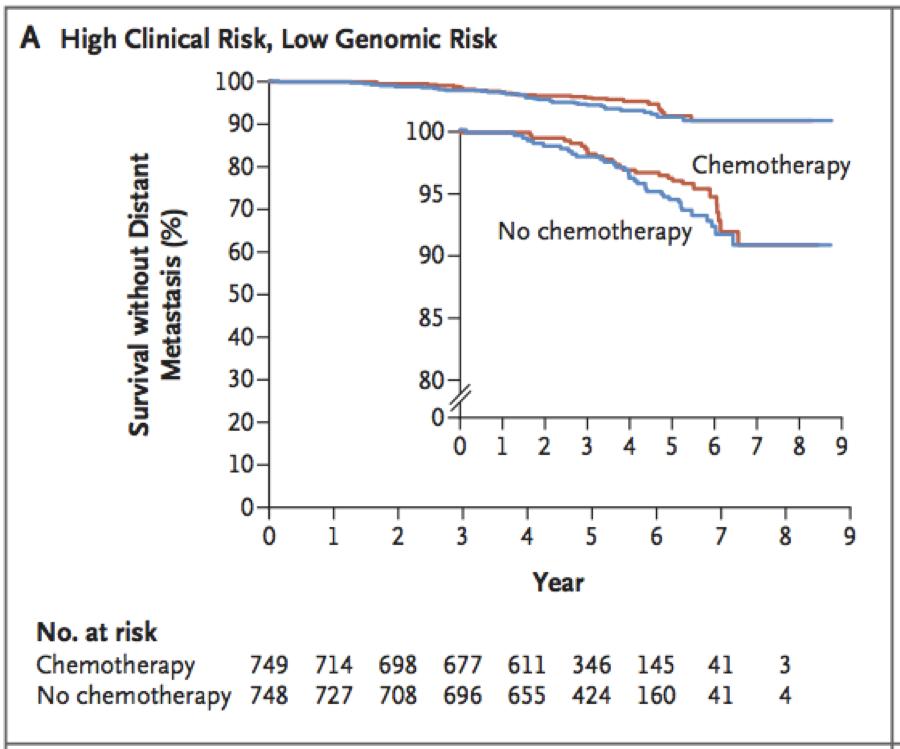
图: 在低风险基因表达和高风险临床特征组中的无扩散生存率。红线为做化疗的病人,蓝线为不做化疗的病人。图中小图和大图数据一样, 只是Y 轴放大了。
6. 头皮冷却疗法能够有效减少化疗期间的脱发。
一个研究显示Orbis Paxman防脱发系列使妇女在化疗期间脱发率减少了50%。[16]

未来展望:
乳腺癌的科研和临床前景十分乐观,相信会有越来越多的有效疗法来造福患者。其中值得关注的有:
专门针对BRCA 基因变异的乳腺癌和三阴性(triple-negative)乳腺癌PARP *制剂抑**;
用肿瘤浸润淋巴细胞 (TILS) 预测乳腺癌的复发率、生存率、及疗效;
还有,别忘了浩浩荡荡的免疫疗法大军也正在乳腺癌领域进行着一场革命。单个免疫疗法目前用在乳腺癌的效果差强人意,但多种免疫疗法结合,或与化疗和放疗结合的疗法可能会有令人欣慰的结果,让我们拭目以待。
本公众号系头条号签约作者,所发文章均为作者原创,并授权发表于头条号“健康不是闹着玩儿”。欢迎读者转发给朋友或朋友圈。任何公共平台(包括微信公众号,媒体等),未经许可,不得转载或盗用。联系我们,请发信到hi@jiankangkp.com。
参考文献:
1.Finn RS et al. The cyclin-dependent kinase 4/6 inhibitor palbociclib in combination with letrozole versus letrozole alone as first-line treatment of oestrogen receptor-positive, HER2-negative, advanced breast cancer (PALOMA-1/TRIO-18): a randomised phase 2 study. The Lancet Oncology. Jan 2015, 16(1):25-35.
2.Finn RS et al. Palbociclib and letrozole in advanced breast cancer. NEJM 2016;375:1925-1936.
3.Hortobagyi GN et al. Ribociclib as first-line therapy for HR-positive, advanced breast cancer. NEJM 375;1738-1748.
4.Baselga J et al; CLEOPATRA Study Group. Pertuzumab plus trastuzumab plus docetaxel for metastatic breast cancer. N Engl J Med. 2012;366(2):109-119.
5.Schneeweiss A et al. Pertuzumab plus trastuzumab in combination with standard neoadjuvant anthracycline-containing and anthracycline-free chemotherapy regimens in patients with HER2-positive early breast cancer: a randomized phase II cardiac safety study (TRYPHAENA). Ann Oncol. 2013;24(9):2278-2284.
6.NeoSphere: Gianni L et al. Efficacy and safety of neoadjuvant pertuzumab and trastuzumab in women with locally advanced, inflammatory, or early HER2-positive breast cancer (NeoSphere): a randomised multicentre, open-label, phase 2 trial. Lancet Oncol. 2012;13(1):25-32.
7.NeoSphere 5 year f/u: Gianni L et al. Five-year analysis of the phase II NeoSphere trial evaluating four cycles of neoadjuvant docetaxel (D) and/ or trastuzumab (T) and/or pertuzumab (P) [ASCO abstract 505]. J Clin Oncol. 2015;33(15)(suppl).
8.NeoALTTO: Baselga J et al; NeoALTTO Study Team. Lapatinib with trastuzumab for HER2-positive early breast cancer (NeoALTTO): a randomised, open-label, multicentre, phase 3 trial. Lancet. 2012;379(9816):633-640.
9.NSABP 41: Robidoux A et al. Lapatinib as a component of neoadjuvant therapy for HER2-positive operable breast cancer (NSABP protocol B-41): an open-label, randomised phase 3 trial. Lancet Oncol. 2013;14(12):1183-1192.
10.EMILIA: Verma S et al; EMILIA Study Group. Trastuzumab emtansine for HER2-positive advanced breast cancer. N Engl J Med. 2012; 367(19):1783-1791.
11.MARIANNE: Ellis PA et al. Phase III, randomized study of trastuzumab emtansine (T-DM1) ± pertuzumab (P) vs trastuzumab taxane (HT) for first-line treatment of HER2-positive MBC: primary results from the MARIANNE study [ASCO abstract 507]. J Clin Oncol. 2015;33(15)(suppl).
12.Goss PE et al. Extending Aromatase-Inhibitor Adjuvant Therapy to 10 years. NEJM 2016; 375(3):209.
13.Spring L et al. Neoadjuvant endocrine therapy (AI)for estrogen receptor-positive breast cancer: a systemic review and meta-analysis. JAMA Oncol. 2016 Nov 1;2(11):1477-1486
14.Cardoso F, et al. 70-Gene signature as an aid to treatment decisions in early stage breast cancer. NEJM 2016; 375:717-729
15.Van't Veer LJ et al. Gene expression profiling predicts clinical outcome of breast cancer. Nature 2002; 415, 530-536
16.Nangia et al. Scalp cooling alopecia prevention trial (SCALP) for patinets with early stage breast cancer. San Antonio Breast Cancer symposium, TX Dec 9, 2016