随着近年来临床及病理专家的不断关注研究,神经内分泌瘤(NEN)已经成为关注热点,对神经内分泌瘤认知度不断提升,目前已不算是临床罕见疾病。

神经内分泌瘤因其起源于无处不在的神经内分泌细胞,可涉及全身多个脏器组织,该病最常见原发于胃肠胰腺及肺部,而最常见的转移脏器为肝脏。文献数据显示小肠NEN的肝转移发生率为67%~91%,胰腺NEN的肝转移发生率为28%~77%,而出现肝转移的NEN患者生存预后往往最差,因此,有效控制肝转移瘤的治疗手段尤为重要,积极控制肝脏转移瘤进展对延缓病情恶化,延长患者生命、改善生存预后具有积极意义。

NEN的肝转移瘤虽然多经门脉系统转移播散至肝内,但是肿瘤供血仍以肝动脉供血为主,且多为富血供肿瘤,为肝动脉介入栓塞提供理论依据。
如为单侧或寡转移瘤者,可以尝试外科姑息性切除或者减瘤手术,甚至部分寡转移瘤者亦可以考虑经皮冷/热消融治疗达到根治手术切除效果。但因NEN肝转移瘤病理特点,肝内转移更多情况下还是以双叶、多发转移为主,此类情况更适合选择经血管途径进行区域性栓塞治疗,方可较为全面控制肝内转移灶。
目前临床上经肝动脉介入栓塞治疗模式主要为:单纯栓塞剂栓塞(TAE),先动脉灌注化疗+序贯动脉栓塞,碘油化疗乳剂(c-TACE)或者DEB栓塞(DEB-TACE),及放射性微球栓塞(RE)。
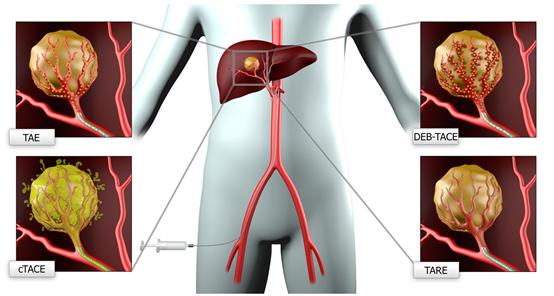
介入栓塞模式
TAE、TACE及DEB-TACE
TAE不同于TACE,TAE仅单纯使用各类栓塞剂,如碘化油、PVA、丙三烯明胶微球等,不联合化疗药物,进行肿瘤供血动脉末梢性栓塞,从而导致肿瘤缺血、坏死。DEB-TACE为近年临床广泛应用是新型栓塞材料,载药微球可搭载多种化疗药物。将载药微球栓塞至肿瘤末梢血管,一方面可以栓塞肿瘤供血动脉,导致缺血、缺氧坏死,另一方面可以缓慢、持续释放化疗药物,达到局部肿瘤组织较高药物浓度,而全身循环系统的化疗药物浓度较低,有效降低相关化疗药物毒副作用对人体全身影响。
文献报道肿瘤控制缓解率及生存率方面,TAE反而疗效更佳、预后更好,此数据结果可能与NEN大多数对化疗药物不敏感,联合使用化疗药物反而加重正常肝组织损害相关。
因此更推荐TAE(碘油或小粒径微球)模式,少部分对化疗药物相对敏感瘤种(如胰腺NEN)可酌情使用碘油化疗乳剂或者DEB,以分次栓塞为宜,以保护残存正常肝脏组织,防止肝功能衰竭。围手术期(24h)使用奥曲肽50μg/h持续泵注,可有效降低术后类癌危象发生率。另对于胆肠吻合术后患者,谨慎使用介入栓塞治疗,以免出现肝脓肿、胆道坏死等并发症,或者先行肝转移栓塞后再行原发肿瘤灶切除及胆肠吻合术,减少术后严重并发症发生。
介入栓塞的疗效与肿瘤病理分级、肝转移瘤负荷程度(≥75%)、肝外转移情况密切相关,亦有文献报道肝转移瘤血管丰富程度与病理分级正相关(病理分级越高,肿瘤病灶血供越加丰富)。
放射性微球栓塞(RE)
放射性微球栓塞(RE)使用玻璃或者树脂放射性微球进行肿瘤血管末梢性栓塞。临床上最常用的放射性微球使用钇90 (Y-90)放射性核素标记,可释放β-射线,半衰期为64.2 h,平均穿透深度2.5 mm。由于放射性微球体积较小(25 ~ 45 μm),相比TACE(大多粒径>100 μm),不会引起明显的缺血。
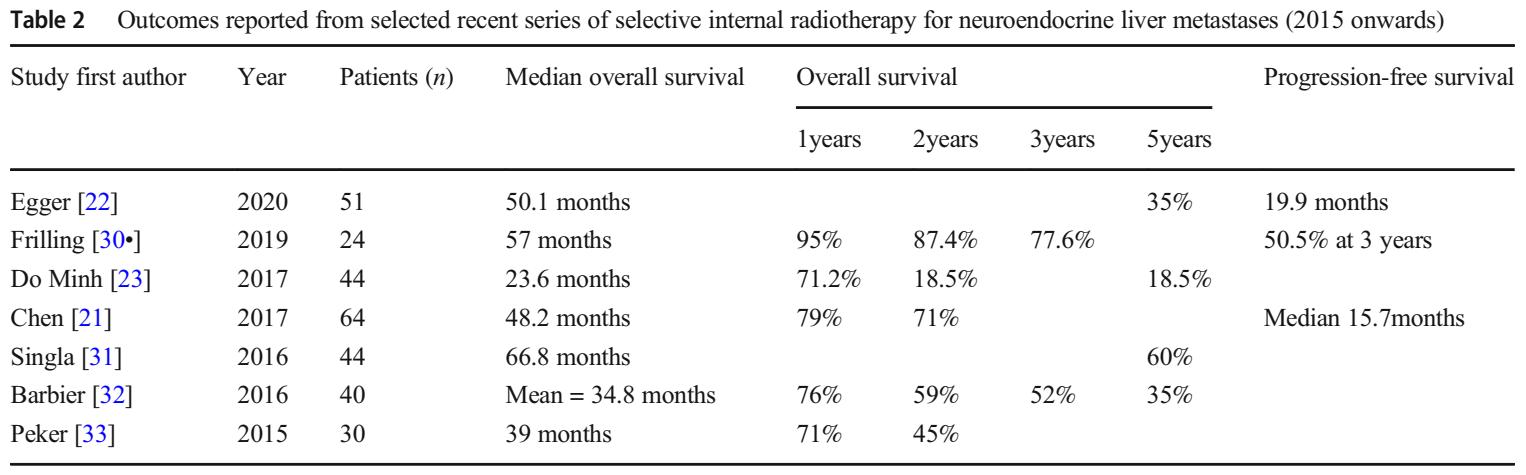
文献报道RE生存率情况
荟萃分析显示RE的客观有效率达51%(47~54%),疾病控制率可达88%(85~90%),中位生存期32个月(18~57个月)。
RE治疗原理不同,对于合并门脉癌栓者亦有一定疗效。但RE需要专用设备,术前需评估肝肺分流情况(AVS)及肝转移瘤负荷等情况,以减少放射性肝、肺损伤风险,保障RE疗效及安全性!今年放射性微球已经引入国内,目前海南、江苏等地已经率先开展,但因费用高昂(30万左右的治疗费用)且无法医保,需要配备专用治疗设备,临床上广泛开展应用仍需要一段较为漫长的路程!希望国内科研单位早日突破技术瓶颈,研发出国产替代产品,纳入基本医疗保障,才可能惠及广大国内患者。

局部介入栓塞治疗与系统治疗
目前系统治疗药物主要有长效奥曲肽(兰瑞肽)、靶向药物(依维莫司、舒尼替尼、索凡替尼等)及核素注射治疗。因NEN大多数为免疫治疗冷肿瘤,目前免疫治疗方面疗效尚未有显著性突破。
局部介入栓塞治疗与系统治疗联合治疗策略不明,如各种治疗手段先后顺序,合理选择系统药物诸多等疑问尚无明确的答案,不同于结直肠癌肝转移已经具有系统、规范指南,相关证据级别较低,仍需要更多研究数据积累。

欢迎点赞与关注,更多肝脏肿瘤微创介入治疗干货等你哦!