在阅读此文前,诚邀您点击一下 “关注” ,既方便您进行讨论与分享,又给您分享更多的专业健康知识,为您的健康保驾护航,感谢您的支持。
胸腔镜技术最早起源于1910年,由瑞典医生Jacobaeus利用改良膀胱镜发明而成,但是在很长一段时间里由于医学以及电子技术的限制,胸腔镜手术仅用于胸膜疾病的诊断及胸膜粘连的松解。
电视辅助胸腔镜手术(VATS)
直到1992年,VATS才首次报道用于肺叶切除术中,在此之后,胸腔镜手术治疗胸部疾病慢慢进入到了大众的视野中。

经过二十年不断的实践与检验,VATS的安全性,可行性,有效性被广泛的认可并且逐步取代传统开胸手术成为现代胸部手术实践操作的主流,也是许多国内外机构治疗大多数肺部、纵膈及胸膜疾病的首选微创治疗方式。
VATS是指在小型医用摄像头的辅助下进行的微创胸外科手术,该手术一般包含1~3个小切口用于通过摄像头及手术的器械装备,是目前胸外科的主要手术方法。

由于摄像头的放大作用,胸腔内的解剖结构及微小的病变得以更加清晰地展现,从而方便外科医生更加精确地判断病变的范围,进行病变部位的移除,增加了胸外科手术的安全性。
胸腔镜手术最大的特色之一是有限的小切口,避免了开胸手术的肋骨扩张等情况,更有利于患者术后的早期康复。 作为一种微创治疗技术,视频辅助胸腔镜手术是胸外科加速康复计划的重要组成部分。

相较于传统开胸手术,胸腔镜手术切口小且保留了相关的肌肉避免了不必要的血管损伤及肋骨扩张,因而极大限度地减少了术中失血量及伤口疼痛。
根据以往文献报道,胸腔镜手术可改善呼吸功能,减少肺炎、伤口感染、肺不张、心律失常等围术期并发症的发生, 从而减少术后总引流量,减轻术后疼痛,缩短总住院时间,提高患者对手术的耐受性,加快术后肺功能的恢复。

虽然胸腔镜手术更有利于患者的康复,但是其术后发生各种并发症的概率仍然很高。 根据癌症的不同阶段,胸腔镜术后五年内的全身复发率并不低,有25~70%患者最终复发。
由于术后疼痛,引起排痰障碍,导致分泌物潴留,引起肺不张、肺炎、胸腔感染、长时间漏气、低氧血症及高碳酸血症等一系列呼吸系统并发症, 发生率高达19~56%。炎症反应和术后疼痛是胸腔镜手术麻醉后两大常见的问题,严重影响着患者的术后康复及生活质量。
胸腔镜手术术后疼痛及术后炎症反应
胸腔镜手术术后疼痛
疼痛是与实际的或潜在的组织损伤相关的一种不愉快的情感体验,可由多种因素引起,包括组织损伤、炎症或者神经病理性改变等。 VATS等外科手术引起患者的疼痛往往是多个因素共同作用的结果。
首先,当伤害性刺激例如切皮等有创操作作用于机体时,会激活外周伤害性感觉神经元引起疼痛,这类疼痛的持续时间、强度等特征与伤害性刺激的存在密切相关。
其次,手术过程中药物的使用、输血及组织损伤等都会引起炎症介质的释放,导致外周痛觉感受器的阈值降低及中枢神经系统神经元的兴奋性增加,即外周致敏和中枢敏化。 这是除了神经损伤因素,造成术后急性疼痛的重要原因。
最后,当手术操作损伤神经时,损伤的初级感觉神经元及其邻近的非损伤神经元的钠离子通道会发生改变从而开始自发地产生动作电位, 产生自发性疼痛,并通过诱导中枢敏化进一步引起痛觉敏化和痛觉超敏的产生。
由于VATS的应用,相比于传统开胸手术而言,神经病理性疼痛的发生率有一定的降低。 术后疼痛是大部分外科手术术后常见的一种急性疼痛。

当伤害性感受器接受炎症因子及手术创伤等伤害性刺激后,会引起术后急性疼痛的发生。 当急性疼痛控制不佳时,则可能会诱发外周和中枢的痛觉敏化,最终演变成慢性疼痛。
虽然相比与传统开胸手术而言VATS一定程度地减少了侵入性伤害, 但是许多患者术后仍然遭受着中至重度的疼痛,特别发生在肺叶切除术等重大胸科手术之后, 因此VATS的镇痛依旧是麻醉医生关注的重点问题。
由于急性中至重度的术后疼痛控制不佳,有多达三分之一的VATS术后患者出现慢性疼痛及感觉异常。 造成这种情况的原因有以下三点:1.个人危险因素的不同,包括吸烟史、年龄和体重等。
2.VATS术中仍然发生了与开胸手术相似的与疼痛相关的病理生理学变化, 例如手术组织创伤、全身炎症反应、单肺通气及血流动力学的变化等。
3.术后引流管的存在、位置及插管的次数和肩痛综合征的发生依旧是常见且难以避免的重要相关因素。
良好的术后疼痛管理是改善恢复和降低并发症发生的先决条件,因此术后疼痛管理不足不但会延长患者住院和恢复的时间,增加阿片类药物的使用, 会影响有效的胸部扩张、咳嗽与呼吸,引起术后肺不张和肺炎等并发症,最后导致生活质量的下降和手术术后病死率的增加。

术后炎症反应
全身炎症反应(Systemicinflammationresponse,SIR)是免疫系统对感染性或非感染性损伤的一种反应, 帮助消除体内感染性病原体,从而达到恢复受损器官正常的解剖结构和功能,维持机体内稳态的目的。

在手术干预过程中,手术创伤可以通过全身促炎和代偿性抗炎反应诱导SIR的发生。 但手术应激诱导的免疫炎症反应不一定与组织损伤成正比,还包括全身麻醉本身、机械通气、使用血液制品、止吐药等其他因素。
对于胸外科手术而言,SIR的重要意义在于减少术后并发症的发生以及控制肿瘤细胞的扩散。

与开胸手术相比,VATS一定程度减少了干预诱导的炎症反应,减少了手术应激,但随着微创胸外科手术的普及和增进, 为了使手术应激最小化、减少并发症的发生、促进患者的快速康复,仍需要进一步优化VATS的麻醉管理。

胸科手术加速康复策略
加速康复外科(enhancedrecoveryaftersurgery,ERAS)策略又称为快速通道,是一种涵盖多学科、多模式的手术患者治疗方法, 旨在最大限度地减少患者的术中应激反应,从而减少并发症,加速患者的术后恢复,缩短住院时间,减少住院成本和发病率。

ERAS的概念是在1997年提出的,首先用于结直肠手术的患者中,但是随着内窥镜和血管内技术等微创技术的发展和进步,它逐渐应用于许多其他领域。
电视辅助胸腔镜技术的应用使得胸外科可以通过微创的方式治疗大多数肺部、胸膜和纵隔疾病,并且使ERAS在胸外科领域中受到了广泛的关注。

但是随着对胸腔镜手术的ERAS项目的开展与研究,外科医生、麻醉医生和重症监护医生开始注意到, 即使在术中使用了微创技术,但与传统的开胸手术相比,总体住院时间和术后肺部并发症的发生率没有出现预期的变化,
因此人们提出术前、术中和术后的麻醉管理是建立成功的胸腔镜手术加速康复计划的关键。
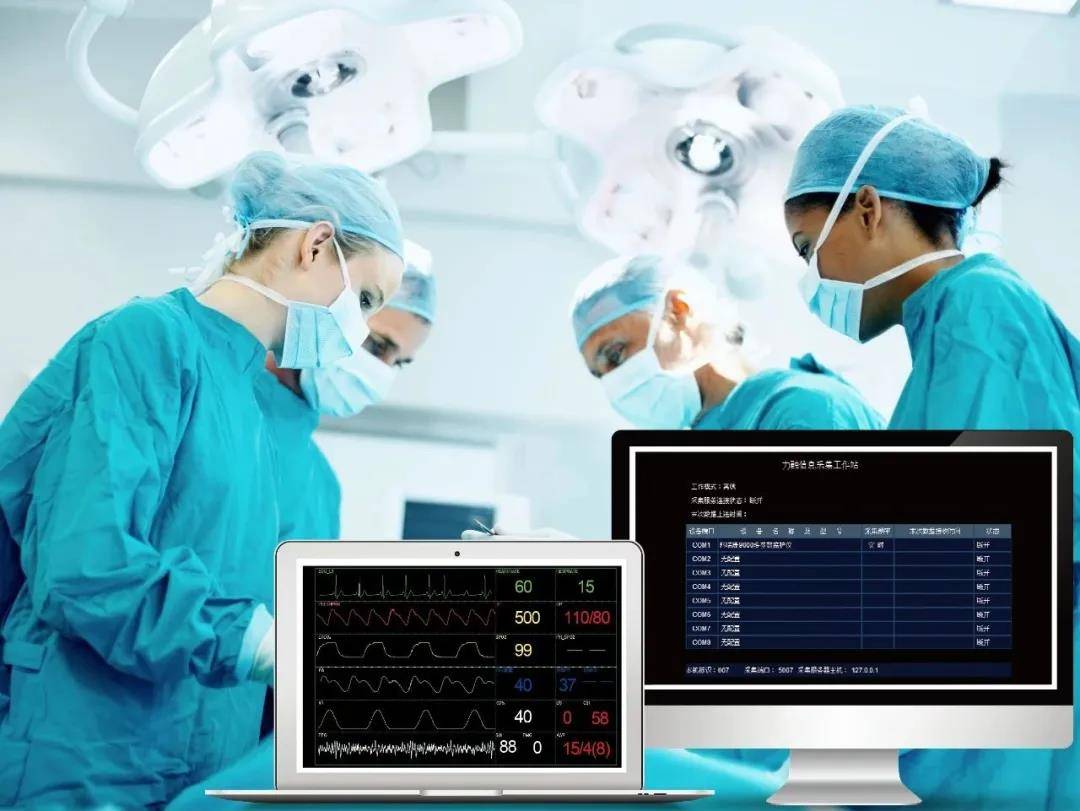
有效的围手术期疼痛管理是ERAS项目的关键部分。临床手术中最常用的是阿片类药物,然而,它们表现出许多不良反应,如呼吸抑制和术后恶心呕吐等,可能会影响患者实现ERAS目标。
以往研究显示阿片类药物单独给药可能对控制持续性疼痛有效,但对与咳嗽和运动相关的偶发性疼痛无效,考虑到大多数胸外科手术的患者可能发生的合并症,最好限制阿片类药物的剂量。
因此,在VATS中,多模式镇痛策略结合个体化镇痛管理应是麻醉医生首选的镇痛方式。VATS手术疼痛管理有两个主要目标: 一是良好的镇痛,提高患者舒适度,二是对抗疼痛引起的生理病理学变化。
局部和全身炎症反应是普遍存在于手术创伤中的病理生理学变化,促炎分子在术后疼痛诱导中起着重要的作用,可能调节术后疼痛的强度。

因此,通过研究药物对促炎因子血清浓度的调节可能丰富多模式镇痛的药物选择。 胸外科手术ERAS的主要目标是减少应激反应,减轻患者炎症反应和疼痛,减少术后肺部并发症的发生,改善患者预后。
其中良好的麻醉管理作为促进恢复的必要条件在胸外科手术ERAS中发挥着重要的作用。 平稳的血流动力学维持、充分的围手术期液体管理、保护性通气策略、有效的镇痛和短效药物的使用是胸外科ERAS的基本要素。

在胸外科ERAS计划中麻醉医生应根据患者的个人因素和明确的手术因素实施量身定制的精确麻醉, 包括全身麻醉结合区域阻滞,短效药物的使用和允许早期拔管等以改善短期和长期的患者预后。
目前面临的挑战是寻求一种短效的麻醉相关药物,既能抑制手术应激反应,又能与其他药物产生良好的协同作用(例如减轻阿片类药物的副作用等), 同时具有良好的安全性,可能避免癌症复发或者减少其他肺部并发症的发生等。

非甾体类抗炎药、利多卡因、n-甲基-d-天冬氨酸拮抗剂、糖皮质激素、加巴喷丁类药物、 α2-肾上腺素受体激动剂 等药物都是目前胸外科ERAS中所提及的药物。
静脉输注利多卡因的临床应用
利多卡因是临床上使用最早的一种中短效酰胺类局麻药,具有起效快、作用强的特点,并且被许可用于静脉注射。

利多卡因主要通过肝脏代谢,在健康成人体内,其消除半衰期为80~110min,一般认为利多卡因的安全有效的血药浓度为1.4~6.0µg/ml, 但由于治疗剂量和中毒剂量相差较小,因此静脉注射利多卡因的安全性是临床上广泛关注的一个重要问题。
2021年发布的第一个关于静脉输注利多卡因的共识推荐以体重计算利多卡因的剂量,输注速度不宜过快, 负荷剂量(≤1.5mg/kg)的输注时间应不小于10min,长时间静脉输注的速度以1.5mg/kg/h为宜,输注时间不应超过24h。

利多卡因起初作为局部*醉药麻**和抗心律失常药在临床被广泛使用,随着研究的不断深入,静脉注射利多卡因在围术期被广泛应用, 其具有以下众多优点:1.减轻术后疼痛,减少阿片类药物的消耗及相关副作用的发生。
2.抑制插管引起的血流动力学变化。3.全身抗炎特性。4.抗癌特性,可能直接抑制癌细胞转移。5.加速胃肠功能的恢复。 6.可通过血脑屏障,维持脑血流,提供脑保护。7.减少术后恶心呕吐的发生。
鉴于以上众多优点,静脉输注利多卡因已经在许多ERAS项目中得到实施,并且很多学者提出可将利多卡因作为多模式镇痛的一部分。 目前围手术期静脉输注利多卡因预防术后疼痛的作用机制尚未明确,可能由多方面因素决定。
较为熟知的利多卡因的作用机制是通过阻断电压门控钠离子通道,降低细胞膜对钠的通透性,减少膜的去极化,阻止动作电位的传播,从而减少疼痛刺激的神经传导。

此外,相关的镇痛机制可能还包括:静脉注射利多卡因可能直接激活阿片类受体产生镇痛作用; 可以直接抑制无髓鞘C纤维的兴奋性和传导;可以作用于毒蕈碱和*碱烟**受体,从而增加中枢神经系统乙酰胆碱的释放,激活疼痛下行抑制通路;
N-甲基-D-天门冬氨酸受体 是中枢神经系统快速兴奋性神经传递的主要受体, 而利多卡因可以与其结合从而抑制N-甲基-D-天门冬氨酸受体,产生抗痛觉过敏的作用等。

利多卡因的抗炎作用已经被广泛的接受和认可,这一作用与炎症细胞特别是多形核细胞密切相关, 而由于多形核细胞等并不表达钠离子通道,因此利多卡因的抗炎作用可能由其他多种机制介导,
例如:利多卡因降低多形核细胞的移动性和黏附性,从而抑制多形核细胞的启动迁移; 利多卡因通过抑制N-甲基-天门冬氨酸受体和抑制中性粒细胞激活而具有抗炎作用, 从而减少细胞因子的产生;

利多卡因通过抑制包括p38丝裂原活化蛋白激酶和核因子-kappaB信号通路,抑制毒性无氧自由基的产生而发挥抗损伤作用; 利多卡因通过丝裂原激活蛋白激酶途径增强半胱氨酸天冬氨酸蛋白酶依赖的癌细胞凋亡;
利多卡因通过抑制细胞迁移和肿瘤TNF-α诱导的Src激酶激活和细胞间粘附分子-1磷酸化从而起到抵抗癌细胞转移的作用。
综上所述, 利多卡因作为一种非阿片类镇痛辅助药物在围术期可能发挥着重要的作用,由于其麻醉、抗炎、调节免疫等多种特性, 利多卡因可作为多模式镇痛的重要部分并可能被纳入到众多外科手术的ERAS策略中,例如静脉注射利多卡因已被纳入结直肠手术ERAS指南中。

然而在胸科手术中围术期是否常规静脉注射利多卡因还存在争议,有研究显示利多卡因在胸外科手术中可以减少阿片类药物的消耗,减轻术后疼痛,促进患者术后恢复,而另一些结果则与之完全相反。
在动物试验中显示静脉输注利多卡因可能通过减少细胞因子的产生,减轻炎症反应从而减少急性肺损伤的发生,起到肺保护和促进术后恢复的作用,但是这一结果是否也适用于临床目前仍不确定。因此,需要更多的研究来证实围术期静脉注射利多卡因在VATS的作用,特别是在镇痛、抗炎和康复方面。
