第一作者:常梦宇
通讯作者:侯智尧,赵彦利,林君
通讯单位:中国科学院长春应用化学研究所;广州医科大学;南洋理工大学;
论文DOI:10.1002/anie.202209245
全文速览
热休克蛋白(HSPs)的上调严重损害了温和光热治疗(PTT)的效果。针对此,作者合成了多孔的铜单原子纳米酶(Cu SAzyme),并将LIK066药物载入其中,从而将热休克蛋白沉默以实现温和PTT。一方面,LIK066通过关闭钠依赖性葡萄糖转运蛋白(SGLT)“阀门”来抑制葡萄糖摄取,有效地阻断三磷酸腺苷(ATP)产生的能量来源。没有充足的能量供应,癌细胞无法合成HSPs。另一方面,Cu SAzyme具有多酶活性,可诱导活性氧(ROS)风暴形成,从而破坏癌细胞中现有的HSPs。因此,通过SGLT*制剂抑**和ROS风暴的“*管双**齐下”策略,负载LIK066的Cu SAzyme可全面清除癌细胞中的HSPs,实现高效的温和PTT。
背景介绍
由于优异的治疗效果和生物相容性,温和PTT在抗肿瘤治疗领域显示出巨大的潜力。然而,癌细胞中热应激响应而上调的HSPs急剧减弱了温和PTT治疗效果。为了解决这一问题,一些小分子*制剂抑**(藤黄酸,17-AAG,STA-9090等)已被应用于温和PTT。然而,由于这种小分子的作用机理往往是损伤热应激之后产生的热休克蛋白,它们通常会造成滞后的治疗效果。为了提高温和PTT的效果,从源头抑制HSPs的产生是极其重要的。在癌细胞的新陈代谢过程中,大部分的细胞能量是由厌氧糖酵解提供。因此,癌细胞必须摄入大量的葡萄糖供应其生理活动,包括热休克蛋白的合成。基于这一新陈代谢特征,抑制葡萄糖摄取途径、能量转化和释放过程将是从源头阻断HSPs产生的最佳策略。
本文亮点
本工作合成了具有丰富的微孔和介孔结构的Cu SAzyme,并将临床批准的降血糖药物LIK066装载入其中,形成产物Cu SAzyme@LIK066(CuL)。
(1) 负载的LIK066可通过阻断主动转运途径钠依赖性葡萄糖转运蛋白(SGLT),有效抑制癌细胞葡萄糖摄取。通过*锁封**能量来源,可从源头上有效抑制热休克蛋白的产生。
(2) 具有高原子利用效率的Cu SAzyme可以产生活性氧(ROS)风暴(·O2-、1O2和·OH),其能损害蛋白质结构,从而消除癌细胞中已经存在的HSPs。
综上所述,CuL提供了SGLT*制剂抑**和ROS风暴“*管双**齐下”策略,使HSPs沉默,从而实现了高效的温和PTT。

图1 (a) CuL的合成步骤。(b) SGLT和ROS风暴“*管双**齐下”策略实现温和PTT的示意图。
图文解析
图2. Cu SAzyme的合成与表征: TEM和BET结果表明了Cu SAzyme具有大量的微孔和介孔。XRD表明在Cu SAzyme样品中,未发现铜纳米颗粒。通过HAADF-STEM表征,检测到了原子分散的Cu单原子,且EDS结果也表明了Cu元素的存在。
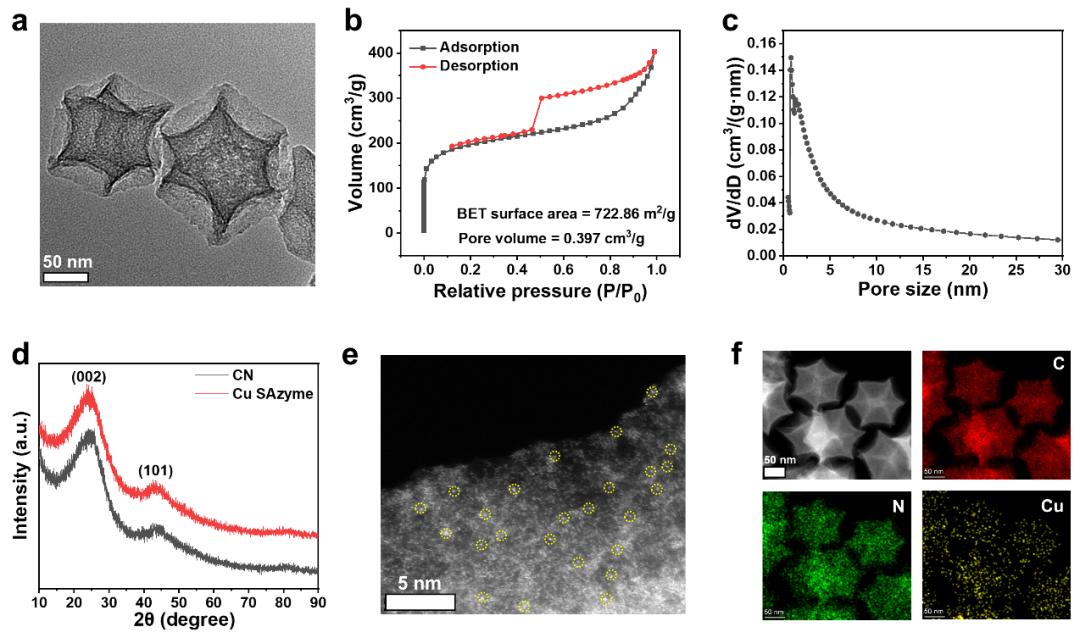
图3. Cu SAzyme的同步辐射表征: 通过同步辐射测试,可得出Cu SAzyme为四配位Cu-N键单原子结构。
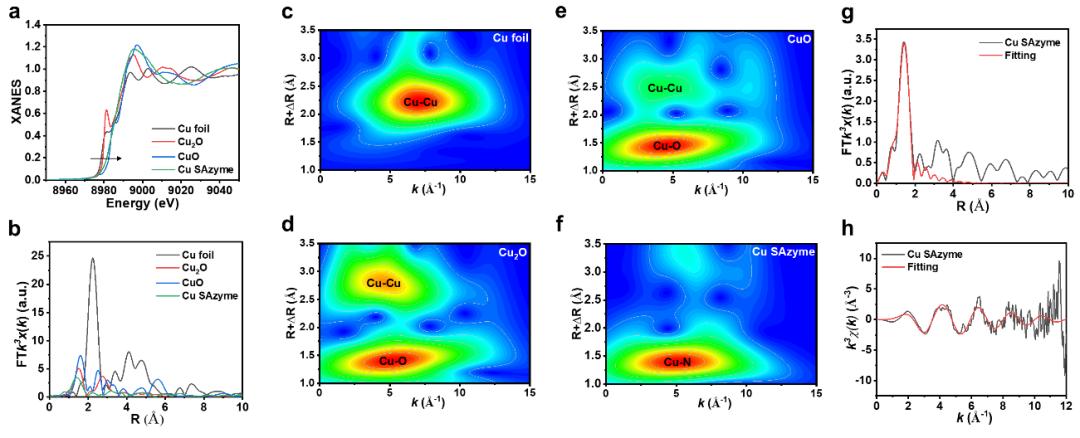
图4. Cu SAzyme的性质 :Cu SAzyme在近红外区域具有强的光学吸收,因此其可在1064 nm激光触发下,实现光热转换。此外,其可产生大量的ROS(·O2-、1O2和·OH)。
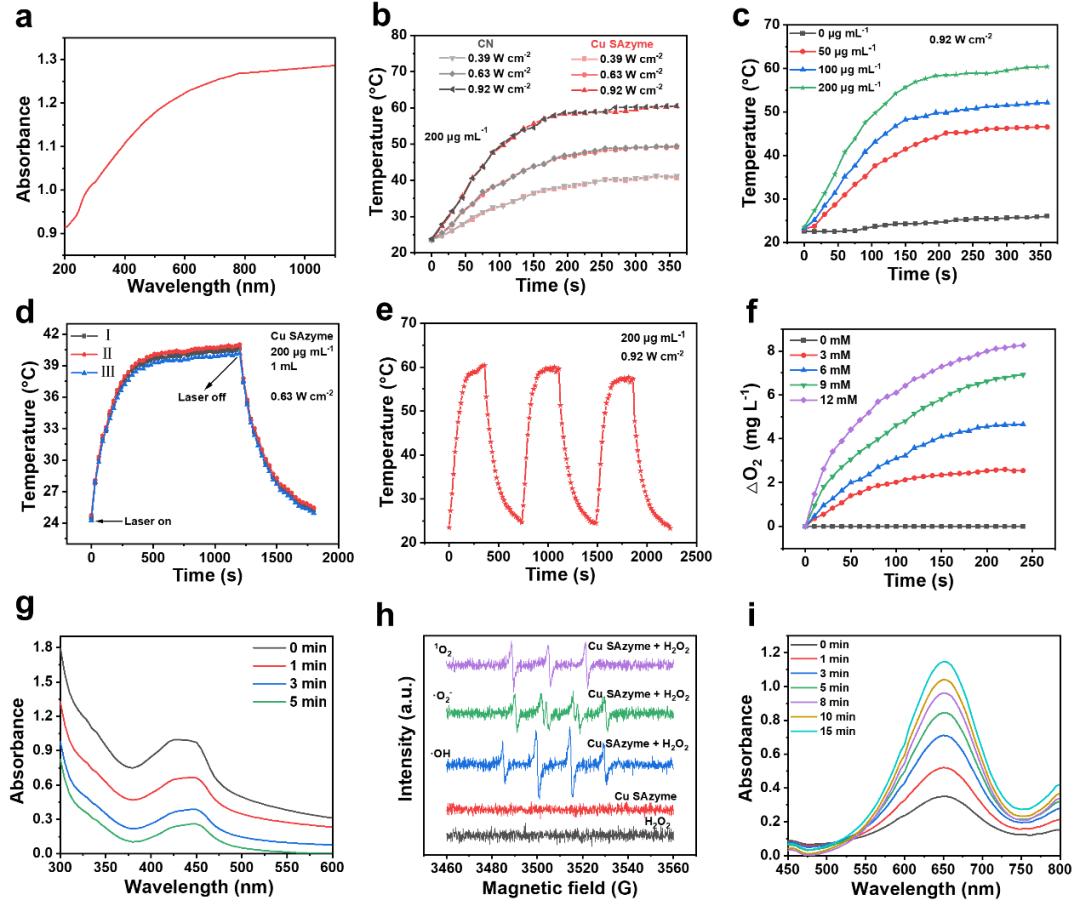
图5. Cu SAzyme担载LIK066性质测试 :Cu SAzyme可有效装载LIK066,并在弱酸性和光照的条件下,实现LIK066药物的加速释放。
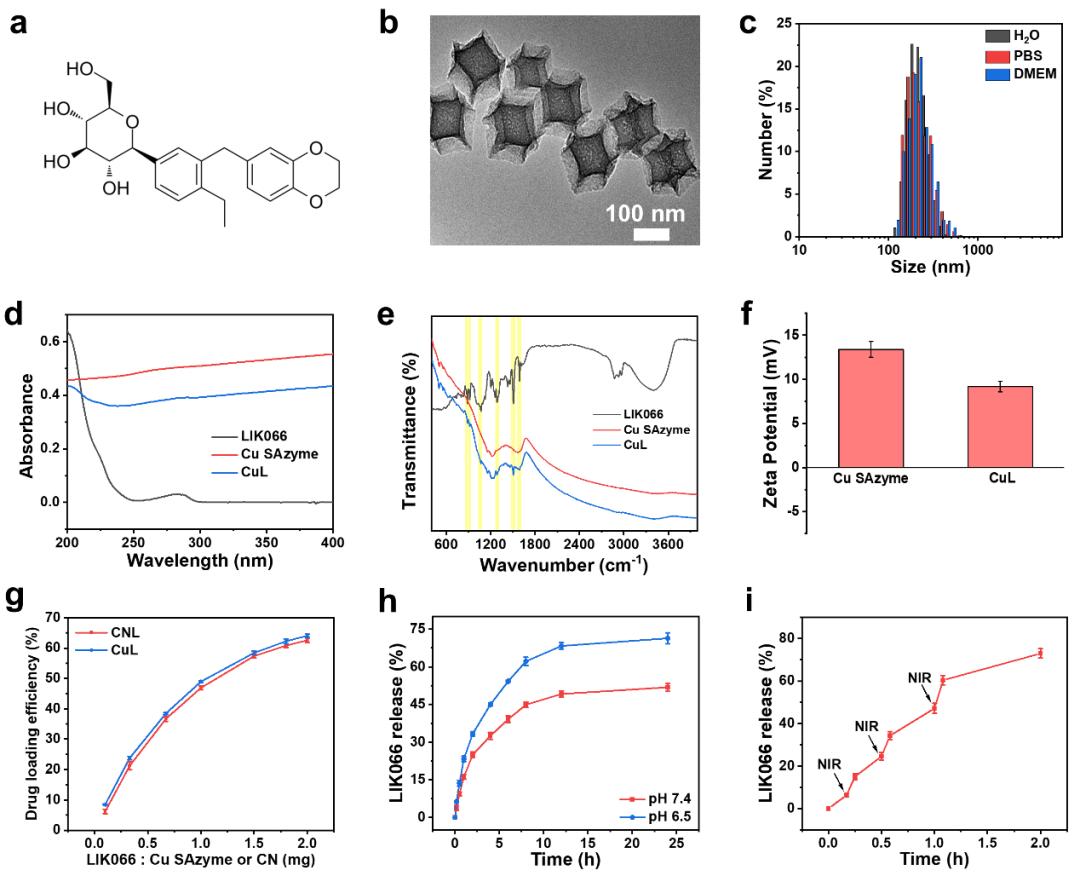
图6. CuL在细胞层面的治疗效果及机理研究 :由于协同的癌细胞能量摄入抑制,以及ROS风暴的产生,其可有效破坏癌细胞中的HSPs。因此,相比于单独的Cu SAzyme,LIK066,以及Cu SAzyme激光照射组,CuL在1064 nm激光照射下,可极大程度地*伤杀**癌细胞。
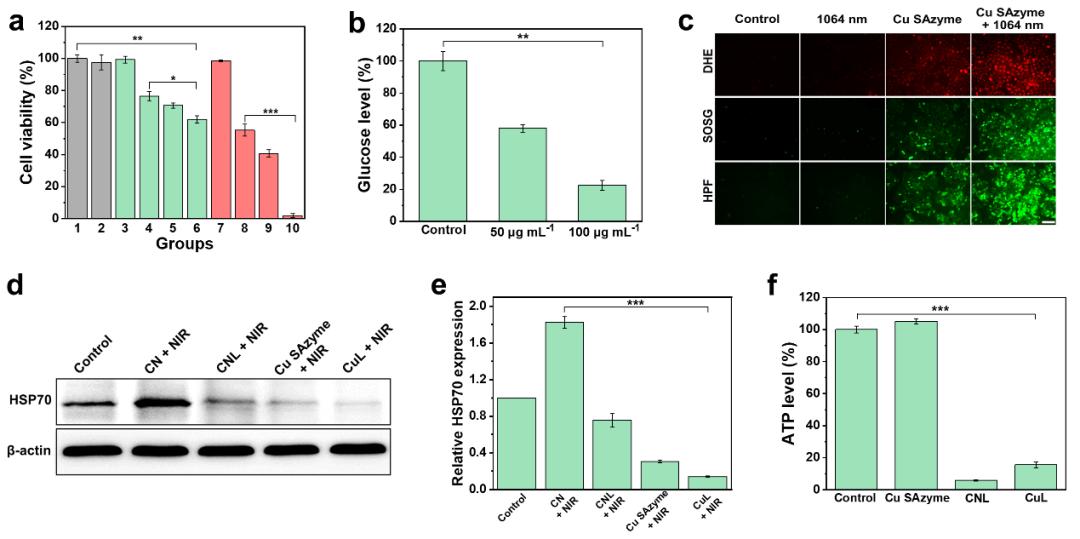
图7. CuL在活体层面的治疗效果 :由于SGLT和ROS风暴“*管双**齐下”策略,CuL可实现高效的温和PTT,几乎可将肿瘤完全消融。

总结与展望
本工作合成了具有丰富介孔和微孔的Cu SAzyme,并负载临床批准的降血糖药物LIK066,形成CuL。通过SGLT*制剂抑**和级联的ROS风暴“*管双**齐下”策略,CuL实现了高效的温和PTT。一方面,LIK066可关闭“SGLT”阀门,从而有效*锁封**葡萄糖的摄入。另一方面,具有高原子利用效率的Cu SAzyme可产生ROS风暴,从而损害癌细胞中已经存在的HSPs的结构和功能。总的来说,这项工作为温和PTT的未来发展提供了有价值的指导方向,其中未研发的代谢通道以及调控癌症细胞代谢的药物值得进一步探索。
作者介绍
常梦宇, 博士毕业于中国科学院长春应用化学研究所(导师:林君研究员,侯智尧教授),现为南洋理工大学赵彦利教授课题组博士后。研究方向为基于无机纳米材料的抗肿瘤治疗。在Adv. Mater., Angew. Chem. Int. Ed.等期刊发表学术研究成果。
侯智尧, 广州医科大学基础医学院,教授,博士生导师。2009年哈尔滨工程大学获得材料学博士学位,2010-2012年中国科学院长春应用化学研究所博士后,师从林君研究员,出站后留所工作。2019年加入广州医科大学,目前主要从事新型纳米光能转换材料构建及其在肿瘤光学诊疗中应用的基础研究。以第一/通讯作者在Adv. Mater.、Angew. Chem. Int. Ed.、ACS Nano、Adv. Funct. Mater.、Small、Biomaterials等期刊上发表论文。
林君 ,中国科学院长春应化所研究员、博士生导师,曾获得国家杰出青年科学基金,并入选万人计划科技创新领军人才,中国*土稀**学会发光专业委员会主任。1989 年毕业于吉林大学化学系,1995 年在中科院长春应化所无机化学专业获博士学位。1996-2000 年分别在香港、德国和美国做访问学者及博士后。主要从事纳-微米结构发光材料的控制合成、形态结构和性能调控及其在显示照明及生物医学领域的应用基础研究。2009年和2014年分别获吉林省科技进步一等奖和吉林省自然科学一等奖;2014-2021连续入选“汤森路透(科睿唯安)全球材料及交叉领域高被引科学家”名录。至今已在国内外核心期刊如Chem. Rev.、Chem. Soc. Rev.、J. Am. Chem. Soc.、Adv. Mater.、Angew. Chem. 等上面发表学术论文800 余篇,他引6万余次。