▎医药观澜/报道
9月18日,中国国家药监局(NMPA)行政事项受理服务查询显示,德国默克西妥昔单抗(爱必妥)的上市申请(受理号JXSS1700013)审批状态更新为"审批完毕-待制证"。这意味着,继转移性结直肠癌之后,爱必妥有望在中国收获第二项适应症。根据德国默克就该药在中国开展的临床试验以及提交的上市申请的情况来看,这项新适应症极有可能为RAS野生型转移性结直肠癌一线治疗。
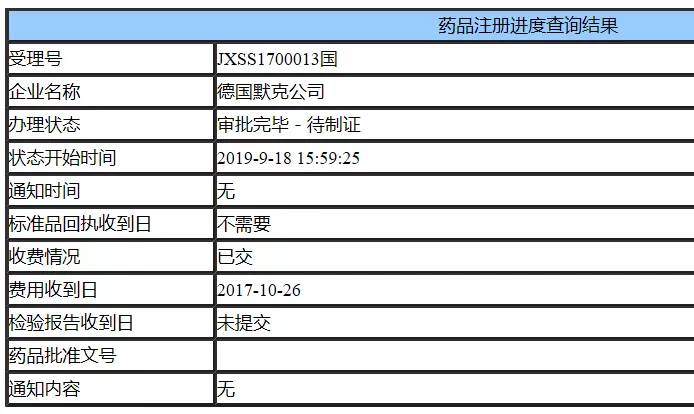
▲截图来源:NMPA行政事项受理服务查询官网
爱必妥是靶向表皮生长因子受体(EGFR)的IgG1单克隆抗体,该药通过与EGFR特异性结合,抑制受体激活以及后续的信号传导通路,从而减少肿瘤细胞对正常组织的侵袭、阻碍肿瘤扩散到新的部位。2005年,爱必妥获得NMPA批准上市,适应症为单用或与伊立替康联用于表皮生长因子受体(EGFR)过度表达的,对以伊立替康为基础的化疗方案耐药的转移性结直肠癌的治疗。
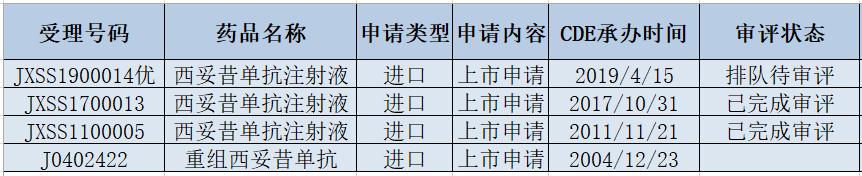
▲爱必妥中国上市申请一览(数据来源:CDE官网)
从NMPA药品审评中心的受理情况来看,德国默克一共在中国递交了4项爱必妥的上市申请。其中,2004年和2011年提出的两项上市申请(受理号J0402422、JXSS1100005)均已在2014年以前获得NMPA批准。
根据药物临床试验登记与信息公示平台,爱必妥在中国登记开展了共计3项临床试验,其中2项针对RAS野生型转移性结直肠癌一线治疗,1项针对复发和/或转移性头颈部鳞状细胞癌一线治疗。3项临床试验的首次公示时间均在2014年及以后,这意味着,德国默克就该药分别在2017年和2019年提交两项上市申请,适应症可能分别为RAS野生型转移性结直肠癌一线治疗,以及复发和/或转移性头颈部鳞状细胞癌一线治疗。

▲爱必妥中国临床试验一览(数据来源:药物临床试验登记与信息公示平台)
2018年欧洲肿瘤内科学会(ESMO)亚洲年会上,德国默克宣布爱必妥联合铂类化疗(EXTREME方案)一线治疗复发性和/或转移性头颈部鳞状细胞癌中国患者的3期临床研究的积极数据。数据显示,在含铂方案中联合爱必妥进行治疗,可以改善无进展生存期、总生存期和总缓解率。
基于该试验结果,德国默克宣布将向NMPA提交注册申请,将爱必妥EXTREME方案带给中国复发性/转移性头颈部鳞状细胞癌患者。另外,2018年默克中国生物制药业务肿瘤事业部负责人袁泽之曾在公开场合表示:爱必妥计划在中国申请的一项新适应症为头颈癌。

由于此次“审批完毕”的上市申请(受理号JXSS1700013)是在2017年提交,这一时间早于爱必妥治疗头颈部鳞状细胞癌中国患者3期数据公布的时间。同时,也比德国默克公开表示要在中国申请爱必妥新适应症头颈癌的上市计划要早。综合来看,此次爱必妥在中国获批的适应症,更有可能为:一线治疗中国RAS野生型转移性结直肠癌患者。
在一项随机2期OPUS试验回顾性分析中,数据显示,对KRAS野生型转移性结直肠癌患者一线西妥昔单抗联合FOLFOX治疗能获得良好的疗效。另一项CRYSTAL研究的回顾性分析也显示,对野生型患者一线西妥昔单抗联合FOLFIRI治疗获得了良好的疗效,疾病进展危险度下降32%。
上述临床研究表明,西妥昔单抗能让KRAS野生型转移性结直肠癌患者获益。基于此,2009年NCCN结直肠癌指南中建议KRAS野生型晚期转移性结直肠癌患者一线治疗可以选择西妥昔单抗联合化疗。
此前,爱必妥联合FOLFOX或FOLFIRI已被中国临床肿瘤学会(CSCO)结直肠癌指南和卫健委中国结直肠癌诊疗规范推荐为RAS野生型转移性结直肠癌的一线治疗方案,尤其针对左半mCRC患者疗效更优。去年10月,爱必妥正式被列入中国国家医保目录,用于RAS野生型转移性结直肠癌患者的治疗。

值得一提的是,爱必妥另一项可能用于头颈部鳞状细胞癌一线治疗的上市申请(受理号JXSS1900014)已在今年8月被纳入优先审评。这意味着,爱必妥在中国很快将迎来两项新适应症的获批。我们祝贺这款生物药在中国取得又一大进展!
题图来源:Pixabay
参考资料:
[1]中国国家药监局(NMPA)行政事项受理服务查询. Retrieved Sep 19, 2019, from http://sq.cfda.gov.cn/datasearch/schedule/search.jsp?tableId=43&tableName=TABLE43&columnName=COLUMN464,COLUMN475&title1=药品注册进度查询
[2]重磅速递 | 默克靶向药物西妥昔单抗注射液成功纳入国家医保目录. Retrieved Oct 11, 2019, from 德国默克官微