本周,美国食品药品监督管理局(FDA)接受了由Spark Therapeutics公司开发的一种名为LUXTURNA(voretigene neparvovec)基因疗法,应该在将来被批准用于一般使用。FDA 将在 1 月做出决定,一般来说,FDA 往往会遵循咨询委员会的意见。
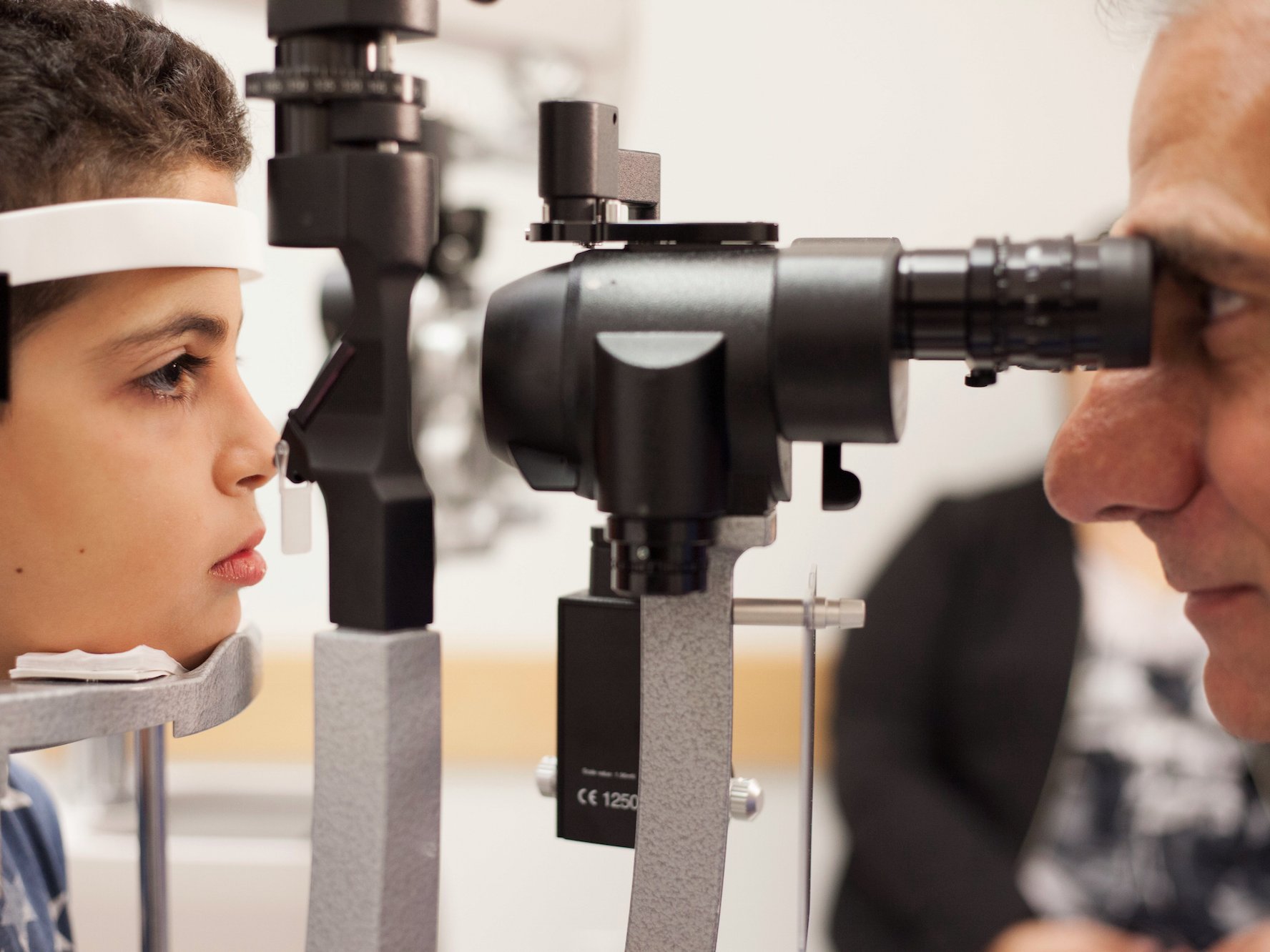
Luxturna 用来治疗莱伯氏先天性黑蒙症(Leber Congenital Amaurosis),这是遗传性的眼盲症,患者的 RPE65 基因具有缺陷,视网膜无法制造重要蛋白质,导致视力恶化。Luxturna能修复一种称为RPE65基因的突变,该基因负责告诉身体如何产生对正常视力至关重要的蛋白质。它通过快速注射到眼睛,将具有校正版本的基因的数十亿工程病毒颗粒引入视网膜细胞。
基因治疗通常使用工程化病毒来管理具有校正版本的错误基因的患者。而不是简单地回应有关条件的症状,它试图改变个人的遗传构成,以解决其根源的问题。
该公司估计,世界各地将有6000名患者可以从Luxturna中获益,其中包括美国的1000至2,000人。这些人中大多数人最终会完全丧失目前的视力,目前还没有为FDA批准的RPE65突变患者设计药物。

然而,Luxturna并不是没有缺点。这不是一个彻底的治疗方法,它不能给予接受者100%的保证。目前还没有关于其效果持续多久的数据,因此患者的视力有可能会随着时间的推移再次消失。
成本也是其可行性的主要因素。两名治疗最大的竞争对手Strimvelis和Kymriah分别花费了70万美元和475,000美元。因此,似乎Luxturna必须降低价格成为一个可行的竞争对手。由于Spark已经宣布计划制定一项计划,以帮助患者支付自付费用,例如前往Spark-proffering设施,他们可能会失去理由。
基因治疗有可能大大改善患有各种遗传疾病的人的生活质量。这种盛开的治疗方式可能是未来的浪潮。Luxturna则有望成为首款直接针对患者基因突变,真正做出“矫正”的基因疗法。

Spark的首席执行官Jeff Marrazzo 对麻省理工学院技术评论说: “这就是我认为,药物在20、30年后的模样,医学将会是如此。我认为这是从根本上改变医学的一个时代的开始。”
我们已经看到使用基因治疗从脑部疾病到骨骼破裂的项目。然而,这些治疗都将需要FDA批准 - 所以在这个领域工作的科学家可能会非常关注Luxturna今天的决定。