分享以前的一篇文章给大家。
维生素 C (VitC) 抗肿瘤的研究始于 70 年代,两届诺贝尔奖得主 Pauling 当时提出 VitC 可有效治疗癌症 ,虽然随后遭到学界的否定,但是 21 世纪以来,越来越多的临床研究证实大剂量 VitC 抗肿瘤方面的潜力。
我们团队从 2016 年首次开展「静脉输注大剂量 VitC (1g/kg) 联合射频局部深部热疗 (mEHT)治疗晚期非小细胞肺癌」的临床研究。研究成果发表在综合类期刊杂志 Journal of Advanced Research (影响因子:5.05) ,结果表明,静脉输注大剂量 VitC (1g/kg) 联合 mEHT 能够改善晚期非小细胞肺癌患者预后。

晚期 NSCLC 患者束手无策?老药 VitC 带来新希望
该 II 期临床研究共纳入 97 例 IIIB-IV 期非小细胞肺癌 (NSCLC) 患者,既往接受多种治疗手段,入组时已经无法手术,且对化疗、靶向治疗耐药或免疫治疗无反应。上述患者接受静脉输注大剂量 VitC (1g/kg) ,与 mEHT 同步治疗 25 次后,相比单纯最佳支持治疗组,显著改善其生活质量,能显著延长该类患者的无疾病进展生存期 (PFS) 与总生存期 (OS)(PFS: 3 个月比 1.85 个月;OS: 9.4 个月比 5.6 个月)(图 1) ,3 个月疾病控制率达 42.9% (单纯最佳支持治疗组为 16.7%) 。
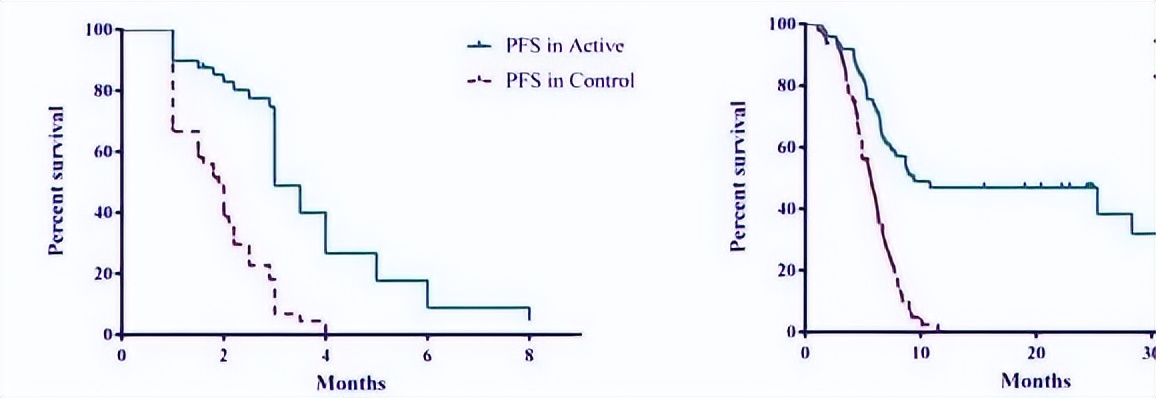
图 1. 大剂量 VitC(1.0g/kg)对 97 例 IIIB-IV 期 NSCLC 患者治疗效果的影响
晚期 NSCLC 患者生活质量明显下降,伴随而来的各种不适症状对他们的折磨更是雪上加霜。该研究应用 QLQ-C30 评分表对患者生活质量进行了评价,结果表明,随着病情进展,单纯最佳支持治疗组的患者症状越来越重,而大剂量 VitC 联合 mEHT 治疗的患者疲劳、恶心、疼痛、呼吸困难、食欲不振、便秘等症状均明显减轻。
配角组合,超高浓度 VitC 成为攻击癌细胞的关键
对于晚期 NSCLC 患者,由于分期较晚,已经丧失手术机会,化疗与分子靶向药物伴随而来的副作用常常令这部分晚期的肺癌患者无法完成整个治疗的疗程。区俊文团队开展的临床研究,旨在评估大剂量 VitC 联合 mEHT 对 IIIB-IV 期 NSCLC 患者生活质量的影响;并初步评价其对肿瘤的治疗效果。
mEHT 是利用射频电磁场作用于深部组织,产生热效应选择性破坏、*伤杀**病变细胞达到治疗目的,其特点是纳米范围的能量释放,其释放的能量利用效率可提升 3-4 倍。VitC 是人体必需的水溶性维生素,价格低廉,容易获得,高浓度使用安全性高,静脉输注大剂量 VitC 能够绕过肠道,产生的血药浓度比口服的血药浓度高数十倍。区俊文团队发现,大剂量 VitC 与 mEHT 同时结合使用时,能令体内 VitC 峰值浓度显著增加 [2],针对晚期肺癌患者体内 VitC 含量极度缺乏,这种「超高」浓度可能是 VitC 攻击癌细胞的关键。
该研究发现这两个配角的组合,能够显著改善晚期 NSCLC 生活质量,延长生存期,还有部分病例肿瘤病灶显著缩小,生存时间超过 5 年。而且,从分组来看,上述治疗方法对于腺癌和鳞癌的患者,EGFR (+)与 EGFR(-) 的患者相比,没有统计学差异,提示,上述治疗方法对于所有晚期肺癌患者疗效是相当的。这无疑对于晚期患者来说,多了一个治疗方案的选择,是一个福音。
延伸阅读
1. 区俊文团队关于大剂量 VitC 抗肿瘤人群研究的成果分享
(1)大剂量输注维生素 C 联合射频局部深部热疗治疗中国 III-IV 期非小细胞肺癌的安全性及药代动力学研究
(https://www.sciencedirect.com/science/article/abs/pii/S0928098717304554?via%3Dihub)
选取 35 例 NSCLC 患者,空腹状态检测血浆 VitC 浓度,并从该人群中选取符合入组标准的 15 例 III-IV 期患者,随机分为 3 组,分别静脉输注 1.0、1.2、1.5 g/kgVitC。第一组患者在 mEHT 结束时静脉输注 VitC (IVC) ;第二组患者同时进行 IVC 和 mEHT;第三组患者先行 IVC,结束后再行 mEHT。分别在单独应用 IVC 和联合 mEHT 应用时获得药代动力学曲线。该临床试验共进行 4 周,每周应用 3 次(隔天 1 次)。
结果表明 ,NSCLC 患者空腹血浆 VitC 水平显著低于正常人群,与疾病分期显著相关,且病理分期越晚,体内 VitC 浓度越低;静脉输注 VitC 两小时后体内达到血药浓度峰值,同时进行 IVC 和 mEHT 的处理组患者,VitC 的峰值浓度显著高于其他联合处理组或单独 IVC 处理组;患者未出现严重的不良反应,少数患者出现口渴症状,偶有患者感觉疲倦,仅有 1 例患者出现严重腹泻。 总体来看,大剂量 VitC 在肿瘤患者中的应用是很安全的。
(2)化疗联合静脉输注维生素 C 对晚期三阴性乳腺癌患者作用的回顾性研究
(https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7031790/)
对 2008 年 1 月 1 日至 2016 年 12 月 1 日在暨南大学附属祈福医院接受化疗的转移性三阴乳腺癌 (TNBC) 患者进行了回顾性研究,将符合入组标准的 70 例患者进行匹配后分为化疗组、静脉输注 VitC (IVC) + 化疗组。化疗组患者分别给予吉西他滨和卡铂进行治疗,IVC + 化疗组患者给予相同的化疗加 IVC 治疗。结果发现,IVC + 化疗组无疾病进展生存时间和总生存期分别为 7 个月和 27 个月,均显著高于对照组的 4.5 个月和 18 个月。并且治疗组不良反应发生率明显低于对照组。
2. 大剂量 VitC 抗肿瘤的机制研究
VitC 生理功能广泛,广为人知的是其抗氧化作用。然而,从 70 年*开代**始,有学者发现在大剂量静脉输注 (VitC 输注剂量在 0.5g/kg.d 以上) 的条件下,VitC 显示全新的作用机制。研究表明无论口服 VitC 的剂量有多大,体内血药浓度峰值均小于 0.3mmol/L,而 VitC 浓度超过 0.5mmol/L 才具有抗肿瘤活性。静脉输注大剂量 VitC 能够绕过肠道,产生血药浓度比口服高数十倍,这种 「超高」浓度的 VitC 是攻击癌细胞的关键 ,VitC 在分子结构上非常类似葡萄糖,其氧化形式脱氢抗坏血酸 (DHA) 可与葡萄糖竞争,通过葡萄糖转运蛋白 (GLUTs) 进入肿瘤细胞内。
(1)VitC 既是抗氧化剂,也是促氧化剂
目前研究认为大剂量 VitC 抗肿瘤作用机制与其在肿瘤细胞内的中间产物 H2O2 的累积有关。VitC 能选择性杀灭肿瘤细胞,其作用机制为:血液中过氧化氢酶和谷胱甘肽过氧化物酶能够有效抑制 VitC 分解;但 VitC 进入细胞外液 (包括细胞间隙) 后,没有上述两种酶,VitC 失去一个电荷阴性的电子,形成抗坏血酸自由基 (Asc-) ;这个活性电子还原一个蛋白质 - 核心金属离子,称之为过渡态金属 (如铁) ;
在此过程中,会形成具有高度活性的氧离子,再与细胞外液中的氢离子聚合产生 H2O2 进入细胞内,正常细胞中,H2O2 很快被清除,但多数癌细胞抗氧化酶活性较低,清除 H2O2 能力差。因此在一定浓度下 H2O2 只对肿瘤细胞有损伤,对正常细胞没有影响。同时,VitC 被氧化为 DHA,通过前述通道进入肿瘤细胞内,DHA 可消耗谷胱甘肽 (GSH) 被还原为 VitC,抑制磷酸甘油脱氢酶 (GAPDH) 活性从而阻止糖酵解反应,最终导致线粒体底物缺乏,造成 ATP 的耗尽,引起细胞死亡。
H2O2 可导致 DNA 单链断裂,DNA 修复酶 PARP 参与修复过程中,消耗大量 NAD + 来合成 ADP - 核糖聚合物,从而抑制 NADPH 活性。为维持 NADPH 在细胞内的浓度,糖酵解途径被抑制,戊糖磷酸途径 (PPP) 代谢增加。此外,H2O2 会损伤肿瘤细胞的线粒体,直接抑制 ATP 合成,导致肿瘤细胞因能量衰竭死亡。
目前不少研究支持大剂量 VitC 的代谢中间产物 H2O2 是其抗肿瘤的重要机制,但有学者认为,具有低水平过氧化氢酶 (CAT) 的肿瘤对大剂量 VitC 治疗敏感,而 CAT 水平较高的肿瘤可能不敏感。
(2)VitC 通过促进 DNA 去甲基化改变基因控制
表观遗传学改变是指基于非基因序列改变所致基因表达水平变化,如 DNA 甲基化和组蛋白修饰等。所谓 DNA 甲基化是指在 DNA 甲基化转移酶的作用下,将 S - 腺苷甲硫氨酸提供的甲基基团共价结合到 CpG 二核苷酸的胞嘧啶 5 碳位上的过程,目前 CpG 岛异常高甲基化所致抑癌基因转录失活成为肿瘤研究中的热点问题。肿瘤中 DNA 高甲基化模式多来自 DNA 甲基转移功能获得和 10-11 易位蛋白 (TET) 的功能丧失。
TET 能够改变甲基基团的分子结构,促使基团从胞嘧啶上脱离,从而发挥其 DNA 的去甲基化作用。VitC 作为辅助因子,通过向 Fe3+ 提供电子以产生 Fe2+,增强 TET 蛋白的活性,促进 DNA 去甲基化,促使抑癌基因的重新表达和干细胞分化。研究表明,Tet 的失活突变和白血病的发生有关,当 Tet 突变和其他突变同时出现时,就会增加造血干细胞的活性和自我更新,诱发白血病,而 VitC 可通过对 Tet2 基因表达产生影响从而调节血液形成血液干细胞的数量和功能。
组蛋白修饰也是表观遗传学重要的调控机制之一,参与调控基因表达等多种生物学过程中。组蛋白去甲基化酶可移除组蛋白中精氨酸和赖氨酸上的甲基,依赖于 Jumonji-C 结构域的铁离子 -α- 酮戊二酸依赖的双氧合酶。类似 TET 蛋白,VitC 氧化还原活性铁,可增强 Jumonji 家族蛋白的去甲基化作用。研究证实 VitC、Tet 和 DNA 甲基化调控之间的直接联系,并证明了 VitC 可以调控 DNA 甲基化。
(3)VitC 能增强免疫细胞的活性
VitC 对维护免疫细胞的功能至关重要,长期缺乏会导致免疫功能受损。有学者建立乳腺癌、结直肠癌、黑色素瘤和胰腺癌小鼠模型,结果发现功能完整的免疫系统可充分发挥 VitC 的抗肿瘤作用。研究发现,VitC 可增加 CD8+ T 细胞的 5 - 羟甲基胞嘧啶水平,对淋巴瘤细胞的毒性增加了 380%[11]。大剂量 VitC 还通过免疫细胞调节肿瘤微环境的浸润,显著增加瘤内 CD8+ T 细胞和巨噬细胞的浸润,增强肿瘤免疫识别能力,并能协同免疫检查点治疗发挥抗肿瘤的作用。