作者:赵堂堂1,肖瑞琳1,2,王丽丽3,常冰梅1
单位:1山西医科大学基础医学院生物化学与分子生物学教研室
2太原理工大学安全与应急管理工程学院
3山西医科大学第一医院麻醉科
结直肠癌(CRC)是常见的恶性肿瘤之一,严重威胁人类生命健康。脂质代谢异常与CRC的发生发展关系密切,但其机制并未完全阐明。脂质包括脂肪(即甘油三酯)和类脂(包括磷脂、胆固醇、鞘脂等),是细胞重要的营养物质之一,参与多种代谢以及信号转导过程[1]。CRC中各种脂质成分的重编程对CRC的凋亡、转移等具有重要意义。本文围绕CRC中脂代谢重编程、肿瘤微环境、肠道微生物群发生的脂代谢改变及其他调控机制研究进展进行综述,为阐明CRC的机制提供理论依据。

1.脂代谢重编程对CRC生物学行为的影响
1.1CRC中脂肪酸的异常
脂肪酸(FAs)的结构通式为CH3(CH2)COOH,作为最简单的一种脂质,是复杂脂质(如脂肪、磷脂、糖脂)的组成部分。CRC细胞中FAs的合成、延长、氧化和去饱和等代谢途径均发生了异常的改变。研究发现,经雷帕霉素激酶(mTOR)信号通路诱导,脂肪酸合成酶(FASN)过度表达,脂肪酸合成增多,进而脂肪合成增多,为癌细胞增殖提供充足的能量。
在CRC中极长链脂肪酸的血清含量明显升高,而长链脂肪酸水平显著降低,说明CRC的发生发展过程中可能存在FAs的延长变化。此外,癌变还与氧化应激有关,增强的脂肪酸氧化(FAO)比*酮丙**酸的氧化能更快产生ATP,以和癌细胞扩散的速度相匹配,来维持CRC细胞的合成代谢,这种作用是为了适应细胞外的酸化环境。多不饱和脂肪酸的相对减少和饱和脂肪酸的增加可导致活性氧减少,增强细胞活性,促进CRC发生发展,从而在脂质相关的重编程中扮演关键角色。
1.2CRC中其他脂质成分的改变
CRC中其他脂质成分代谢也会发生改变。研究表明,与未转化的细胞相比,癌细胞中胆固醇合成增加。细胞质中的溶酶体胆固醇可通过肠道胆固醇转运关键蛋白(NPC1L1)信号复合物激活mTORC1,进而导致癌细胞增殖、侵袭和转移增加。另外,作为脂质成分的重要组成之一,鞘脂(SLs)在CRC细胞中的水平也发生改变。1-磷酸鞘氨醇/神经酰胺(S1P/Cer)比率变化是CRC中SL代谢改变的显著特征。Cer增加导致CRC细胞的凋亡和自噬激活,抑制细胞增殖和CRC发展。
CRC细胞表现出异常的脂质代谢,主要表现为脂肪合成增多(包括从头脂肪酸合成和甘油三酯合成增多)、脂质的摄取和含量增加,以及对FAs的普遍依赖增强。与健康组织相比,肿瘤中总脂质含量的变化、脂滴(LDs)中三酰甘油和胆固醇储存的改变以及编码脂肪生成相关酶基因的差异表达证明了CRC细胞脂代谢异常(图1中总结了CRC中脂肪酸代谢相关过程)。因此,CRC细胞中异常脂代谢将影响许多过程,如凋亡、自噬、坏死、增殖、分化等,从而驱动肿瘤的发生和发展,对CRC的发展和不良预后具有重要意义。

2.脂代谢异常对肿瘤微环境的影响
肿瘤微环境(TME)由免疫细胞、脂肪细胞、癌症相关成纤维细胞、内皮细胞等组成。TME成分和癌细胞相互作用,最终导致肿瘤的增殖、侵袭和转移。一方面,癌细胞生长需要大量的能量,因此它们与邻近细胞竞争养分,营养耗尽通常会驱使其他细胞转向不同的代谢程序或者阻碍其正常调节;另一方面,TME中分泌的代谢物可以影响周围细胞类型的功能和表型,导致TME中各细胞增殖或活化减少。这些事件有助于CRC发展,使其逃避免疫监测。
2.1免疫细胞
脂质代谢与肿瘤微环境中的免疫细胞有密切关系。在CRC中,巨噬细胞、树突状细胞、淋巴细胞、自然*伤杀**细胞(NKs)都存在上调脂肪酸合成、FAO增加。来自术后CRC患者的NK细胞也表现出CD36和脂质水平升高。组织常驻记忆T细胞和调节T细胞(Treg)表现出对外源FAs摄取效应增强,FAs在线粒体中被氧化以产生足够的能量。基础脂质摄取受损或进一步的分解代谢过程会阻碍Treg的分化和存活,甚至导致向其他T细胞表型转变,如辅助性T细胞17。总之,这些研究证明,癌症和免疫细胞之间的相互作用导致双方的脂质代谢重编程,从而影响CRC的进展。
2.2脂肪细胞
CRC通常会侵入周围的脂肪组织,并与邻近的脂肪细胞建立密切联系。癌细胞暴露于脂肪细胞,导致癌细胞中肉碱棕榈酰转移酶和FAO的表达上调,有利于促进Wnt信号转导和癌症干细胞特性。这是由于脂肪细胞通过提供FAs支持癌细胞在缺乏营养的情况下存活。脂肪细胞或FAs的存在也促进了CRC细胞的自噬,有助于促进脂肪细胞的生长。
2.3其他细胞
成纤维细胞存在于结缔组织中,并产生包括胶原蛋白在内的细胞外基质成分。在病理条件下,癌细胞分泌的因子可以激活并影响其功能。癌症相关成纤维细胞(cancer associated fibroblasts,CAF)的特点是具有明显的代谢物异质性,并在各类癌症中表现出不同的表型[26]。代谢压力可以对CAF进行重编程,以创造一个营养丰富的环境来支持肿瘤生长。研究表明,脂质代谢的重编程和CAFs中FASN酶表达增加导致脂质产生增多,促进CRC细胞迁移[27]。内皮细胞中的脂质代谢尚未充分阐明,内皮细胞将脂质转运至其他细胞类型,CD36在这一过程中起重要作用,CD36缺失导致实质细胞对FA的摄取失控。且内皮细胞在生理条件下不增殖,但在肿瘤新生血管形成过程中会转变为增殖和迁移状态。
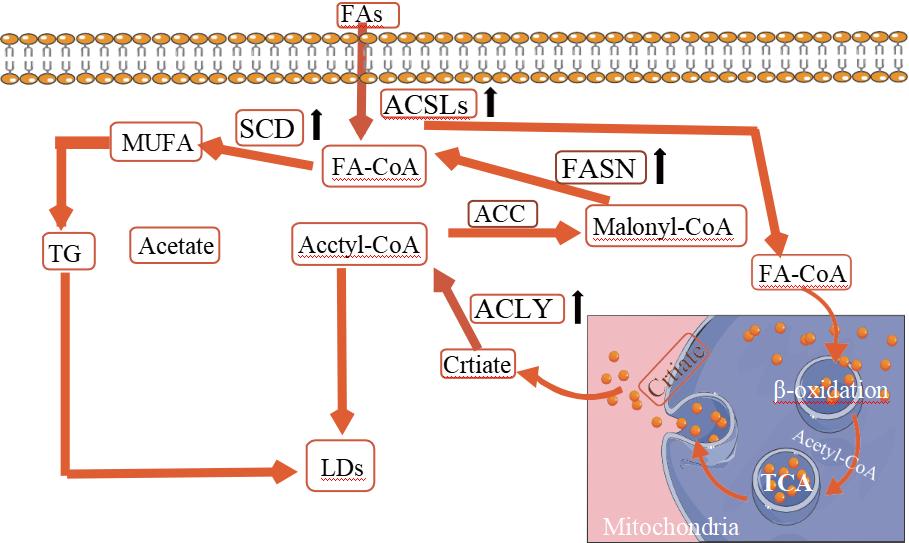
图1 CRC中脂肪酸(FAs)代谢相关过程
3.肠道菌群代谢物对CRC中异常脂代谢的影响
结直肠中具有多样的微生物群,参与体内平衡的维持和疾病的进展。细菌和代谢物之间相互作用,能使结肠上皮细胞和免疫细胞的功能维持平衡。因此,生态失调和由此导致的肠道微生物群代谢物与CRC的发展和转移有关。此外,微生物群还可以通过它们的代谢产物——包括短链脂肪酸(SCFAs)、脂多糖等修饰TME,同时影响肿瘤免疫抑制治疗。本节主要针对CRC中肠道菌群代谢物丁酸盐、胆汁酸及其衍生物与异常脂代谢的联系进行综述。
3.1肠道菌群代谢物丁酸盐与脂代谢异常
细菌产生的短链脂肪酸丁酸盐为结肠细胞提供了主要的能量来源,并显示出抗炎和免疫调节特性。丁酸是碳水化合物的发酵产物,可由某些种类的杆菌(如具核梭杆菌)产生。在正常结肠细胞中,它作为能量来源,在Krebs循环中代谢为乙酰辅酶A,可促进正常结肠上皮细胞的增殖。CRC细胞中丁酸盐积累并可作为组蛋白脱乙酰酶(HDAC)的*制剂抑**。在CRC中,丁酸不进入Krebs循环并累积进入细胞核,通过HDAC抑制调节基因的表达,抑制细胞增殖。通过丁酸盐介导的持续利用谷氨酰胺和脂肪酸分解作用,可促进氧化磷酸化,使SCFAs增强CD8+T细胞的细胞毒性和记忆潜力。
3.2胆汁酸及其衍生物与脂代谢异常
胆汁酸及其衍生物构成了另一组重要的脂质代谢物。一小部分初级胆汁酸如胆酸或鹅脱氧胆酸可逃脱重吸收,进入结肠,经某些微生物群介导,恶性转化为次级胆汁如脱氧胆酸(DCA)和石胆酸。DCA能够激活内皮生长因子EGF与其受体EGFR途径和下游激活蛋白1反应,诱导CRC细胞增殖,参与了CRC的发生发展。
4.其他调控机制的研究进展
4.1MiRNAs对异常脂代谢的调控作用
MiRNAs常可作用于脂质代谢中的调节因子,影响CRC细胞的增殖和发展。研究发现,脂肪酸酰基辅酶a合成酶的亚型之一ACLS5在CRC中表达,并受miRNA调节。MiR-497-5p可以靶向长链脂酰CoA合成酶(ACSL)5-3′UTR,并降低其在CRC中的表达,使CRC细胞中脂肪酸不能正常合成酰基辅酶a,导致β-氧化异常,抑制CRC的发展,减少CRC从脂质代谢中获得的能量。MiR-27a作为肉碱棕榈酰转移酶-1和酰基辅酶a脱氢酶9的潜在靶点,可以调节CRC中的脂质代谢,影响CRC的侵袭性和耐药性。
4.2信号通路异常对脂质成分的影响
CRC涉及Wnt、P13K/AKT、p53等多种信号突变累积。Wnt信号异常被认为是CRC发生的主要引信,β-catenin是其核心组分。Wnt/β-catenin可通过c-Myc参与体内脂肪生成,诱导甘油三酯中的磷脂合成,导致不饱和脂肪酸与饱和脂肪酸比例增加。PI3K/AKT是人类癌症中突变率最高的网络,异常的PI3K/AKT信号改变在CRC中也常可见到。异常PI3K/AKT信号可通过直接磷酸化和激活ATP-柠檬酸裂合酶(ACLY)诱导脂肪生成,并增加细胞质中乙酰辅酶a的含量,提高脂代谢水平,为癌细胞供能。大多数癌症包括CRC,都可发生TP53基因突变,导致p53通路异常。而p53相关通路在控制细胞周期、凋亡和衰老中有关键作用。也有研究表明,p53也可通过调控参与脂肪酸合成的一些关键基因(如FASN基因)的表达,通过调节脂代谢过程抑制肿瘤发展。
4.3脂代谢重编程相关基因突变
CRC进程中也伴随着某些脂代谢相关基因的改变,如脂代谢相关基因CGI-58[44],CGI-58主要通过激活甘油三脂水解酶参与脂质水解。在CRC中可出现特征性CGI-58缺失现象,CGI-58缺失的肠道上皮细胞抑制脂肪酸线粒体氧化,酯酶水解活性下降,使细胞内中性脂质沉积。CGI-58缺失也与CRC的分期、分级、转移及复发率呈显著正相关,与CRC患者的预后呈负相关。CGI-58缺失还可上调Wnt通路靶基因c-MET、诱导YAP/TAZ核转位激活Wnt信号通路,促进细胞恶变和侵袭。其他脂代谢相关基因如ABHD5缺失可降低正常结肠上皮细胞和腺瘤细胞自噬水平、损伤DNA修复、基因组稳定性,从而促进CRC发生发展。
5.小结与展望
结直肠癌的发生发展过程中会出现十分复杂的调控机制,包括脂代谢重编程、肿瘤微环境、肠道微生物群代谢物等。在CRC发生发展过程中,CRC细胞会重新建立脂质代谢,如脂肪酸合成、FA摄取或细胞内脂质积累及相关基因表达上调等,以供自身完成生长、增殖、侵袭等一系列活动。
TME中的成分如免疫细胞上调脂质代谢支撑其免疫活性,CAFs和脂肪细胞通过分泌FAs供应CRC细胞的代谢需求,导致其侵袭和转移。肠道菌群的脂类代谢物丁酸盐的累积或胆汁酸等的变化也参与CRC发生发展。对CRC细胞重编程的代谢途径进行干预或可有效抑制CRC的发展,但目前尚无针对CRC的脂质靶向疗法。随着对CRC及脂质代谢相关研究的深入,异常的代谢调控机制将进一步被阐明,这将为深入了解CRC中复杂的细胞通讯和脂质代谢相互作用提供新的见解;并为扩展CRC分子生物学靶标,开发新型诊断技术,完善CRC临床诊疗策略,以及疾病的预防、诊断、治疗和预后提供完整可信的理论依据。
整理自:生命的化学,2022,42(6):1083-1088