编者按:根据日本PARADIGM试验 (摘要号LBA1) 结果,帕尼单抗是左侧RAS野生型转移性结直肠癌(mCRC)患者首选的靶向治疗,与VEGF*制剂抑**相比,该EGFR*制剂抑**与FOLFOX联合可带来3.6个月的中位总生存期(OS)优势,同时也是一线mCRC前瞻性3期试验中报告的最长OS持续时间。日本国立癌症中心东医院的Takayuki Yoshino教授在2022年ASCO年会的全体会议上介绍了这些数据。

Takayuki Yoshino 教授
意大利比萨大学的医学博士Chiara Cremolini 对PARADIGM研究进行了点评,“该前瞻性研究证实了在左侧RAS野生型原发性肿瘤患者中,FOLFOX联合帕尼单抗与FOLFOX联合贝伐单抗相比,在OS和客观反应方面的获益,且转化为更高的二次R0切除率,另一方面,RAS 野生型肿瘤患者的常规前期治疗无法抵消右侧肿瘤的不良预后。FOLFOX联合帕尼单抗和 FOLFOX联合贝伐单抗在OS方面的结果非常令人失望。”

Chiara Cremolini 博士
对于患有RAS野生型疾病的患者,VEGF*制剂抑**贝伐单抗和EGFR*制剂抑**帕尼单抗和西妥昔单抗都是在一线环境中与双药化疗联合使用的推荐选择。然而,可用于帮助区分靶向治疗的头对头数据很少,特别是在肿瘤偏侧的情况下,可能会根据各种临床病理学特征显著影响对治疗的反应。这可能是因为对抗EGFR药物的内在耐药性相关基因组和表型特征在右侧肿瘤中更为普遍,包括RAS和BRAF的突变,以及MAPK和PI3K/PTEN/AKT信号通路的其他改变。
尽管有几项回顾性分析表明,在具有野生型RAS的左侧mCRC的一线治疗中,抗EGFR治疗优于VEGF治疗,但由于缺乏前瞻性数据,贝伐单抗继续广泛用于该人群。PARADIGM数据清楚地回答了这个问题。Takayuki Yoshino教授表示,这项试验表明,对于RAS野生型的左侧mCRC,一线靶向药物与化疗的选择确实很重要,并且帕尼单抗与FOLFOX的一线治疗优于贝伐单抗和FOLFOX 化疗。PARADIGM结果强调了RAS检测在左侧转移性CRC初步诊断中的重要性,且需根据检测结果选择初始治疗方案。
PARADIGM研究结果
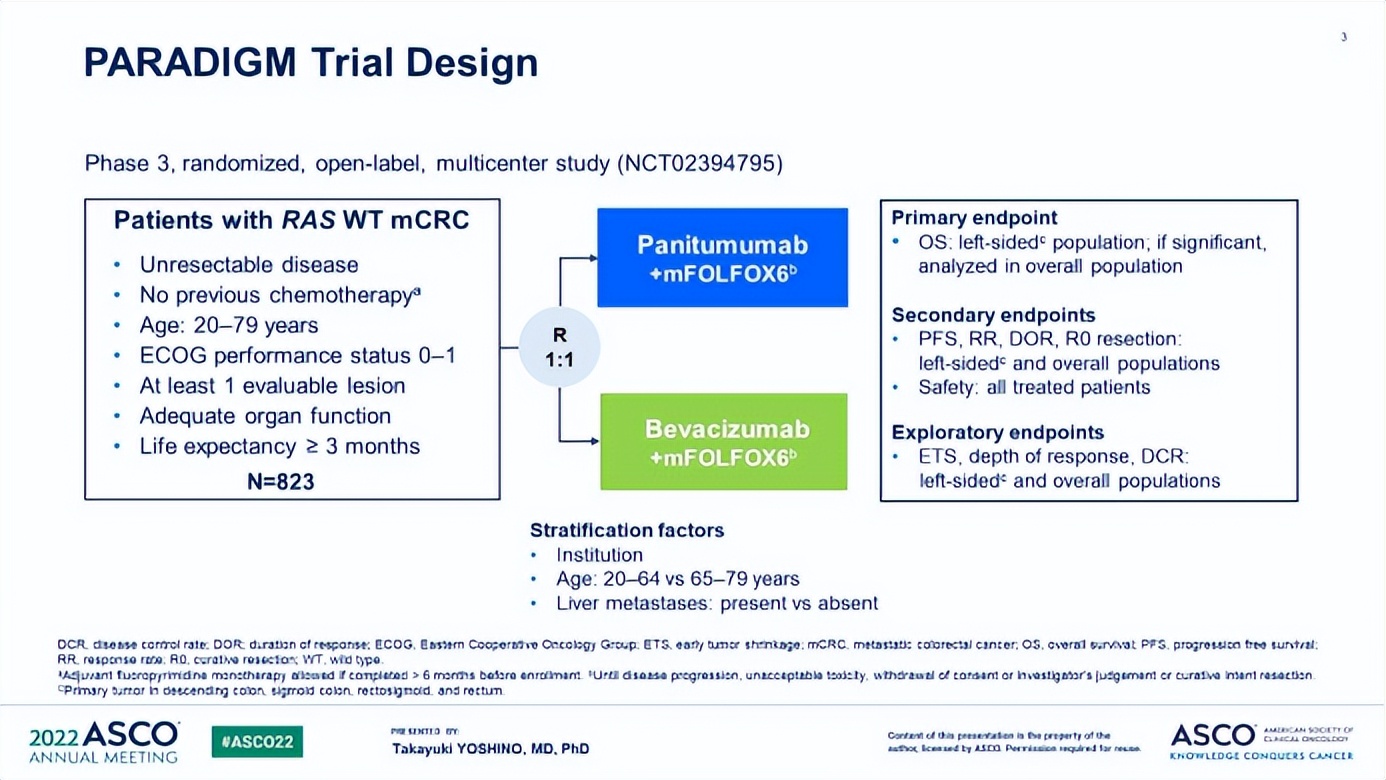
图1 PARADIGM研究设计
PARADIGM主要纳入823例RAS野生型mCRC 患者,重点关注左侧亚组人群的OS。在整个患者组中,就OS获益而言,结果也显著支持帕尼单抗优于贝伐单抗(中位数36.2个月 vs 31.3个月;HR 0.84, 95% CI [0.72, 0.98];P = 0.030)。然而,这种差异似乎是由左侧人群驱动的,因为在探索性分析中右侧肿瘤患者的OS没有显着改善(中位数20.2个月对23.2个月;HR 1.09, 95% CI [0.79, 1.51])。

图2 左侧和总体人口的OS
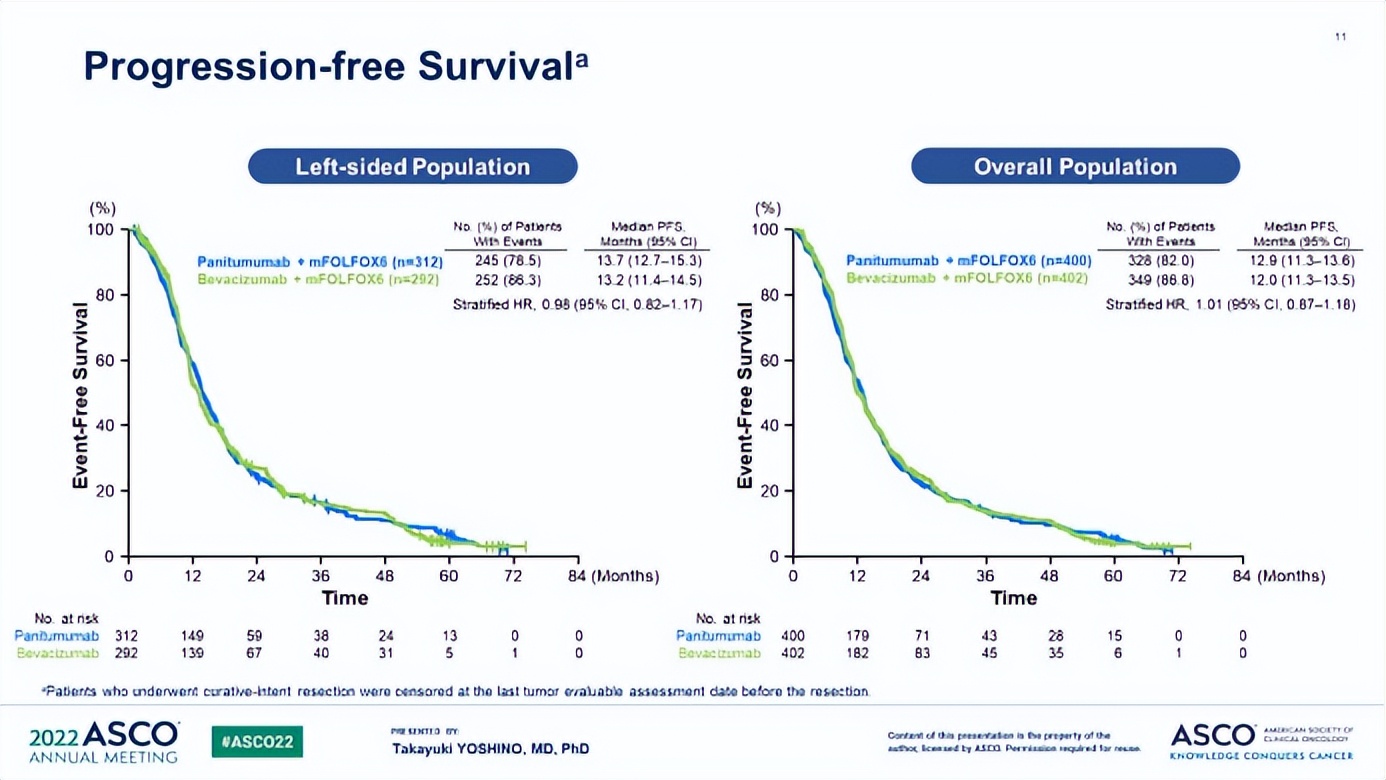
图3 左侧和总体人口的PFS

图4 右侧人群的OS和亚组分析

图5 帕尼单抗和贝伐单抗组的安全性
左侧疾病亚组的其他结果显示,帕尼单抗和贝伐单抗组的中位无进展生存期相当(13.7个月 vs 13.2个月;HR 0.98, 95% CI [0.82, 1.17])。相比之下,帕尼单抗的客观缓解率(80.2% vs 68.6%)和R0切除率(18.3% vs 11.6%)均明显高于贝伐单抗,中位缓解持续时间(13.1 vs 11.2个月)。安全性方面,正如预期的那样,帕尼单抗比贝伐单抗产生更多的皮肤、指甲和粘膜毒性(如*疮痤**样皮炎、口腔炎、甲沟炎和皮肤干燥)。这些毒性通常与EGFR*制剂抑**有关。
应根据患者分层情况选择合适的一线治疗
Cremolini 博士同样认为这些结果支持选择FOLFOX联合帕尼单抗作为左侧RAS野生型 mCRC患者的初始治疗。然而,她认为这个亚组应该更明确地定义为左侧、微卫星稳定、RAS和BRAF野生型mCRC 患者,因为检查点*制剂抑**是微卫星不稳定肿瘤的首选。此外,在激活BRAF突变的情况下,EGFR*制剂抑**与化疗联合使用的效果有限。
在其他治疗选择方面,鉴于缺乏前瞻性的头对头比较,目前尚不清楚化疗双药联合EGFR药物是否比三药联合(即FOLFOXIRI)贝伐单抗更有优势。对于右侧肿瘤而言,FOLFOXIRI联合贝伐单抗是首选的一线治疗方案,该领域正在等待支持在早期治疗中使用靶向治疗的数据。
鉴于PARADIGM试验是在日本进行的,一些人可能会质疑这些数据是否适用于非亚洲患者群体。Yoshino教授反驳了这个疑问。“就疗效而言,日本和非日本患者之间没有显著差异,这在之前的研究中已经证明,在欧洲进行的比较西妥昔单抗与贝伐单抗联合FOLFIRI 的FIRE-3试验显示了与PARADIGM相似的结果,并且帕尼单抗的药代动力学分析发现日本人和非日本人之间没有显着差异。”
未来进一步研究方向
在下一步方面,Yoshino教授及其同事正在以PARADIGM数据为基础,对治疗前后收集的肿瘤活检和循环肿瘤 DNA样本进行生物标志物分析 (NCT02394834),他们的目标是确定每种靶向治疗的预测性生物标志物,并了解每种治疗方案的耐药机制。他表示,“我相信,基于这种全面的分子分析,可以更精确地选择抗EGFR敏感肿瘤患者,这可能导致OS曲线比我们在左侧RAS野生型mCRC亚组中观察到的更早、更清晰的分离。”
参考文献:
1.Heinemann V, von Weikersthal LF, Decker T, et al. FOLFIRI plus cetuximab or bevacizumab for advanced colorectal cancer: final survival and per-protocol analysis of FIRE-3, a randomised clinical trial.?Br J Cancer. 2021;124(3):587-594.;124(3):587-594.