
文章来源:王晓琳,饶本强,江波,石汉平.生酮饮食联合疗法治疗恶性肿瘤研究进展.肿瘤代谢与营养电子杂志2016,4(3):255-260
正文
肿瘤细胞一个突出的代谢特点是葡萄糖摄取量和乳酸积累量逐渐升高,利用糖酵解作为主要能量代谢来源,获得更高的糖酵解能力,使得葡萄糖转变为乳酸产生ATP,这种现象我们称为Warburg效应[1]。葡萄糖糖酵解途径依赖和细胞内高浓度乳酸积累是Warburg效应的两个主要特征,与肿瘤细胞的攻击性和侵袭性具有显著关联[2-5]。超过90%的肿瘤患者死亡原因是肿瘤细胞转移或者从原位扩散至远端组织。目前没有更好的治疗方法可以有效控制肿瘤细胞全身性转移。由于肿瘤细胞的转移性是一个突出表型,以肿瘤代谢为主要靶点进行纠正或干预的肿瘤代谢疗法可能会为侵袭性或晚期肿瘤患者提供新的治疗方法。研究显示,生酮饮食(ketogenic diet,KD)联合酮酯(ketone ester,KE)--外源性酮体、高压氧治疗(hyperbaric oxygen therapy,HBOT)、能量限制(calorie restriction,CR)、运动、维生素D及二甲双胍等治疗肿瘤将会取得更好疗效。
1 生酮饮食与酮体
与Warburg效应相关的糖酵解依赖促使研究人员探究通过饮食疗法降低肿瘤可用的糖。虽然KD的抗肿瘤作用主要是由于减少糖酵解底物和抑制胰岛素样生长因子-1(insulin-like growth factor-1,IGF-1)信号转导,但新的证据表明,酮体本身已具有治疗肿瘤的潜力[6-8]。正常细胞较易适应将酮体作为一种高效能代谢物,但许多肿瘤细胞不具有这种适应性[9, 10]。与正常组织相比,恶性肿瘤细胞利用酮体酶的表达较正常细胞减少[11, 12]。例如,与健康神经元相比,酮体无法缓解葡萄糖缺乏导致的神经胶质瘤细胞死亡[13]。最近,研究人员在转移性肿瘤小鼠模型上发现,直接补充KE可以抑制肿瘤生长。结果表明,即使应用高碳水化合物饮食,KE的补充在体内也会具有有效的抗肿瘤作用。同样,在体外应用高葡萄糖培养基培养肿瘤细胞加入KE也存在类似效果[7]。有研究证明了一种新的代谢组合疗法--KD+KE+HBOT在侵袭性转移瘤小鼠模型上具有明显抗肿瘤效果,该转移表型模型在很多人类侵袭性肿瘤中也可看到[14-17]。体内研究中,单独应用这些疗法可抑制肿瘤的增殖和活力,减缓肿瘤进展 ;联合应用时,通过抑制肿瘤细胞全身性转移扩散,使转移性肿瘤小鼠存活时间比对照组明显延长。前期研究证明,KD+KE+HBOT组合对转移性肿瘤小鼠的抗瘤作用显著,可减缓转移性荷瘤小鼠的发展[7, 18],见图1。结果显示,组合这些治疗方案可以提供更显著的抗肿瘤效果。

2 生酮饮食与高压氧
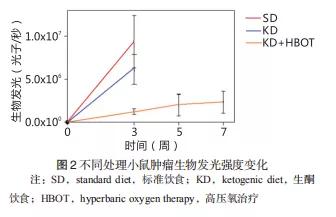
细胞的能量代谢常常受到组织供氧影响而进行复杂的代谢调节[19, 20] :当氧充足时,正常细胞产生的高达90%三磷酸腺苷来自于线粒体呼吸;当氧有限时,如运动中的肌肉,细胞通过葡萄糖酵解产生ATP。这种代谢的转换可维持细胞功能,并在短暂缺氧时提高存活率,其作用机制在很大程度上是由细胞内的一种转录因子--缺氧诱导因子-1(hypoxia inducible factor-1,HIF-1)驱动的[20, 21]。HIF-1转录因子可提高60多个基因的表达,其中包括许多参与糖酵解、血管生成、细胞生长和存活的基因[20, 22]。HIF-1异常表达时,使肿瘤生成许多不成熟及有缺陷的血管,使血液无法充分灌注整个肿瘤组织[25]。这导致肿瘤缺氧区域内Warburg效应增强并且促进肿瘤的发展、侵袭和转移[23-25],因此肿瘤组织氧供应、HIF-1信号与肿瘤的侵袭和预后是密切相关的[26]。肿瘤缺氧还会介导其对放化疗的抵抗[27-30]。因为这些疗法在很大程度上是通过刺激肿瘤内的活性氧簇(reactive oxygen species,ROS)来发挥作用的,肿瘤局部有限的氧供可以减弱肿瘤治疗效果[31, 32]。HBOT应用的是高压下100%的氧气。在体内,高压氧使血浆中的氧饱和,并进一步扩散到组织和缺氧的肿瘤区域[33-35]。体外研究中,高压氧同样可将氧扩散到培养中的细胞内,因而,HBOT对肿瘤细胞的效果可在体外培养环境进行评价。结果显示,HBOT可抑制肿瘤血管生成和肿瘤生长并可增加多种细胞、组织、动物和患者存活时间,可作为抗肿瘤的独立或辅助治疗方法[36-42]。研究显示,KD联合HBOT是转移性肿瘤一种有效的联合治疗方式[18]。有研究采用荧光素酶标记的转移瘤VM-M3小鼠模型来比较标准饮食(standard diet,SD)、KD单独或KD联合HBOT处理后肿瘤进展和小鼠生存状况。瘤体生长通过小鼠体内生物发光成像进行监测。结果显示,KD组血糖显著降低,肿瘤生长延缓,平均生存时间与对照组相比增加56.7%;HBOT本身并不能影响肿瘤的发展,KD与HBOT联合应用才能引起血液中的葡萄糖水平以及肿瘤生长速率的显著下降,与对照组相比,平均存活时间增加77.9%。在转移瘤模型研究中,KD和HBOT联合治疗可产生显著的抗肿瘤作用[43],见图2。组合这些无毒的治疗方法可发挥更强的协同抗肿瘤作用。这些疗法可作为全身转移性肿瘤患者潜在的无毒治疗或辅助治疗,值得进一步研究。
3 生酮饮食与能量限制
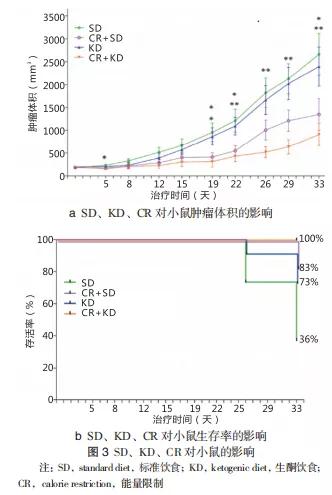
CR是一种受控制的治疗性禁食,减少了身体的氧化压力,同时促进更有效率的能量代谢。CR和KD的治疗潜力已在临床尤其是多种神经系统疾病动物模型中得到反复证实,其基本机制涉及线粒体功能改善、细胞凋亡因子表达减少和神经营养因子活性增加。最新证据表明,通过每天减少能量摄入或间歇性禁食,不仅对于癫痫,可能对许多急性和慢性神经系统疾病均具有神经保护作用[44]。中枢神经系统肿瘤前期临床数据表明,CR和(或)KD可成为肿瘤治疗的一个潜在辅助方法[45-48],这是通过采用CR+KD支持治疗的两个病例报告得出的结论[49, 50]。奥地利Paracelsus医科大学的Morscher RJ等[51]研究了神经母细胞瘤异种移植瘤模型限制能量摄入后肿瘤生长和CD1缺失小鼠生存时间的变化。研究发现,CR+KD组小鼠移植瘤体积较其他组小,生存时间较其他组长[51],见图 3。针对神经母细胞瘤的代谢特性,可以研究在标准治疗方案基础上结合代谢调节治疗新方法。推测,CR和KD的联合应用对于神经母细胞瘤的患者可能起到更好的辅助治疗作用。
4 生酮饮食与运动
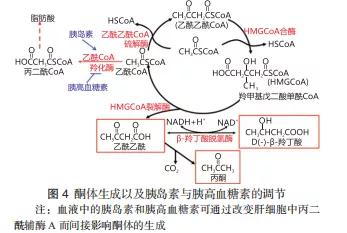
酮体合成速率是靠游离脂肪酸进入线粒体速率调节的。游离脂肪酸进入肝细胞线粒体是由肉*碱毒**脂酰转移酶Ⅰ(carnitine acyl-transferase I,CAT I)所催化的生化过程。胰岛素能激活乙酰辅酶A羧化酶(Acetyl-CoA carboxylase,ACCase)的活性,而胰高血糖素则抑制该酶的活性。ACCase催化乙酰辅酶A和HCO- 3合成丙二酰辅酶A,后者可以进一步合成脂肪酸。所以,运动中和运动后血液中胰岛素和胰高血糖素含量的改变可通过改变肝细胞中丙二酰辅酶A而间接影响酮体的生成[52],见图4。Koeslag JH[53]认为,正常人血液中酮体浓度相对恒定,但在长时间运动状态下,就会使酮体的生成超过其被利用的限度,造成血液中酮体水平升高[53]。在运动恢复阶段,大多数生理、生化指标都会迅速恢复至正常水平,而血液中酮体浓度却会不断上升。酮体在运动结束后依然会保持在较高水平。在高蛋白和高脂肪膳食后运动 , 尿中酮体含量增多;反之,在高糖膳食后运动,尿中不出现酮体或只有少量酮体[52]。因此,我们可以考虑利用这种现象,辅助KD来达到治疗效果。
5 生酮饮食与维生素
DKD是肿瘤患者营养治疗途径之一,得到了广泛的应用[54],肿瘤患者希望能通过遵循这种饮食方式,作为减少肿瘤生长和具有最大限度抗瘤潜力的方法。KD的一个共同点是碳水化合物供能的限制以及脂肪供能的增加。在地中海国家,脂肪类能量的重要来源是橄榄油,许多研究表明,脂肪供能对肿瘤治疗是有益的[55-59]。然而,KD的一个主要副作用是维生素D摄入不足,第一次观察到这个副作用是在应用KD治疗儿童癫痫时发现的[60, 61]。意大利佛罗伦萨大学的Branca JJ等[62]研究了一例高剂量维生素D联合KD导致乳腺癌生物标志物的变化。该患者在诊断和手术之间的三个星期,没有应用其他治疗计划,仅为患者提供高剂量口服维生素D(10000 IU/ 天),并严格遵循KD。术后分析手术标本显示,HER2的表达阴性,并且PGR显著增加(20%)。ER和Ki67阳性没有改变。研究表明,高剂量维生素D联合KD可导致乳腺癌生物标志物的变化。在应用KD时联合应用维生素D以增加血清中维生素D的代谢水平,其与乳腺癌的风险降低密切相关。因此,可以推测,开始应用KD干预肿瘤患者时,可以补充维生素D来平衡和抵消KD的不足,同时受益于维生素D在肿瘤管理中的作用,包括联合应用下调乳腺癌HER2表达,见表1。

6 生酮饮食与二甲双胍
最近的研究表明,肿瘤的代谢产物--乳酸可能是许多器官,包括脑组织的一种有效替代葡萄糖的能量来源[63]。因此,宿主组织可将肿瘤组织葡萄糖酵解的最终产物--乳酸作为替代能源。乳酸和酮体联合应用可以充分防止早期文献提出的患者因KD引起的低血糖[64-66]。KD帮助我们控制组织内局部葡萄糖水平,也可以控制和减缓肿瘤细胞糖酵解和核糖供给速度,而这在快速生长的肿瘤细胞中是必不可少的。由于体内的葡萄糖还可来自于肝、肾糖异生作用,因而抑制肿瘤细胞生长还需要糖异生*制剂抑**的应用。二甲双胍可以利用肝细胞G蛋白恢复胰岛素对腺苷酸环化酶的抑制,减少肝的糖异生,降低肝糖输出以降低空腹血糖;抑制葡萄糖在肠道的吸收,以降低餐后血糖;抑制脂肪组织分解,降低非酯化脂肪酸,减少对β细胞的脂毒性。有实验研究了*酮丙**酸(3-*酮丙**酸)类似物耗尽细胞内能量(ATP)从而导致肿瘤细胞死亡,证明3-*酮丙**酸对糖酵解的抑制作用,这个过程的发生十分迅速。作用的机制涉及甘油醛-3-磷酸脱氢酶(glyceraldehydes-3-phospho-dehydrogenase,GAPDH)不可逆的烷基化和糖酵解的完全抑制作用[67]。该酶是在肝、肾糖异生作用中的关键催化剂。在肿瘤恶液质情况下,肝和肾可以通过生糖氨基酸、甘油和乳酸合成大量的葡萄糖。因此,Jalving M等[68]提出采用KD联合抗糖尿病药物二甲双胍的治疗方式来治疗或辅助治疗肿瘤。据此推测,KD结合抗糖尿病药物二甲双胍对糖异生的抑制作用可作为肿瘤新的治疗方法进行探索。
7 生酮饮食与放化疗
多形性胶质瘤患者预后差,其平均生存期为15个月[69]。多形性胶质瘤是常见的原发性恶性肿瘤,患者和医生在不断寻找新的治疗方法,其中限制碳水化合物和KD越来越受欢迎。最近的数据显示,随着血糖水平升高,患者死亡率升高,说明脑胶质瘤的代谢依赖葡萄糖。因此,KD可降低血糖和胰岛素水平,正常脑细胞和神经胶质瘤细胞的代谢差异可作为辅助放化疗新的治疗方法。有人研究了KD对神经胶质瘤小鼠模型的影响,比较正常动物和荷瘤动物喂食KD或SD的基因表达模式,发现KD能显著减少肿瘤生长和提高生存率。此外,KD的一个标志性特点是增加了酮体,以此作为替代原料,增加肿瘤细胞中ROS的产生,提高神经胶质瘤小鼠模型的生存时间,这种保护作用的机制,涉及复杂的细胞代谢改变,而不仅仅是简单降低葡萄糖水平、改变细胞中涉及氧化应激反应基因的表达[70]。因此,可以深入研究,将KD作为放化疗的有效辅助治疗手段。
8 小结
综上所述,生酮饮食联合其他治疗已被证实可以抑制动物模型恶性肿瘤生长, KD联合KE、HBOT、CR、运动、维生素D及二甲双胍等治疗肿瘤可取得更好疗效。由于疾病共同的代谢特点,组合这些无毒的治疗方法应用于患者可发挥更强的协同抗肿瘤作用。这些疗法可作为全身转移性肿瘤患者潜在的无毒治疗或辅助治疗,但仍需大量的前瞻性研究证明其在临床应用的可行性。




