
自CRISPR/Cas基因编辑技术诞生以来,便很快地应用于各项基础或临床研究的工作上。在过继性细胞疗法中,基于CRISPR/Cas9的基因编辑技术其原理是首先利用设计好的sgRNA引导Cas9核酸酶靶向切割目标DNA,在靶向位置形成一个双链断裂。然后依赖DNA同源重组修复机制(homology-directed repair, HDR),使用修复模板对断裂的DNA进行修复,从而实现基因的敲除或敲入。
目前,对于过继性细胞疗法的许多研究和临床应用仍然依赖于提高基因编辑效率、细胞生存能力以及非病毒基因打靶的实用性上面。因此,为了创造更广泛的细胞过继疗法,就要求基因编辑技术能够更加的通用和精确。
2019年12月9日,美国加州大学旧金山分校Alexander Marson团队在Nature Biotechnology杂志上发表了题为:Polymer-stabilized Cas9 nanoparticles and modified repair templates increase genome editing efficiency 的研究论文。
该研究通过优化同源重组修复模板并添加聚合物以增加Cas9核糖核蛋白(ribonucleoprotein, RNP)纳米颗粒的稳定性,从而在不同的免疫细胞类型和造血干细胞间进一步将基因组编辑效率提高了2-6倍。

研究内容
首先,研究人员设计了一种新颖的方法,尝试将具有核定位序列(nuclear localization sequences, NLSs)的Cas9 RNPs招募到HDR模板中,以促进HDR模板能够更容易进入细胞核。他们在HDR模板的两端分别加上了一段缩短到只有16bp的Cas9靶标序列(Cas9 target sequences, CTSs),这样既能保证Cas9 RNP能有效地与CTS序列结合,又不至于对CTS序列发挥双链剪切作用。
结果发现,使用优化的修复模板能够以更高的效率对多种T细胞进行基因编辑,并且带有缩短CTS(truncated CTS, tCTS)的HDR模板甚至在与未修饰的HDR模板同时导入到相同细胞后的直接竞争中也获得了优先的靶向性。

由于高浓度的外源DNA具有较强的细胞毒性,为此研究人员也分析了RNP-HDR模板相互作用对细胞活力的影响。研究结果发现,使用tCTS修饰的HDR模板进行基因编辑可显著提高效率,但也观察到,其比未修饰的HDR模板表现出更强的细胞毒性。之前的研究表明,与Cas9 RNP共传递可以减轻人T细胞中的外源DNA毒性。
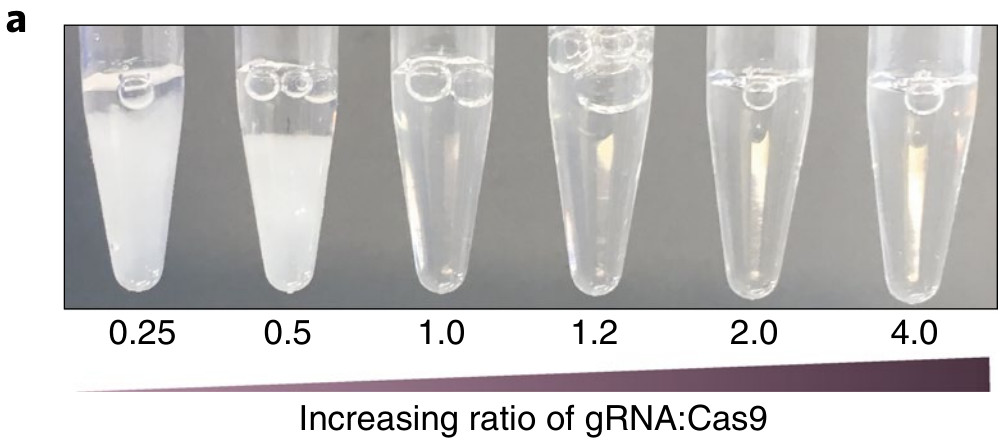
当过量摩尔质量的蛋白质(RNA与Cas9蛋白质的摩尔比<1.0)与gRNA结合时,会形成乳白色不透明的溶液,即功能性较差的蛋白质。通过添加额外的sgRNA或非同源单链寡核苷酸(non-homologous single strand oligo, ssODNenh)将有助于分散Cas9 RNP从而增加其稳定性并提高基因编辑效率。然而,研究人员也发现过量使用gRNA和ssODNenh的组合并不能进一步改善编辑,表明这其中也许存在共同作用的机制。
接下来,研究人员假设,核酸的聚合和阴离子性质可将Cas9蛋白的过量带正电荷的残基与Cas9结合的gRNA的附近暴露部分隔离开,从而防止聚集并改善RNP颗粒的稳定性。并筛选了各种商用水溶性生物和合成高分子材料,以探究由电穿孔介导的Cas9基因编辑的能力。研究结果发现,单纯的Cas9蛋白直径在10-15nm之间,加入gRNA与之混合后会发生聚集,使直径达到200nm。
而当加入聚谷氨酸(poly-l-glutamic acid, PGA)或ssODNenh后,均显示阻止了Cas9蛋白聚集,改善了RNP纳米颗粒的尺寸分布,使之降低到100nm左右,从而提高了基因编辑效率。进一步的实验表明,将携带tCTS序列的修复模板与阴离子聚合物PGA相结合,显著提高了基因敲入的效率以及细胞生存能力,并提高了在多种内源性基因组位点编辑的活T细胞的生存率。

最后,为了评估Cas9 RNP纳米粒子的稳定性提高后是否也有可能会同时提高基因编辑的脱靶性。当加入PGA后,研究人员观察到,相对于单独的RNP,脱靶插入缺失的形成仅略微增加。另外,通过tCTS修饰的HDR模板与标准dsDNA HDR模板相比,不会增加转基因的脱靶表达。尽管需要进一步的工作来评估特定RNP和HDR模板的全局脱靶效率,但这些结果表明PGA和修改后的模板可以显著提高基因敲入的靶向性,同时最大程度地减少脱靶效应的增加。
获得了以上这些数据结果的支持下,研究人员便尝试在不同的细胞类型中应用优化的CRISPR/Cas9系统。最终结果显示在CD3+ T细胞、CD4+ T细胞、CD8+ T细胞和CD127lowCD4+ CD25+Treg细胞中,50%以上的细胞实现了基因编辑,相比于为优化的系统取得3-8倍的基因编辑效率;在γδ T细胞中,编辑的细胞从5%提高到了28%,取得了5-6倍的编辑效率。在人CD34+造血干祖细胞(HSPCs)中实现了在15%的细胞中转入大片段基因,取得了2-3倍的敲入效率。证明了,联合非病毒系统的优化CRISPR/Cas9技术在多种人类造血细胞类型中能够显著提高基因编辑效率。

小结
结合使用PGA作为RNP纳米颗粒稳定增强剂和tCTS修饰的HDR模板,可以在多种原代造血细胞类型中实现高百分比的编辑,并提高了编辑后的细胞产量,为T细胞以外的下一代过继性细胞疗法打开了大门。
值得注意的是,聚合物或tCTS的进一步优化也可能会带来其他方面改进。该研究的数据提供了一个技术上十分简单易操作的系统,大大增强了Cas9 RNP介导的非病毒基因组在原代人类造血细胞中的基因编辑能力。并且具有向基础性研究、生物技术和临床应用直接转化的潜力。
论文链接:
https://doi.org/10.1038/s41587-019-0325-6