目前有越来越多的证据证明生物活性化合物在治疗结直肠癌肝转移中的作用。这些药物包括抗血管生成药物,如贝伐珠单抗,和抗表皮生长因子受体药物,如西妥昔单抗和帕尼单抗。
图1 贝伐珠单抗
贝伐珠单抗是一种重组人源化单克隆抗体,它通过抑制血管内皮生长因子A来阻断血管生成(图1)。
它是美国食品和药物管理局(FDA)批准的第一个血管生成*制剂抑**。在化疗之外使用贝伐珠单抗的理由是,血管内皮生长因子介导的微转移灶的增殖可能导致结直肠癌肝转移切除后的复发,抑制血管内皮生长因子可以阻止复发。一项早期研究探索了围手术期的CAPOX(卡培他滨和奥沙利铂)联合贝伐珠单抗在未进行前期切除的高风险结直肠癌肝转移患者中的疗效[1]。在新辅助治疗CAPOX加贝伐珠单抗应用后,客观缓解率(ORR)达到了78%(95%可信区间为63%-89%)。这一研究同时表明,在40%的患者中,不可切除的异时性结直肠癌肝转移可以被转变成可切除的疾病。
Bertollini等人的另一项研究显示,12例患者(57.1%)接受了FOLFOX6方案加贝伐珠单抗产生了客观反应(图2)[2]。本研究还表明,联合用药不会增加术后并发症,并可获得较高的可切除率。尽管贝伐珠单抗引起的手术后创伤愈合受损一直备受关注,但一些研究已经证明了该药物在结直肠癌肝转移治疗中的安全性。

图2 贝伐珠单抗治疗效果
抗表皮生长因子受体药物在RAS和BRAF野生型左侧转移性结直肠癌中具有活性,且已有多项研究检测了它们在治疗治疗结直肠癌肝转移中的作用。
在PLANET-TTD试验中,帕尼单抗联合FOLFOX4方案或者FOLFIRI方案作为KRAS外显子2野生型结直肠癌患者及结直肠癌肝转移患者的一线治疗方案。帕尼单抗联合FOLFOX4方案的客观缓解率为74%,帕尼单抗联合FOLFIRI方案的客观缓解率为67%,两者分别有45%和59%的患者进行了手术治疗。帕尼单抗联合CAPOX方案的活性也得到了证明,其客观缓解率为54%[3]。在KRAS野生型肿瘤中,客观缓解率达到了65%,使得15例原本无法切除的肝转移癌转变成了可切除性疾病。

图3 西妥昔单抗
西妥昔单抗在这一人群中也得到了广泛的研究(图3)。在CELIM试验中,比较了一线的FOLFOX方案联合西妥昔单抗和FOLFIRI方案联合西妥昔单抗,两种方案在57-68%的患者中均表现出反应,并且在化疗后,可切除率从基线时的32% (68例中的22例) 增加到60%(68例中的41例)[4]。在一项随访生存分析中,研究证实了对转化治疗有反应并行切除术的最初不能切除的结直肠肝转移患者有良好的长期生存结果[5]。在此研究中,对于KRAS野生型肿瘤,FOLFOX方案联合西妥昔单抗和FOLFIRI方案联合西妥昔单抗似乎都是转化治疗的合适方案。其他一些研究也显示了西妥昔单抗联合FOLFOX6方案或FOLFIRI方案具有类似的活性。
相反地,新的EPOC试验表明,与单独化疗相比,化疗方案(FOLFOX、CAPOX或FOLFIRI)联合西妥昔单抗对于可切除的或可考虑切除的结直肠癌肝转移的KRAS外显子2野生型患者来说,会导致中位无进展生存期(mPFS)缩短。抗表皮生长因子受体疗法被认为在结直肠癌合并左侧原发肿瘤中更为有效。然而,本研究中大部分患者为左侧原发肿瘤,因此肿瘤侧边性并不能解释化疗加用西妥昔单抗后无进展生存期差异。Pugh等研究者认为,对于microRNA (miR)-31-3p低表达的肿瘤患者,加入西妥昔单抗并不会产生不良影响[6]。但是,未来的研究将需要进一步探索在结直肠癌肝转移切除术中哪些RAS野生型患者会从西妥昔单抗中获益。
最近,一些研究比较了抗血管内皮生长因子和抗表皮生长因子受体疗法。
在BECK试验中,35例不可切除结直肠癌肝转移患者被纳入,KRAS野生型肿瘤患者接受mFOLFOX6方案联合西妥昔单抗治疗,而KRAS突变型肿瘤患者接受mFOLFOX6方案联合贝伐珠单抗治疗。野生型肿瘤患者中转化率为72.7%,突变型肿瘤患者为33.3% (P = 0.03)。58.8%的患者按照治疗方案行肝切除术,客观缓解率为64.7%。
在患者接受贝伐单抗或西妥昔单抗治疗后,Stremitzer等人对不同的转移病灶组织进行了检测,他们发现,与西妥昔单抗相比,贝伐单抗联合化疗使得转移灶更多的坏死(图4),但更少的纤维化,并倾向于具有更高的组织学及放射学反应,和更长的无复发生存期。[7]
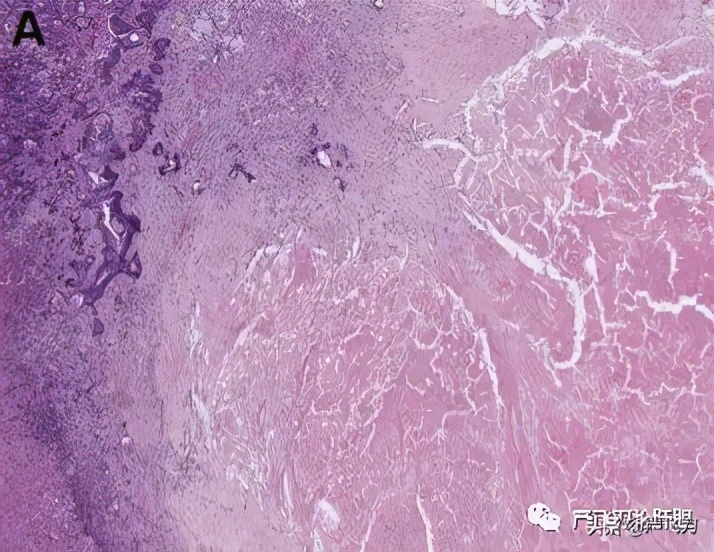
图4 坏死反应
参考文献:
[1] Wong R, et al. A multicentre study of capecitabine, oxaliplatin plus bevacizumab as perioperative treatment of patients with poor-risk colorectal liver-only metastases not selected for upfront resection. Ann Oncol. 2011;22(9):2042–8.
[2] Bertolini F, et al. FOLFOX6 and bevacizumab in non-optimally resectable liver metastases from colorectal cancer. Br J Cancer. 2011;104(7):1079–84.
[3] Leone F, et al. Panitumumab in combination with infusional oxaliplatin and oral capecitabine for conversion therapy in patients with colon cancer and advanced liver metastases. The MetaPan study. Cancer. 2013;119(19):3429–35.
[4] Folprecht G, et al. Tumour response and secondary resectability of colorectal liver metastases following neoadjuvant chemotherapy with cetuximab: the CELIM randomised phase 2 trial. Lancet Oncol. 2010;11(1):38–47.
[5] Folprecht G, et al. Survival of patients with initially unresectable colorectal liver metastases treated with FOLFOX/cetuximab or FOLFIRI/cetuximab in a multidisciplinary concept (CELIM study). Ann Oncol. 2014;25(5):1018–25.
[6] Pugh S, et al. Association between miR-31-3p expression and cetuximab efficacy in patients with KRAS wild-type metastatic colorectal cancer: a post-hoc analysis of the new EPOC trial. Oncotarget. 2017;8(55):93856–66.
[7] Stremitzer S, et al. Histological response, pattern of tumor destruction and clinical outcome after neoadjuvant chemotherapy including bevacizumab or cetuximab in patients undergoing liver resection for colorectal liver metastases. Eur J Surg Oncol. 2015;41(7):868–74.