2017年为肝细胞癌治疗方法突破的一年,不仅Amgen/Bayer的Stivarga (regorafenib)与BMS的Opdivo (nivolumab)获得药证,Eisai的Lenvima (lenvatinib)亦已提交肝细胞癌新适应症申请,将打破肝细胞癌药品市场十年来仅有Nexavar (sorafenib)一款药独占局面。
肝细胞癌根据巴塞隆纳临床肝癌分期系统(Barcelona Clinic Liver Cancer,BCLC)的分期,会有不同治疗方式,药品部分自Nexavar于2007年9月在美国、2007年10月在欧盟、2009年5月在日本获准治疗无法切除之肝细胞癌以来,已独占肝细胞癌药品市场约十年。
Nexavar作为第一款肝细胞癌标靶药物,其当年上市为晚期肝细胞癌的治疗开启新里程碑,然而其反应率(ORR)相当低(2.3~3.3%),使得能受益于该款药物的病患数量相当有限。
第二款上市的标靶药物Stivarga,于2017年4月在美国、5月在日本、8月在欧盟获准用于肝癌治疗,作为在Nexavar治疗过后的二线疗法。Stivarga整体存活期OS与Nexavar接近,约10个月多,ORR也仅7%。
Opdivo是当今癌症免疫疗法的领先药物之一,Opdivo以CheckMate 040(NCT 01658878)试验提交肝细胞癌美国药证申请。Opdivo在该试验结果,以RECIST v1.1衡量标准的ORR为14.3%,有效反应持续时间(DoR)为大于等于6个月者有91%,大于等于12个月者有55%,此成果获得美国FDA加速核准(Accelerated Approval)。Opdivo在肝细胞癌适应症的正式核准,仍需仰赖临床三期试验CheckMate 459(NCT02576509)的成果。
Keytruda(pembrolizumab)与Imfinzi(durvalumab)是另外2款积极开发肝细胞癌治疗的癌症免疫疗法药物。Imfinzi已揭露一些早期临床试验数据,其在临床一/二期试验(NCT01693562)结果,反应率ORR为10.3%,整体存活期OS为13.2个月,而在另外一个临床一/二期试验(NCT02519348),Imfinzi并用tremelimumab(CTLA-4*制剂抑**)尚未有非预期的安全性事件产生。AstraZeneca现已开始Imfinzi三期临床试验HIMALAYA(NCT03298451)。
Lenvima以临床三期试验REFLECT(NCT01761266)于2017年7月递交肝细胞癌适应症之sBLA申请,美国FDA已于2017年9月27日接受申请。
在该试验中,Lenvima和Nexavar直接进行比较,从试验结果来看,Lenvima整体存活期OS(13.6 vs. 12.3,HR:0.92(CI: 0.79~1.06))不劣于Nexavar,无恶化存活期PFS则显著较佳(7.4 vs. 3.7,HR:0.66(CI: 0.57~0.77)),治疗至疾病进展时间TTP亦较佳(8.9 vs. 3.7,HR:0.63(CI: 0.53~0.73)),反应率ORR亦较佳(24.1% vs. 9%,p<0.00001);部份较佳的临床数据,带给Lenvima切入晚期肝细胞癌第一线药品市场机会。
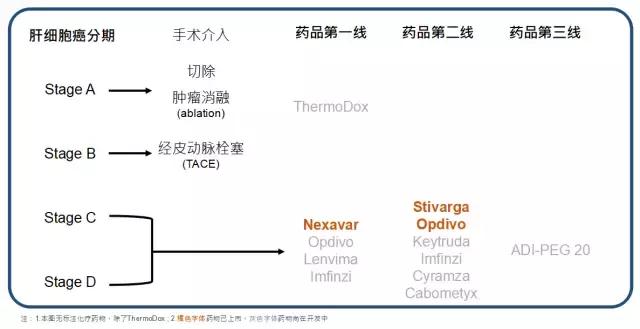
▲肝细胞癌已上市药品发展中新药 source:拓墣产业研究院
综观肝细胞癌药品市场,第一线药品除了Nexavar外,预计Lenvima可望在2018年进入市场和Nexavar竞争,二线药品则已有Stivarga与Opdivo在市场上。
预期在3~5年内,Opdivo可能借由CheckMate 459将适应症扩张至第一线,而Keytruda或/及Imfinzi则有机会成为接续获准用来治疗肝细胞癌的免疫检查点*制剂抑**,Keytruda的KEYNOTE-224、KEYNOTE-240,以及Imfinzi的NCT02519348、HIMALAYA试验值得继续关注。若这些开发中新药皆顺利上市,在第二线药品市场的竞争度较高。
基于肝细胞癌诸多特性,有不少癌症新药在治疗肝细胞癌开发失败,而长年以来的治疗方法或药物对肝细胞癌的治疗成效有限,特别在BCLC阶段C与阶段D的肝细胞癌,肝细胞癌不仅未满足医疗需求高且一直是癌症新药难以挑战的癌种,这也显示出肝细胞癌的药品开发亟需从新的作用标的与机制着手。
整体观之,预期将因多款新药进入市场,晚期肝细胞癌治疗成效可望获得改善,由Nexavar独占局面将开始被打破,在新药驱动下,全球肝细胞癌药品市场也可望快速成长,免疫疗法未来将成为肝细胞癌治疗的主流之一。
(文/拓墣产业研究院 刘适宁)