目前有研究证实放疗除了能*伤杀**肿瘤,也能激活宿主的免疫系统。放疗能调节肿瘤表型,增强抗原提呈和肿瘤免疫原性,增加细胞因子的产生,改变肿瘤微环境,从而通过增强免疫系统*伤杀**肿瘤。免疫治疗能促进宿主抗肿瘤免疫反应,研究者们近几年开始注意到,相比单独使用放射治疗或免疫治疗,两者联合可以导致更有效的抗肿瘤反应。免疫治疗和放疗之间的协同作用已经成为癌症研究项目中的一个热门领域。

要知道肿瘤治疗一向是个复杂的“工程”,单靠某一种治疗手段是很难取得良好效果,肿瘤治疗需要综合性治疗,各手段相互配合才有可能在对付肿瘤的战役中取得最后的胜利。
免疫治疗作为标准治疗,广泛的免疫治疗联合放射治疗的临床前证据
一、广泛的临床前证据
众多临床前研究数据显示在使用 SABR 后免疫应答激活。
在小鼠模型中,使用单次分割 (15-25Gy) 照射后,引流淋巴结区域的T细胞增多,导致CD8+T细胞依赖的原发性肿瘤大小减少或根除以及远处转移。
有研究发现,表达卵清蛋白(OVA)的 B16-F0 肿瘤经过单次分割 (15 Gy) 或照射 (3 Gy×5 次) 后,无论使用其中任何一种分割方案,都会加快抗原提呈以及 T 细胞在引流淋巴结区域的集聚。
另一个B16–OVA 的黑色素瘤小鼠研究发现,在经过不同分割方式(总剂量达 15 Gy)的放疗后,放疗剂量为 7.5 Gy 和 10 Gy 均可以有效激活免疫系统,但 5 Gy 不行,使用较高剂量放疗(≥ 15 Gy)会增加脾脏调节 T 细胞 (TREG) 的比例。
有许多研究显示使用放疗联合抗 CTLA-4 治疗后,与单一治疗模式相比,可以使肿瘤更大程度退缩,且原发灶及远处转移均缩小。进一步研究证实这些效应是由 CD8+T 细胞依赖的抗肿瘤免疫效应引发的。
其他类型的免疫治疗联合高剂量放疗也能增强抗肿瘤效应。例如刺激抗肿瘤免疫的相关单克隆抗体(如抗 CD137 和抗 CD40 抗体)或解除免疫抑制的相关单克隆抗体(抗 PD-1 抗体)联合单次(12 Gy)/ 多次(4-5 Gy×4)放疗。在小鼠模型中,单次分割的放疗与抗 CD137 和抗 PD-1 抗体结合提高了宿主抗肿瘤免疫应答能力(肿瘤排斥率达 40%)。类似地,多次分割放疗结合抗 CD137 和抗 PD-1 抗体也被证实比单一治疗模式更有效。
综合这些数据,可以看出放疗后可以产生有效的免疫刺激,而且放疗治疗联合免疫治疗可提高疗效。

二、积极的病理报告证据

图2 部分免疫治疗联合放射治疗的远隔效应及其协同作用的病理报告证据。
三、大力开展的临床试验

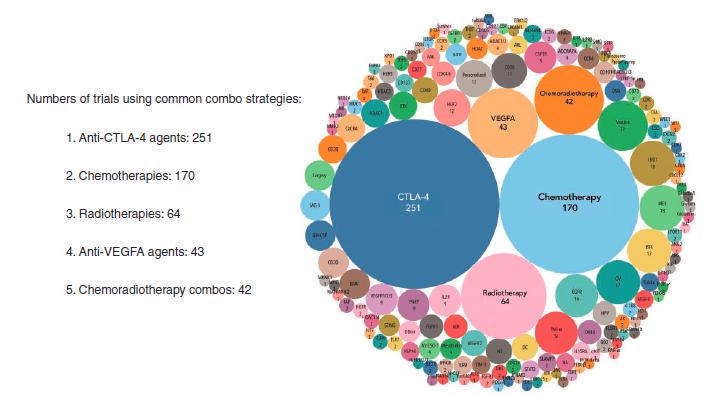
图3.截止2018年PD-1\PD-L1*制剂抑**联合治疗的临床研究大数据分析

图4.部分正在进行中的免疫治疗联合放射治疗的临床试验
放疗与全身免疫系统之间的相互调节作用使放疗与免疫联合治疗成为可能,而且在大量临床前期试验取得显著疗效,在临床实践上主要可以以三种治疗方案来实现:
大分割放疗+免疫治疗方案:主要针对寡转移肿瘤,目的是利用放疗的“原位疫苗”效应最大化射野外联合治疗疗效,即活化抗原呈递细胞(APC)以及解除T细胞抑制信号。该“原位疫苗”效应具有剂量依赖性和分割模式依赖性,而剂量过大或过小都不足以使肿瘤释放更多的抗原。总体来讲,肿瘤控制及肿瘤特异性T细胞激活随放疗剂量增大而增加。

常规分割放化疗+免疫治疗方案:免疫治疗作为放疗后的辅助治疗存在,目的是为了最大化放疗联合免疫的局部协同作用及免疫治疗的全身作用。
放疗作为免疫治疗的调节剂方案:目的提供联合治疗最大化射野内治疗疗效。不同于大分割放疗引起的原位疫苗,激发远端效应的作用。低剂量放疗可以重塑肿瘤微环境,将钝化的免疫微环境重新活化,从而逆转肿瘤患者对免疫治疗的耐药。
四、未来:优化免疫治疗联合放射治疗的临床设计及放疗方
目前设计证明免疫治疗联合放疗疗效的临床试验需要充分考虑以下几个问题。
首先选择合适的病人仍然是至关重要的,肿瘤位置、临床分期和组织学类型等的不同都会影响临床结局。
其次,要把握好免疫治疗联合放疗的最佳时机。
最后,要充分考虑患者对治疗的敏感性差异并制定相关治疗策略和检验疗效的方法,以往使用的肿瘤缩小率、生存期等指标用于免疫治疗联合放疗不够全面,显示不出早期疗效,因此研究者提出了几项免疫治疗联合放疗的研究设想,用常规和生物标志物相结合的方法来鉴定获益于免疫治疗联合放疗的患者。
在免疫疗法背景下,如何优化放疗方案,还需要考虑最佳的分割方案和剂量、放疗和免疫治疗的间隔时间、对临床目标体积(CTV)的影响,病灶的选择和安全性。

如果大家想全面了解自身的免疫状态或相关的免疫疗法,可私信联系我了解更多信息。