▎药明康德/报道
两针包一年! RNAi创新疗法再获新突破
The Medicines Company宣布,每年只需接受两次皮下注射的RNAi疗法inclisiran,在降低低密度脂蛋白胆固醇(LDL-C)的关键性3期临床试验中,达到试验的所有主要和次要终点。同时,Inclisiran表现出良好的安全性和耐受性。Inclisiran是使用Alnylam Pharmaceuticals公司的GalNAc递送系统设计的靶向PCSK9的RNAi疗法。此前,RNAi疗法大多用于治疗患者人数较少的罕见病。这一临床试验的成功展现了RNAi疗法在治疗患者人数众多的大众疾病类型方面的潜力,是RNAi疗法自去年首款疗法获得FDA批准以来又一个重要突破。
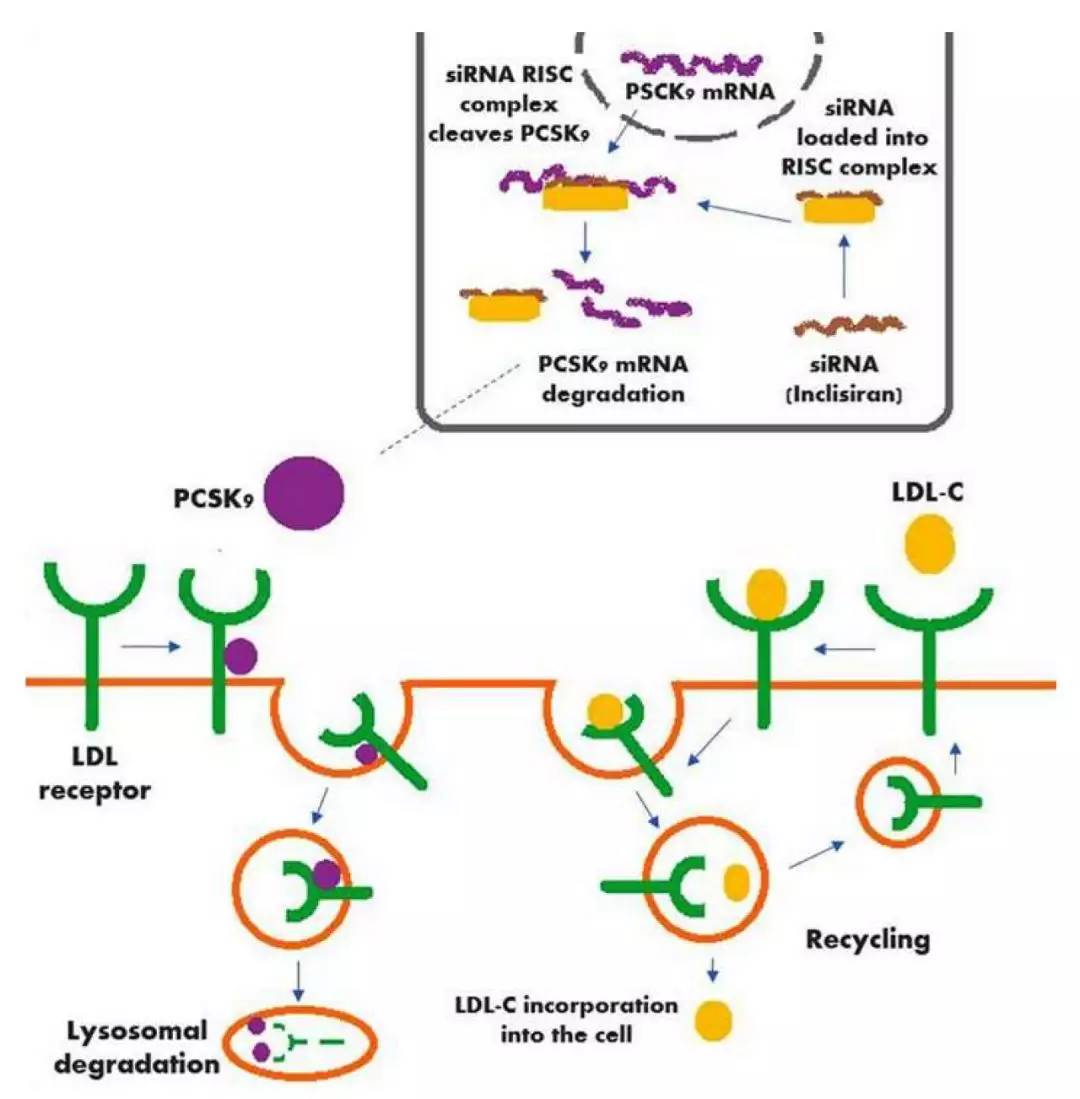
▲Inclisiran作用机制(图片来源:Diseases)
Inclisiran是第一款降低LDL-C的RNAi疗法。它直接与编码PCSK9蛋白的结合,通过RNA干扰作用降低mRNA的水平,从而防止肝脏生成PCSK9蛋白。PCSK9蛋白的作用是抑制LDL受体的回收和再利用。因此,降低PCSK9蛋白的水平可以让更多LDL受体回到肝细胞表面,与更多LDL结合,将它们从血液中清除。多款PCSK9*制剂抑**已经获得FDA批准,而这款RNAi疗法的优势在于患者只需要每年接受2次皮下注射就可以控制胆固醇水平,为患者提供了一款非常便捷的治疗选择。
无袖套时代来临!FDA批准新型无创血压监测仪
专注于研发先进传感技术和患者远程监控解决方案的Biobeat公司宣布,FDA通过510(K) 通道批准其无袖套式血压监测仪上市。该仪器可以在医院和家庭等任何场所监测血压、血氧和心率等生命体征并自动上传到智能应用程序和云端进行远程监控,协助改善疾病管理。这是第一款FDA批准的无袖套式血压监测仪。

图片来源:Biobeat官网
Biobeat的专利技术是基于光学体积描记术(PPG)。它通过使用LED光源,多个波段,以及特定的算法,在即使有背景噪音的情况下也可以精确地接收到PPG信号。这一技术在检测、测量和记录不同生命体征的方法上取得了重大突破。
Biobeat血压监测仪分为两个部分,分别是手表和可以适应任何类型测量的灵活无袖套式传感器。它可以用于进行远程监测,若身体体征引发警报,患者可直接从应用程序中接收警报,护理人员也可进行干预。除了对血压、血氧饱和度、心率、心量输出做出监测,Biobeat监测仪还对体温、步数、汗液、所摄入的卡路里等都有记录。BioBeat的这一创新解决方案不仅可以监测静止的患者,也可以监测进行户外活动的患者,这为护理人员提供了辅助疾病管理和优化临床结果的重大帮助。
十年砺剑终成锋! 协和麒麟Nourianz获FDA批准上市
美国FDA宣布,批准协和麒麟(Kyowa Kirin)株式会社开发的创新药Nourianz(istradefylline)上市,作为左旋多巴/卡比多巴的辅助疗法,治疗经历“关闭”期(“off” episodes)的帕金森病(Parkinson’s disease, PD)成人患者。“关闭”期时患者的药物作用不佳,导致PD症状加剧,包括震颤和行走困难。Istradefylline是一种选择性腺苷A2A受体拮抗剂。协和麒麟曾在2007年向美国FDA递交这款新药的上市申请,然而没有获得批准。10余年之后,这款新药终于获批,有望帮助改善PD患者的生活质量。
Istradefylline是一种口服给药的选择性腺苷A2A受体拮抗剂,腺苷A2A受体是一种存在于基底神经节(basal ganglia)中的G蛋白偶联受体。基底神经节在控制人体运动方面具有重要作用,在PD患者中则会出现变性或异常。Istradefylline可选择性阻断腺苷A2A受体,减缓多巴胺能神经元的退行性病变,且副作用小,可作为左旋多巴类药物的辅助治疗手段。
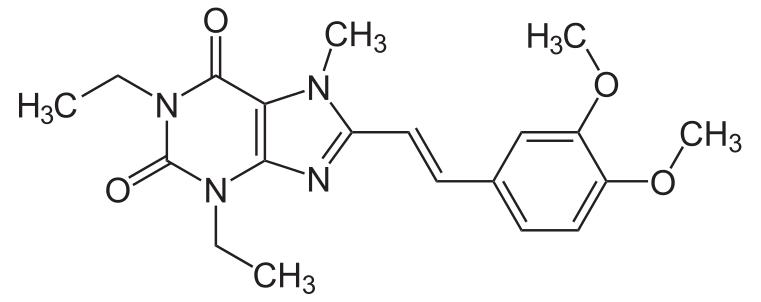
▲Istradefylline分子结构式(图片来源:NEUROtiker [Public domain])
Istradefylline治疗处于“关闭”期PD患者的疗效,在总计包含1143名患者的4项含安慰剂对照的临床试验中得到验证。这些患者都在使用左旋多巴/卡比多巴。在这四项试验中,接受istradefylline治疗的患者每天经历“关闭”期的时间与安慰剂组相比得到统计显著缩短。
“功能性治愈”乙肝迎曙光!GSK斩获两大创新疗法
专注于开发靶向RNA的反义寡核苷酸(ASO)药物的Ionis Pharmaceuticals公司宣布,基于其在研药物IONIS-HBVRx和IONIS-HBV-LRx,在治疗慢性乙肝(CHB)患者的2期临床试验中获得的积极结果,葛兰素史克(GSK)公司将选择获得这两款在研疗法的研发和推广权益。近年来,靶向乙肝病毒基因表达的创新疗法纷纷在临床试验中显示出良好的疗效,它们可能带来“功能性治愈”乙肝的曙光么?
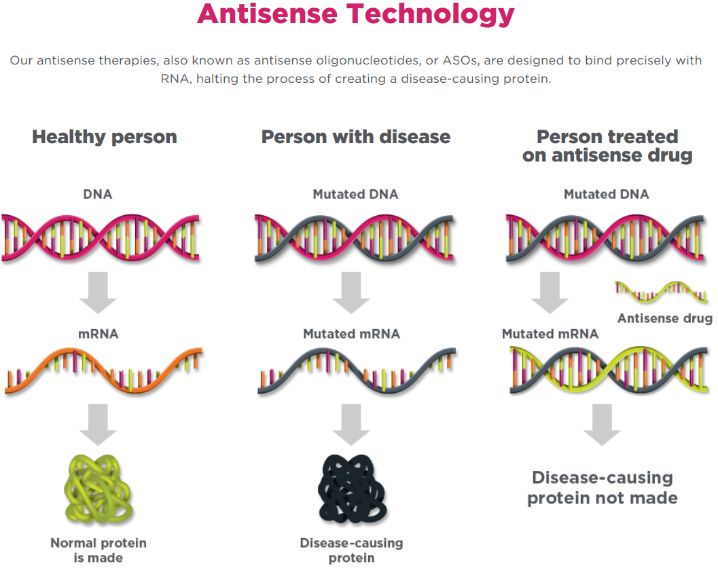
▲Ionis反义疗法图示(图片来源:Ionis官方网站)
Ionis公司开发的IONIS-HBVRx和IONIS-HBV-LRx反义寡核苷酸药物使用了配体复合反义技术(LICA),这种技术通过在反义药物上添加特定化学结构或者分子,增强了药物向特定组织的递送能力,高效特异地抑制HBV的复制与表达。IONIS-HBVRx和IONIS-HBV-LRx这两款药物的设计在于降低跟乙肝病毒感染和复制相关的病毒蛋白,包括乙肝表面抗原(HBsAg),该表面抗原在急性和慢性乙肝中均有表达。
根据协议,GSK将负责这两种药物随后的所有研发、监管和推广活动。Ionis公司将获得高达2.62亿美元的里程碑付款和相应的销售分成。
“亮剑”COPD!阿斯利康三联疗法达到3期临床终点
阿斯利康(AstraZeneca)宣布其三联疗法PT010, 在治疗中度至极重度慢性阻塞性肺病(COPD)患者的3期临床试验ETHOS中,达到试验的主要终点。新闻稿指出,这是首次在一项治疗COPD的3期临床试验中,确定两种不同剂量的三联疗法的临床效益。

PT010是一款由布地奈德(ICS)、格隆溴铵(LAMA)和富马酸福莫特罗(LABA)构成的固定配方复方三联疗法。它使用Aerosphere递送技术,可以装在一个吸入器中使用,为患者提供了更为便捷的服药方式。PT010已于今年6月在日本获得全球首批。目前,它也正在中国、美国和欧盟进行监管审查,且已获得中国国家药监局(NMPA)的优先审查资格。
ETHOS是阿斯利康公司针对PT010的3期临床试验计划中的关键性试验之一。有8500多名中重度COPD患者参与这一随机双盲试验,这些患者在一年内曾经历过中重度疾病恶化情况并且在进入试验之前至少接受了两次的吸入性维持治疗。
试验结果表明,PT010达到了试验的主要临床终点。在标准和低ICS剂量下,与活性对照组的双联疗法相比,PT010显著降低中重度COPD患者的疾病恶化率,且表现出和双联疗法一致的安全性和耐受性。该试验中的双联疗法是目前治疗COPD的推荐疗法,预计这一结果将有助于完善当前的治疗选择。其详细试验数据将在即将召开的医学会议上公布。
挑战红斑狼疮!阿斯利康anifrolumab达到3期临床终点
阿利斯康(AstraZeneca)宣布,其用于治疗系统性红斑狼疮(systemic lupus erythematosus,SLE)的在研单抗药物anifrolumab,在关键性3期临床试验TULIP 2中,达到了显著改善病情的主要终点。Anifrolumab是一款抑制I型干扰素信号通路的单克隆抗体。
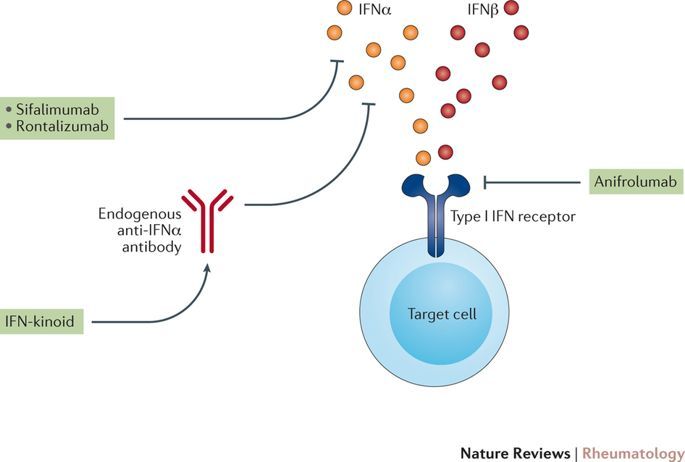
▲Anifrolumab的作用机理(图片来源:Nature)
Anifrolumab可与I型干扰素受体的亚基1相结合,进而拮抗所有1型干扰素(IFN-α、IFN-β和IFN-ω)相关活动。I型干扰素是一类参与炎症反应的细胞因子。IFN-α能促进各种免疫细胞的激活和分化,包括促进自身反应性B淋巴细胞分化成分泌免疫球蛋白的浆细胞,促进树突状细胞成熟并诱导其表达B细胞激活因子(BAFF)和增殖诱导配体(APRIL)。60%到80%的SLE患者存在I型干扰素高表达特征,而I型干扰素浓度与SLE患者疾病活动指数(SLEDAI)评分呈正相关。
373名中重度SLE患者参与了TULIP 2试验,他们被随机分为两组,在接受标准疗法的基础上,分别接受每4周注射一次300mg anifrolumab,或安慰剂。试验结果显示,anifrolumab显著改善了基于BILAG的狼疮综合评价指数(BICLA),为患者病情带来统计显著且具有临床意义的缓解。BICLA改善意味着患者所有器官的疾病活动都有所改善,并且没有新的疾病突发。
百分百控制!创新抗癌疗法喜获FDA突破性疗法认定
SpringWorks Therapeutics公司宣布,美国FDA授予该公司开发的nirogacestat突破性疗法认定,用于治疗复发或难治性、无法切除的硬纤维瘤(desmoid tumors)或深部纤维瘤病(deep fibromatosis)。
Nirogacestat是一款口服特异性γ-分泌酶小分子*制剂抑**。γ-分泌酶能够切割多种跨膜蛋白复合体,其中包括Notch蛋白。而Notch蛋白被认为能够激活导致硬纤维瘤生长的信号通路。除了治疗硬纤维瘤以外,SpringWorks还与葛兰素史克(GSK)公司达成研发协议,在多发性骨髓瘤(MM)患者中检验nirogacestat与其它MM疗法联用的效果。
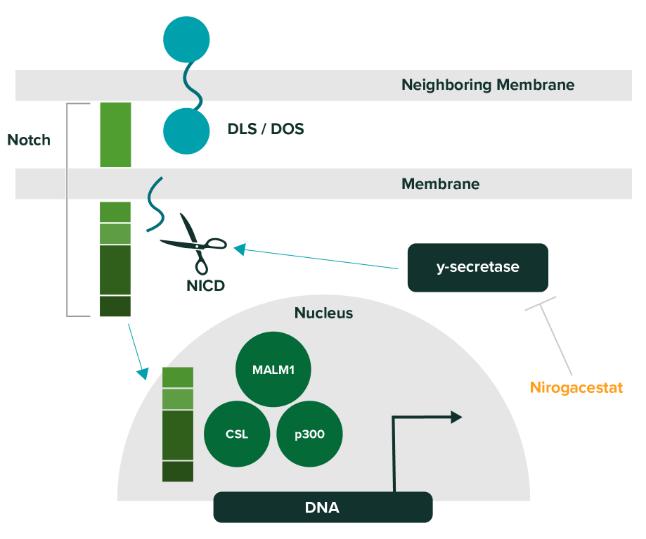
▲Nirogacestat的作用机制(图片来源:SpringWorks公司官网)
这一突破性疗法认定是基于nirogascestat在治疗包含24名硬纤维瘤患者的1期和2期临床试验中的表现。在这些研究中,nirogacestat治疗表现出100%的疾病控制率,由于患者的疾病缺乏进展,在试验数据公布时患者的中位无进展生存期尚未达到。
更进一步!诺华ofatumumab治疗多发性硬化症3期结果积极
诺华(Novartis)公司宣布,其人源化的CD20抗体ofatumumab,在治疗复发性多发性硬化症(RMS)患者的3期临床试验中达到主要终点,ofatumumab的表现优于另一款治疗多发性硬化症(MS)的常用药。诺华公司预计将在年底向FDA递交监管申请。如果获批,ofatumumab有望成为首款可在家自行使用的治疗RMS的B细胞疗法。
Ofatumumab是一款完全人源化的CD20抗体。它通过与B淋巴细胞表面的CD20结合,能够清除血液中B细胞,而这些细胞在MS患者中对激发自身免疫反应有重要作用。这款疗法能够让患者每月一次,在家中通过皮下注射给药。不但为控制病情提供了便利,而且可以更好地靶向淋巴节中的B细胞,减少对脾脏中B细胞的损伤。在此前,ofatumumab已经获得FDA批准作为白血病疗法。 共有1882例MS患者参与这一为期30个月的ASCLEPIOS试验。该试验包含两项双盲、随机试验,是头对头的疗效比较试验,对比ofatumumab与teriflunomide治疗MS成人患者的安全性和疗效。结果表明,ofatumumab与活性对照组相比,在降低MS的年复发率(ARR)上达到了主要临床终点。其延缓疾病进展的关键性次要终点也得以满足。Ofatumumab还表现出良好的安全性和持续的疗效。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。