**今条头日**上无法显示上标、下标,欲获得更好的阅读体验请前往微信公众号。
*前往“纳米酶Nanozymes”公众号,了解有关纳米酶的最新消息!
*本文首发于“纳米酶Nanozymes”公众号,2022年5月15日
*编辑:俞纪元
一、 背景介绍:
氧化应激与许多急慢性炎症相关,过度炎症反应中的活性氧(ROS)会加重局部损伤,但一些用于清除ROS的广谱性抗氧化剂的有效性、稳定性差等缺点限制了它们的应用。纳米医学的发展为探索清除ROS的新方法提供了方向,利用具有ROS清除能力的纳米酶就是一种很有效的策略。具有过氧化氢酶(CAT)、超氧化物歧化酶(SOD)和谷胱甘肽过氧化物酶(GPx)活性的纳米酶的活性氧清除能力可与天然酶媲美,能够清除多种有毒活性氧,并且具有稳定性更好、可快速从体内清除、生物相容性好等优点。
基于此,浙江大学高分子合成与功能构造教育部重点实验室的毛峥伟教授、美国国立卫生研究院的陈小元教授以及第三军医大学烧伤研究所的罗高兴教授等研究团队共同开发了一种超小的Cu5.4O纳米颗粒Cu5.4O USNPs,这种超小的铜基纳米颗粒能够模拟CAT、SOD、GPx酶活性,具有良好的生物相容性、ROS清除能力以及肾脏清除性能,可有效治疗ROS有关的疾病 图1。
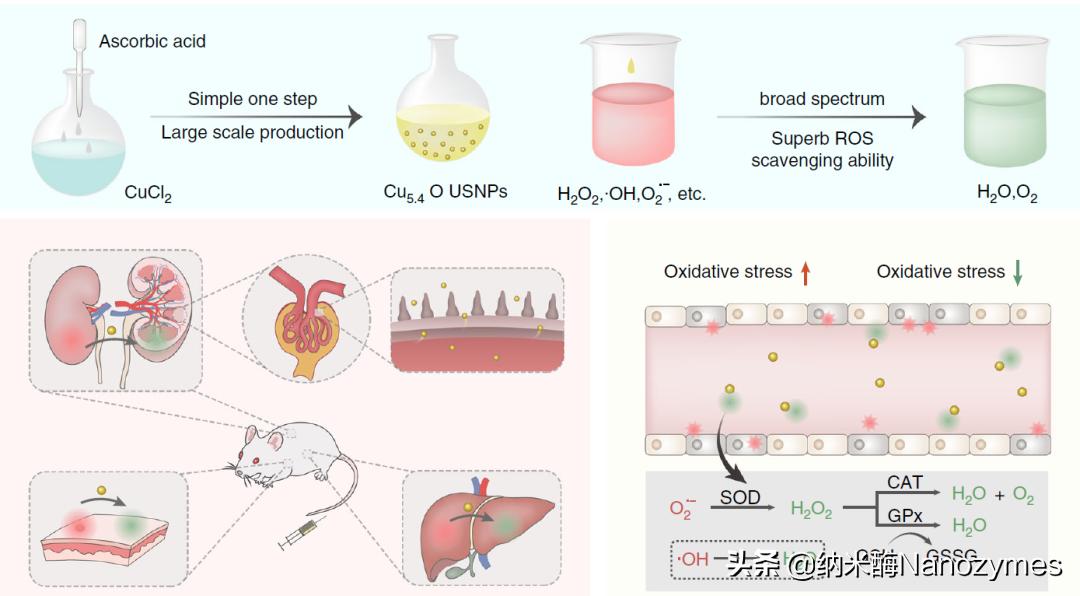
图 1 Cu5.4O超微纳米颗粒治疗ROS相关疾病的示意图
二、 图文导读:
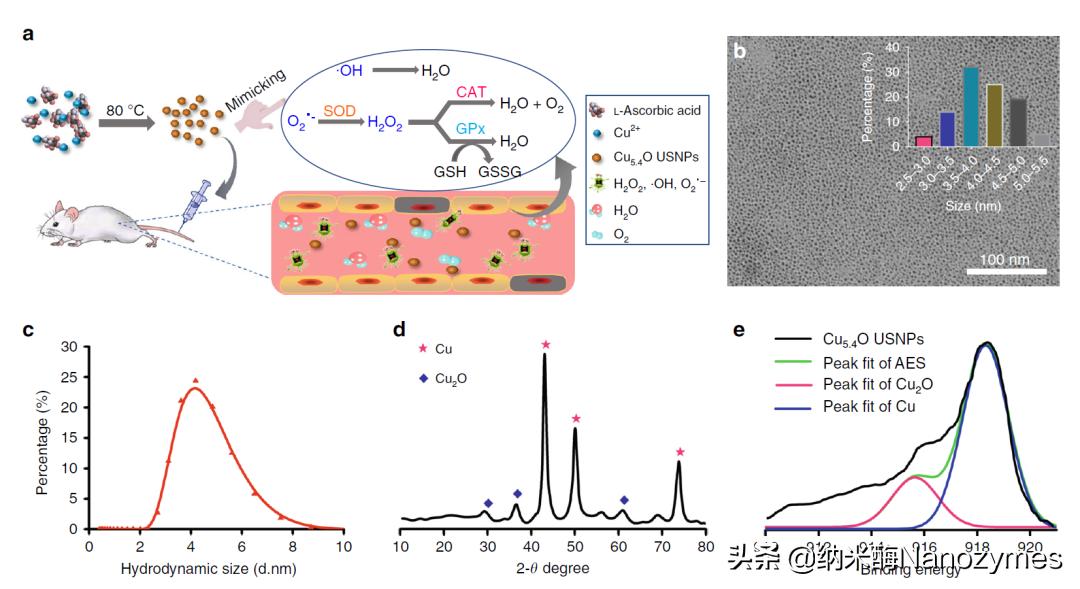
图 2 Cu5.4O USNPs的合成与表征 a. Cu5.4O USNPs的制备示意图; b. Cu5.4O USNPs的TEM图像,插图为粒径分布统计图; c. Cu5.4O USNPs的流体动力学直径分布图;. d, Cu5.4O USNPs的X射线衍射(XRD)图; e. Cu5.4O USNPs的俄歇电子能谱XAES图。
USNPs的合成采用绿色、快速、经济的方法 图2a,TEM图像显示这些Cu5.4O USNPs粒径均匀,在干燥状态下的平均直径为3.5-4.0nm(图2b)。Cu5.4O USNPs的流体动力学直径平均约为4.5 nm,小于肾脏过滤阈值5.5nm 图2c,保证其能够被肾脏有效摄取、在肾脏中积累并被清除。通过X射线衍射研究Cu的氧化状态(图2d),结果表明,反应生成的不是纯Cu NPs,而是CuO和Cu+的混合物(Cu和Cu2O NPs)。如图2e,根据Cu 2p的峰面积计算出Cu和Cu2O的比例约为3.4。因此,将所得到的超小铜基NPs记为Cu5.4O USNPs。
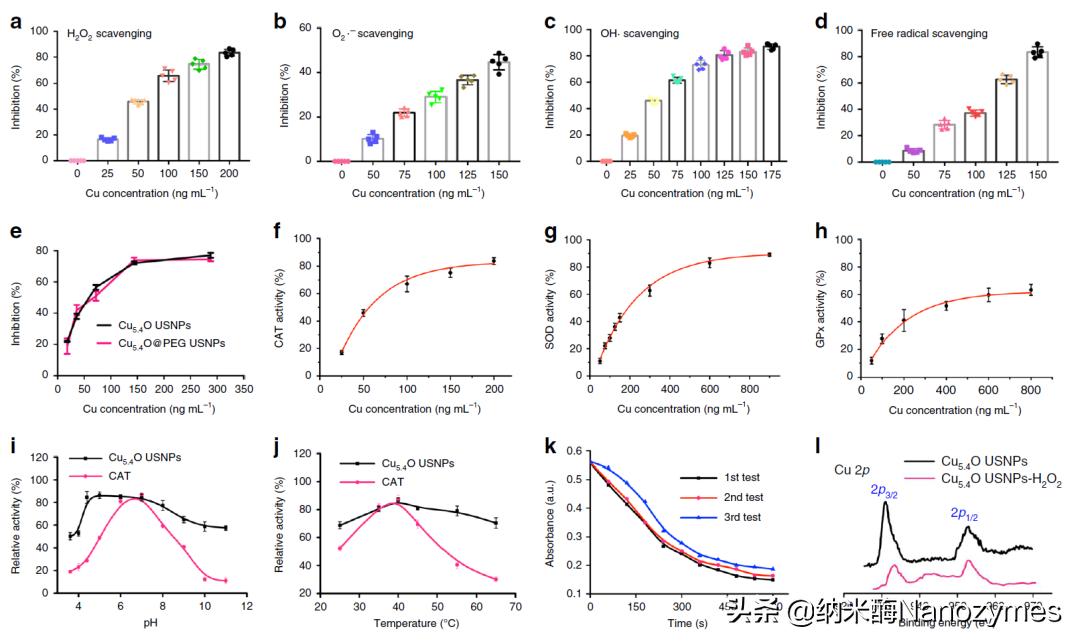
图 3 Cu5.4O USNPs的ROS清除能力和多酶活性 a. H2O2, b. O2-, c. ·OH和 d. 自由基被Cu5.4O USNPs清除的情况; e. Cu5.4O USNPs and Cu5.4O@PEG USNPs的H2O2清除情况; f. Cu5.4O USNPs的CAT酶活性; g, Cu5.4O USNPs的SOD酶活性; h. Cu5.4O USNPs的GPx酶活性; i. 不同pH条件下Cu5.4O USNPs和天然CAT分解H2O2 2mM的情况; j. 不同温度条件下Cu5.4O USNPs和天然CAT分解H2O2 2mM的情况; k. Cu5.4O USNPs (250 ng/mL) 在不同循环下的稳定性测试; l. 对Cu5.4O USNPs与H2O2反应前后的XPS分析。
研究人员选取了3种具有代表性的ROS,H2O2、O2-和·OH,研究Cu5.4O USNPs清除ROS的能力。如图3所示,Cu5.4O USNPs具有较强的ROS清除能力,并且与浓度有关。200ng/mL的Cu5.4O USNPs可分解约80%的H2O2 (图3a);150ng/mL的Cu5.4O USNPs可清除约50%的O2- (图3b)和80%的·OH(图3c)。图3d也显示,150ng/mL的Cu5.4O USNPs可清除约89%的自由基。用化学惰性的HS-PEG-OH代替Cu5.4O USNPs表面的抗坏血酸后检测其H2O2的清除能力并与Cu5.4O USNPs进行比较,结果显示二者的H2O2清除能力相近(图3e)。随后,研究人员研究了Cu5.4O USNPs的多酶活性,图3f、g、h显示Cu5.4O USNPs具有浓度依赖性的CAT、SOD、GPx酶活性。由于天然酶在应用中有稳定性较差的缺点,研究人员比较了Cu5.4O USNPs与天然CAT酶在不同温度和pH条件下稳定情况,图3i、k显示Cu5.4O USNPs的稳定性显著优于天然CAT酶。X射线光电子能谱(XPS)显示Cu5.4O USNPs的Cu 2p能级区的在932.4和952.0 eV处有两个峰,被H2O2氧化后两个主峰的位置没有发生变化,并且没有出现新的峰。这说明Cu5.4O USNPs可利用其多酶活性清除ROS。

图 4 Cu5.4O USNPs体外ROS清除情况 a. 不同处理条件下HEK293细胞的ROS染色(绿色荧光)情况; b. 未使用Cu5.4O USNPs处理和Cu5.4O USNP预处理细胞与250 μMH2O2孵育后的ROS情况; c. 不同处理条件下HEK293细胞ROS水平的统计分析情况; d, 不同处理条件下HEK293细胞的存活情况; e. 流式细胞仪检测未使用Cu5.4O USNPs处理和Cu5.4O USNP预处理的细胞的凋亡和坏死分布情况; f. 不同处理条件下HEK293细胞坏死和凋亡比例的统计分析情况。
研究人员利用人胚胎肾293 (HEK293)细胞检测Cu5.4O USNPs体外对ROS损伤的细胞的保护性。如图4a所示,250μM H2O2处理HEK293细胞后,细胞内ROS水平(绿色荧光信号)明显升高,而Cu5.4O USNPs预处理的细胞内ROS水平明显降低。流式细胞术对细胞内ROS水平的定量分析进一步证实了这一结果(图4b,c)。CCK-8分析结果(图4d)也显示低浓度(25 ng/mL)的Cu5.4O USNPs能够保护细胞免受250 μMH2O2的损伤。进一步通过流式细胞术检测Cu5.4O USNPs对H2O2诱导的细胞凋亡和坏死的影响的结果显示,Cu5.4O USNPs显著降低了H2O2诱导的细胞凋亡和坏死的比例(图4e,f),进一步表面Cu5.4O USNPs在细胞水平上清除ROS和保护细胞的能力。

图 5 Cu5.4O USNPs体内外生物相容性 a. 在静脉给药24h后,评估Cu5.4O USNPs对主要器官(心、肝、脾和肺)的体内毒性; b. 静脉给药24h后,评估Cu5.4O USNPs对肾脏的体内毒性; c. 血清中IL-6和TNF-α水平; d, 血清肝功能指标:天冬氨酸转氨酶 (AST)、丙氨酸转氨酶 (ALT)水平; e. 血清肾功能指标:血尿素氮 (BUN)、肌酐 (CRE)水平; f-j. 正常小鼠(对照组)和小鼠静脉注射Cu5.4O USNPs 24h后的血液参数。
接下来,研究人员评估了Cu5.4O USNPs (4 μg/kg)对健康小鼠主要器官组织病理学的影响,以评估它们在体内治疗时的生物相容性。如图5a、b所示,在单次静脉注射Cu5.4O USNPs 24h后,未观察到心脏、肝脏、脾脏和肺的坏死、充血和出血,并且小鼠的肾小球、小管、集合管和尿道也未观察到明显的炎性病变或组织损伤。如图5c所示,Cu5.4O USNPs处理组血清白细胞介素-6 (IL-6)和肿瘤坏死因子-α (TNF-α)水平与对照组相似,表明Cu5.4O USNPs在实验浓度*体下**内不会引发明显的免疫反应。图5d、e的血清生化分析结果显示,Cu5.4O USNPs处理组的肝功能指标(AST)、丙氨酸转氨酶(ALT)和肾功能指标(BUN和CRE)的浓度也与对照组相似,表明Cu5.4O USNPs对肝脏和肾脏也具有良好的生物相容性。全血分析结果(图5f-j)也显示,Cu5.4O USNPs治疗组与对照组相比没有明显差异。
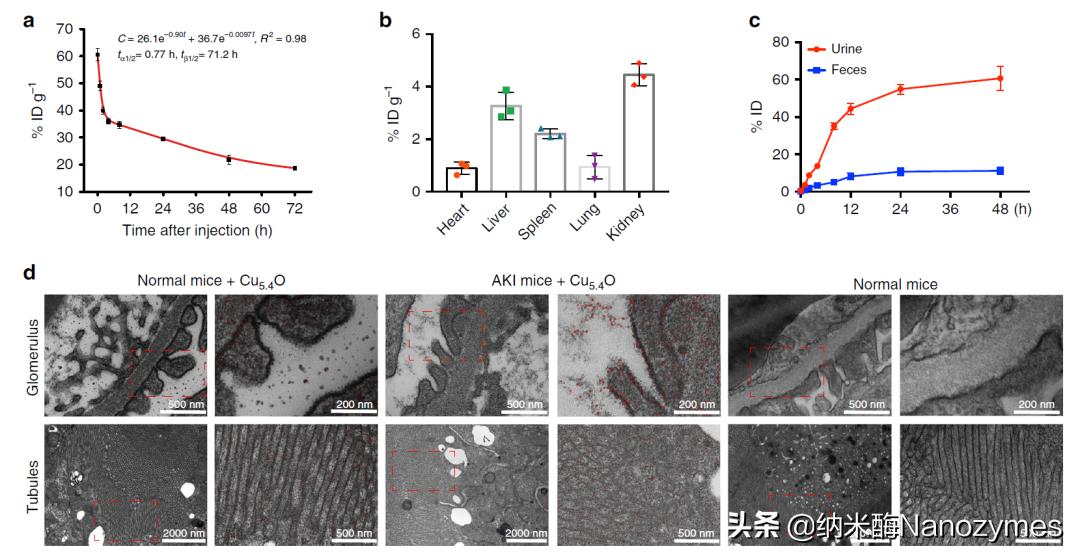
图 6 Cu5.4O USNPs在小鼠体内的药物代谢动力学和生物分布情况 a. 静脉注射Cu5.4O USNPs后小鼠体内的血液药动学曲线; b. 注射24h后Cu5.4O USNPs在主要器官中的分布情况; c. 不同时间点尿液、粪便排泄的累积情况; d. 透射电镜观察Cu5.4O USNPs在肾组织中的生物分布情况,红色虚线表示被放大区域。
随后,研究人员对Cu5.4O USNPs在小鼠体内的药物代谢动力学和生物分布情况进行了探究。如图6a所示,Cu5.4O USNPs在小鼠体内主要成和次要成分的半衰期分别为0.77和71.2h。采用电感耦合等离子体发射光谱法检测Cu5.4O USNPs注射后24 h在急性肾损伤小鼠的主要器官中的生物分布情况, Cu5.4O USNPs在肾脏的分布最高(4.4% ID g-1),而在心脏、肝脏、脾脏和肺的NPs分布分别为0.89、3.2、2.1和0.94% ID g-1 图6b。此外,尿液中Cu5.4O USNPs随时间积累的现象表明,这些颗粒主要通过肾脏被清除,而非通过肠道 图6c。约70%的Cu5.4O USNPs可在注射后48h内排出(60%通过肾脏排出,10%通过肠道排出),这说明Cu5.4O USNPs的清除比较迅速,长期毒性较低。TEM观察小鼠肾组织的结果显示,Cu5.4O USNPs在肾小球基底膜、肾小管的尿腔和上皮细胞纤毛中都有出现 图6d,表明Cu5.4O USNPs可通过肾小球基底膜到达含尿小管。
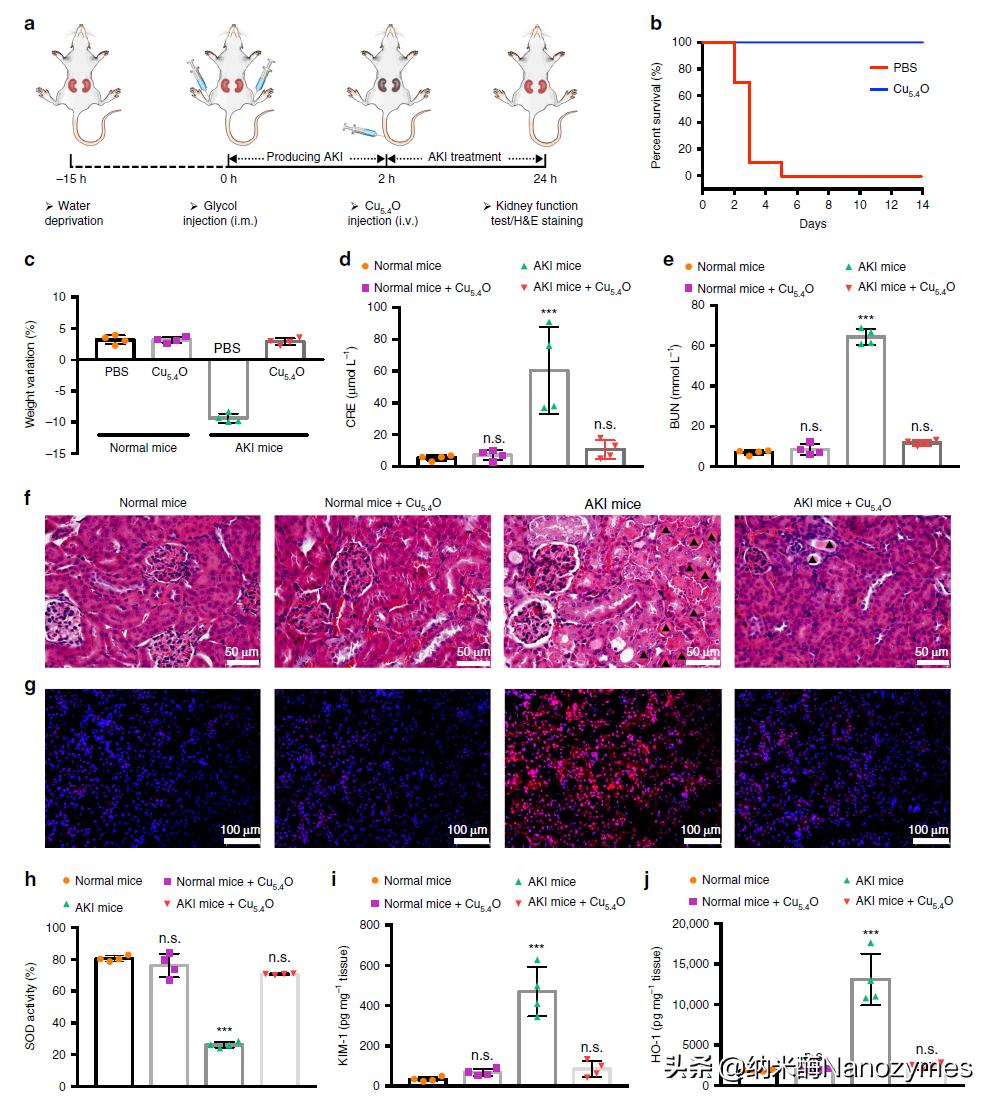
图 7 Cu5.4O USNPs对急性肾损伤AKI小鼠的体内治疗情况 a. AKI小鼠模型的建立及治疗方案示意图; b. 不同治疗的AKI小鼠生存曲线; c. Cu5.4O USNPs治疗24h后AKI小鼠的体重变化; d-e. Cu5.4O USNPs治疗24h后AKI小鼠血清CRE, BUN水平; f. 各组小鼠肾脏的H&E染*图色**像; g. 各组小鼠肾脏组织的荧光染*图色**像; h-j. 各组小鼠肾脏组织SOD, KIM-1, HO-1水平。
为了评估Cu5.4O USNPs的体内治疗效果,研究人员建立了急性肾损伤AKI小鼠模型并进行治疗 图7a。如图7b所示,与对照组90%的小鼠在AKI模型建立后5天内死亡相比,Cu5.4O USNPs治疗的AKI小鼠存活时间超过了14天,并且治疗组小鼠体重增长情况也与健康小鼠相似 图7c。此外,治疗组小鼠的两个重要的肾功能指标,BUN和CRE水平也显著低于对照组的AKI小鼠,并且与健康小鼠相比也没有明显差异 图7d, e,表明Cu5.4O USNPs对小鼠AKI有良好疗效。图7f显示,在AKI小鼠的肾组织中可发现许多变性蛋白在小管中沉淀形成的铸型结构,这是肾脏疾病诊断中重要的病理标志,而在Cu5.4O USNPs处理的AKI小鼠中只能观察到少数,这表明Cu5.4O USNPs治疗可保持肾脏组织的完整性。对小鼠肾脏的ROS清除情况的结果显示,与PBS治疗的AKI小鼠相比,Cu5.4O USNPs治疗的小鼠的超氧化物水平明显降低,达到正常小鼠的水平 图7g。图7h显示,Cu5.4O USNPs治疗组小鼠肾脏SOD活性与健康小鼠相似,而对照组AKI小鼠则明显降低。这表明Cu5.4O USNPs在小鼠体内具有抗氧化剂的作用。并且与对照组AKI小鼠相比,治疗组小鼠的肾损伤生物标志物血红素加氧酶-1(HO-1)和肾损伤分子-1(KIM-1)水平也明显降低 图7i, j,与CRE和BUN的结果一致。
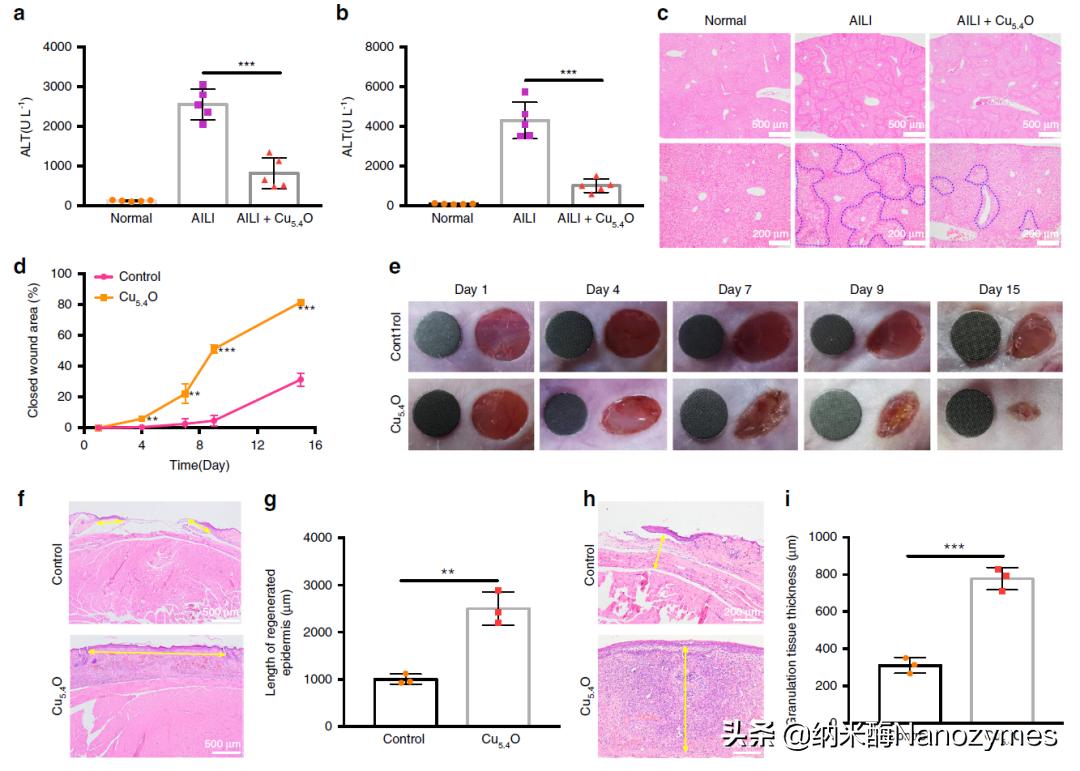
图 8 对急性肝损伤及创面愈合的治疗情况 a, b. 不同治疗24h后AILI小鼠血清ALT, AST水平; c. 各组小鼠肝组织H&E染*图色**像; d, 治疗组与对照组伤口愈合面积比例随时间变化情况; e. 不同时间点小鼠伤口照片 以6mm绿色圆片作为对照; f. 术后15天时的组织学图像; g. 定量测量的术后15天再生表皮长度; h. 术后15天时的组织学图像; i. 定量测量的术后15天肉芽组织厚度。
为了探究Cu5.4O USNPs对AKI以外的ROS相关疾病是否有治疗作用,研究人员建立了扑热息痛APAP诱导的急性肝损伤AILI和全层皮肤损伤模型。图8a、b显示,Cu5.4O UCNPs治疗的AILI小鼠ALT、AST水平显著低于未治疗的AILI小鼠,说明Cu5.4O USNPs对AILI有较好的疗效。肝部的组织学观察进一步证明了这一结果(图8c)。伤口部位的ROS会影响伤口愈合的速度,图8d、e显示,Cu5.4O USNPs组的伤口在术后第4、7、9、15天的愈合情况明显优于对照组,这说明Cu5.4O USNPs可促进伤口愈合。图8f-i显示,Cu5.4O USNPs组新生表皮的长度和肉芽组织的厚度明显大于对照组,进一步证明Cu5.4O USNPs可促进伤口愈合。
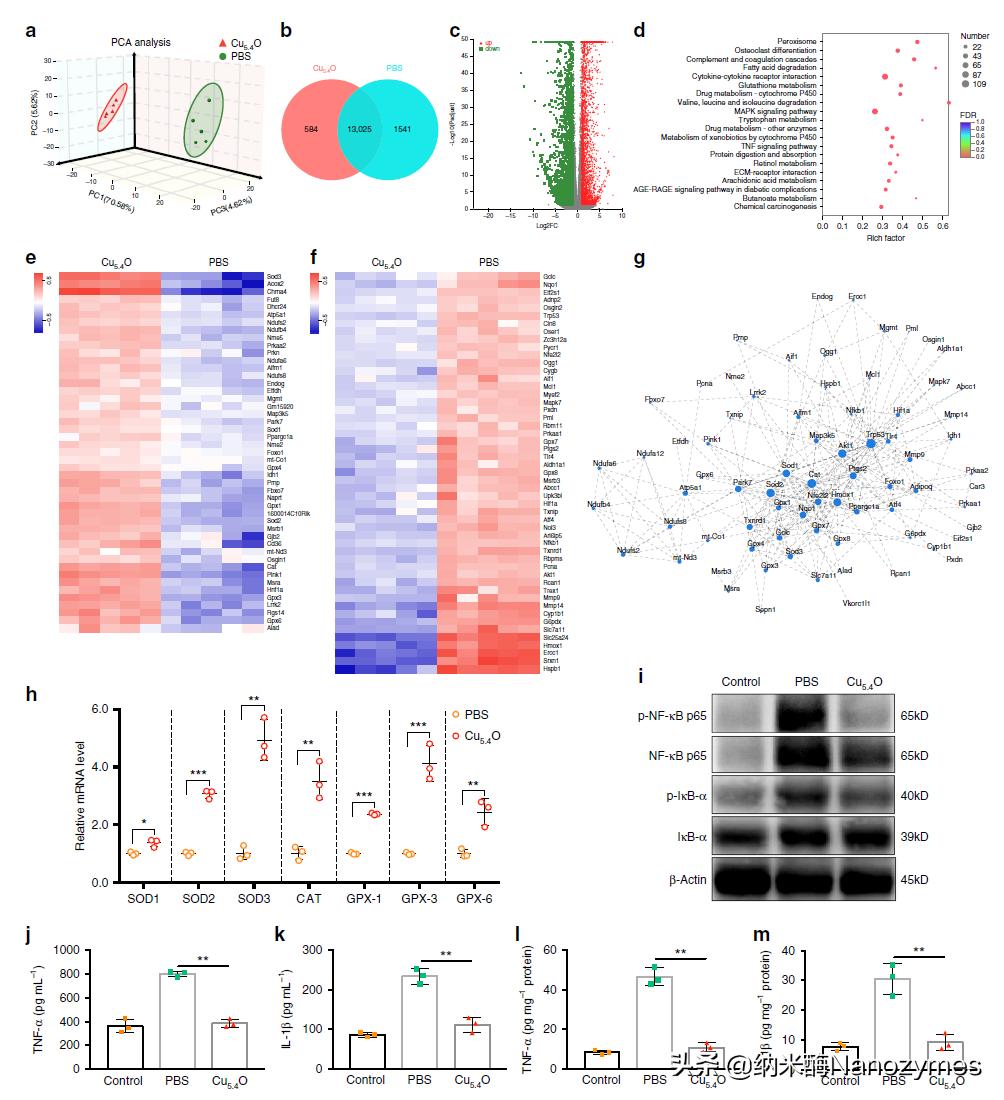
图 9 Cu5.4O USNPs治疗AKI机制研究 a. 两组肾脏差异表达基因的主成分分析(PCA); b. Cu5.4O USNPs和PBS组转录谱; c. 上调基因与下调基因; d, 鉴定差异表达基因的KEGG通路分析; e. Cu5.4O USNPs治疗后上调的参与氧化应激的基因; f. Cu5.4O USNPs治疗后下调的参与氧化应激的基因; g, 参与氧化应激的差异表达基因的蛋白质蛋白质相互作用网络分析; h. qRT-PCR分析抗氧化基因mRNA表达水平; i. Western blot分析AKI小鼠肾组织中phospho-NF-κB p65、总NF-κB p65、phospho-IκB-α和总IκB-α的表达水平; j-m. 血清TNF-α、IL-1β和肾脏TNF-α、IL-1β水平。
为了阐明治疗机制,研究人员对Cu5.4O USNPs和PBS治疗的AKI小鼠进行了转录组学分析。图9a显示两组小鼠的转录谱有显著差异。图9b显示,两组共表达了13025个基因,而Cu5.4 O USNPs处理组表达了584个基因。图9c显示5819个显著差异表达基因中2813个上调,3006个下调。KEGG通路分析 图9d显示,谷胱甘肽(GSH)代谢、MAPK信号通路和TNF信号通路都与Cu5.4O USNPs的治疗机制有关。除了信号通路,Cu5.4O USNPs治疗后,几个重要的抗氧化基因SOD1、SOD2、SOD3、GPX1、GPX3、GPX4、GPX6、CAT表达水平都显著上调 图9e, f。对Cu5.4O USNP治疗后变化的氧化应激相关基因的蛋白质蛋白质相互作用网络进行分析,发现与主导蛋白相连的相邻蛋白中含有SOD1、SOD3、CAT等 图9g,说明这些基因在Cu5.4O USNPs治疗中对ROS清除起重要作用。图9h显示,Cu5.4O处理后小鼠肾脏中抗氧化基因mRNA表达水平显著高于对照组,说明Cu5.4O USNPs可通过保护肾细胞免受ROS损伤来维持AKI中抗氧化基因的高表达。AKI小鼠NF-κB和IκB的磷酸化水平明显增强 图9i,表明NF-κB信号通路在AKI中被激活。对NF-κB信号通路的下游炎症因子检测后发现,Cu5.4O USNPs还可降低血清和组织中TNF-α和IL-1β的水平 图9j-m,说明Cu5.4O USNPs可通过抑制过多促炎因子的产生来保护肾脏组织免受氧化应激的损伤。
三、总结与展望:
本研究中所合成的Cu5.4O USNPs具有粒径超小、肾脏清除速度快、生物相容性好、清除ROS能力强等优点,可模拟胞内抗氧化酶防御体系,对AKI、AILI、伤口愈合这些与ROS相关的疾病有良好疗效,是一种可用于AKI和其他氧化应激相关疾病的治疗的十分有前景的抗氧化剂。
原文: Liu, T.F., et al., Ultrasmall copper-based nanoparticles for reactive oxygen species scavenging and alleviation of inflammation related diseases. Nature Communications, 2020. 11(1).
撰稿:王前
校审:周子君
编辑:周逸夫