
一日三餐是我们日常最平常不过的事情,可是你知道吗?偶尔饿一饿(间歇性禁食)居然可以延年益寿,改善健康状况。那么间歇性禁食的好处有哪些?其潜在的机制是什么?近期新英格兰医学杂志(NEJM)对间歇性禁食进行了综述[1],你想知道的全在这里......

间歇性禁食对代谢的影响:由葡萄糖供能向生酮代谢的转化
葡萄糖和脂肪酸是细胞的主要能量来源,进食后,葡萄糖提供能量,而脂肪则以甘油三酯的方式贮存在脂肪组织中。在禁食期间,甘油三酯分解为脂肪酸和甘油来供能,肝脏将脂肪酸转化为酮体,可在禁食期间为组织供能(尤其是大脑),成为能量的主要来源。
在进食状态下,酮体在血液中的水平很低,人类禁食后的 8 到 12 小时内酮体水平会升高,24 小时会达到 2 到 5mM。啮齿动物禁食开始后的 4 至 8 小时内血浆酮体水平升高,在 24 小时内达到毫摩尔水平 ,目前在人类进行研究中应用最广泛的三种间歇性禁食方案为隔日禁食,5:2 的间歇性禁食(每周禁食2 天)和每天定时禁食[2]。从葡萄糖供能向脂肪酸和酮体供能的代谢转换可导致呼吸交换率的(二氧化碳与氧气之比)降低,这意味着代谢活性的增加及脂肪酸和酮体高效产能[3]。
酮体不仅在禁食期间供能,同时它们也是对细胞和器官功能产生重大影响的强有力的信号分子,调节着许多已知会影响健康和衰老的蛋白质分子的表达活性,包括过氧化物酶体增殖物激活的受体γ共激活因子 1α(PGC-1α),成纤维细胞生长因子等[4-7], 禁食期间产生的酮体通过影响这些主要的细胞信号途径来影响全身代谢。此外,酮体会刺激脑源性神经营养因子的基因表达,对大鼠健康、精神疾病以及神经退行性疾病有影响[8]。
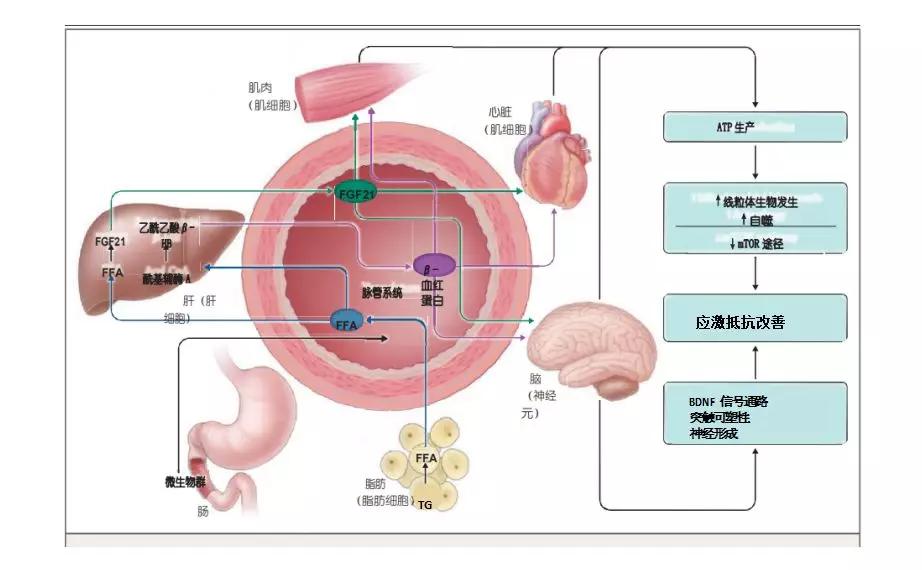
图1.间歇性禁食的代谢适应
那么,间歇性禁食得益于代谢转换的比例是多少?得益于体重减轻的比例是多少呢?许多研究表明,间歇性禁食的一些获益与其对体重减轻的影响无关。这些获益包括改善血糖调节、改善血压及心率、提高运动耐力 以及减少腹部脂肪[9,10]。
间歇性禁食增加机体对应激抵抗,潜在机制不简单
一些研究[11,12]结果显示,大部分器官系统都会对间歇性禁食做出反应,使机体能够忍受或克服这一挑战,然后恢复体内平衡。反复暴露于禁食期会带来持久的适应性反应,从而赋予机体抵抗后续挑战的能力。细胞通过参与协调适应性应激反应来响应间歇性禁食,这些过程包括抗氧化物生成,DNA修复,蛋白质质量控制,线粒体生物合成、自噬以及炎症反应下调。
在动物中,进行间歇性禁食方案后整个身体和大脑细胞都表现出更好的功能并对广泛潜在的损害展现出良好的抵抗力,其中包括对代谢、氧化、离子、创伤和蛋白毒性应激损害的抵抗 。
此外,间歇性禁食可激活自噬和线粒体吞噬,同时抑制mTOR(雷帕霉素的哺乳动物靶标)蛋白合成途径,进而去除氧化损伤的蛋白质和线粒体并且回收未损坏的分子成分,也会暂时减少整体蛋白质的合成以节约能量和原料。然而,饮食过量且久坐的人却无法激活或抑制这些途径[12]。
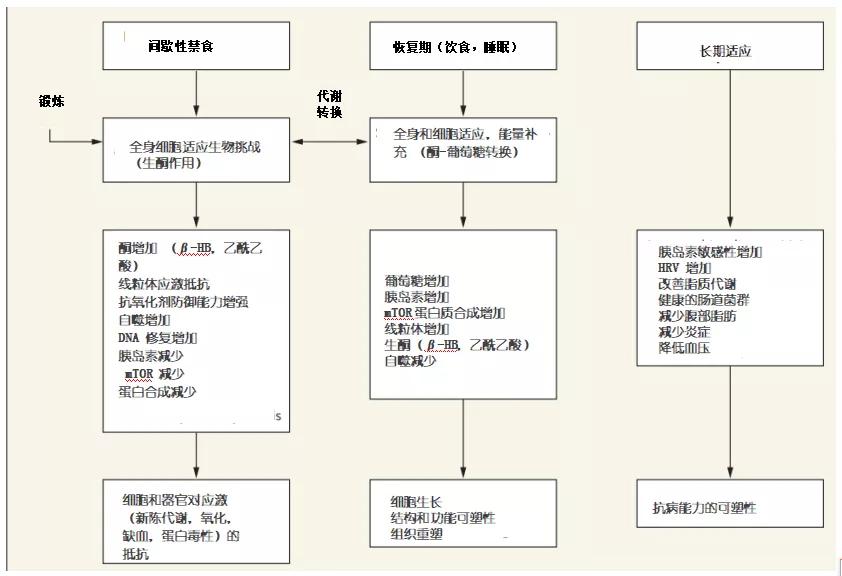
图2 间歇性禁食代谢转换改善器官功能、对抗应激和增加对疾病病抵抗力的细胞和分子机制。
间歇性禁食对健康和衰老的影响如何?
直到现在,热量限制和间歇性禁食的研究都集中在延缓衰老和延长寿命上。近一个世纪的热量限制的动物研究总的结论是减少食物摄入量可以有效地延长寿命。最早的一项间歇性禁食研究显示从幼年开始,每隔一天进行一次喂食就可以使大鼠的平均寿命延长 80%。然而,热量限制对健康和寿命的影响程度却大不相同,并且受性别,饮食,年龄和遗传因素的影响[13]。肥胖与寿命之间存在反比关系
[14],这表明在严格限制热量摄入的情况下,寿命短的动物脂肪减少得更多,并且迅速转变为饥饿,而寿命长的动物脂肪减少却最少(代谢转化的高效产能作用)。
在人类中,间歇性禁食可以减轻肥胖,改善胰岛素抵抗、血脂异常,高血压和炎症[15],并且间歇性禁食对健康的改善作用似乎比单纯热量摄入减少的程度更大。在一项试验中,16 名健康参与者采取隔天禁食的方案 22 天体重减少了 2.5%和脂肪降低4%,空腹胰岛素水平降低了57%[16]。另外两项试验中,超重妇女(每个试验中约有 100 名妇女)分为 5:2 的禁食方案或每日减少 25%的热量摄入。两组中的妇女在 6 个月内的体重减轻相同,但5:2间歇性禁食组中妇女的胰岛素敏感性增加幅度更大,腰围减少幅度更大[10,17]。
间歇性禁食改善身体机能,促进认知功能改善
在动物和人类中,间歇性禁食都显示出改善身体机能的作用,例如,尽管体重相似,但隔天禁食的小鼠比无限制进食的小鼠具有更好的跑步耐力。限时喂养或隔日禁食的动物身体的平衡性和协调性也得到了改善[18]。每天禁食16小时的年轻男子在2 个月的抵抗训练中脂肪减少,同时保证了肌肉质量[19]。
在改善认知方面,动物研究表明,间歇性禁食可增强多个领域的认知能力,包括空间记忆,联想记忆和工作记忆[20]。隔日禁食和每日热量限制可以逆转肥胖、糖尿病和神经炎症对空间学习和记忆的不利影响。一项临床研究显示短期热量摄入限制的老年人言语记忆得到了改善[21]。一项在轻度认知障碍的超重成年人进行的研究结果显示12 个月的热量限制可改善他们的言语记忆,执行能力和整体认知功能[22]。最近,一项大型的多中心随机临床试验表明, 2 年的每天热量限制可显着改善工作记忆[23]。当然,在老年人中进行间歇性禁食对认知功能的影响进一步的研究显得尤为必要,尤其是目前还缺乏影响大脑衰老和神经退行性疾病的治疗药物[12]。
间歇性禁食在临床多种疾病都显示出良好获益
临床前的研究结果一致显示间歇性禁食在动物模型中对多种慢性疾病(包括肥胖症,糖尿病,心血管疾病,癌症和神经退行性脑疾病)具有良好的获益。在肥胖和糖尿病病方面,两项最新研究表明,每日热量限制或 4:3 的间歇性禁食(每周3次24小时禁食)可逆转糖尿病前期患者或 2 型糖尿病患者的胰岛素抵抗[24-25],在心血管疾病改善上,间歇性禁食可改善动物和人类心血管健康的多项指标,包括血压、静息心率、高密度脂蛋白胆固醇(HDL-C)和低密度脂蛋白胆固醇(LDL-C),甘油三酸酯,葡萄糖和胰岛素的水平[26-29]。
大量动物研究表明,每日热量限制或隔日禁食可减少啮齿动物正常衰老过程中自发性肿瘤的发生,并抑制多种类型肿瘤的生长,同时增加肿瘤对化疗和放疗的敏感性[30]。在癌症患者中进行的间歇性禁食的临床研究已经完成或正在进行中,大多数初步研究都集中在间歇性禁食的依从性、不良反应和生物学特征上。例如,一项在前列腺癌男性进行的研究显示每日热量限制显示出极好的依从性(95%)并且没有不良事件[31]。正在进行的临床试验专注于乳腺癌,卵巢癌,前列腺癌,子宫内膜癌,结直肠癌和胶质细胞瘤患者的间歇性禁食。特定的间歇性禁食方案因研究而异,但均需要在化疗期间实施间歇性禁食方案,目前尚无研究确定间歇性禁食是否会影响人类癌症的复发。
在神经退行性脑疾病方面,目前已有充分的临床前证据表明,隔日禁食可延缓动物模型阿尔茨海默氏病和帕金森氏病的发作和进展[12]。目前尚缺乏在患有神经退行性疾病风险或受其影响的人中进行的间歇性禁食临床对照试验数据。理想情况下,干预应在疾病的早期开始,并持续足够长的时间以检验干预措施对疾病的改善作用(例如,为期1年的研究)。此外,目前还有一些研究[33-35]显示间歇性禁食在哮喘,多发性硬化症和关节炎乃至外科手术和缺血性组织损伤中发挥着良好作用。
间歇性禁食好处多,实际应用的阻碍却困难重重!
尽管越来越多的证据表明间歇性禁食的健康获益,并且适用于许多疾病,但多种因素阻碍了这种饮食方式在社区和患者中的广泛应用。首先,在我们的文化中,一日三餐加零食的饮食习惯已根深蒂固,以致于饮食方式的改变很少会被患者或医生所采纳,发达国家丰富的食品和广泛的营销也是需要克服的主要障碍。其次,在转为间歇性禁食的过程中,许多人在禁食期间会感有饥饿感,出现易怒和注意力不集中的情况,即便这些最初的不良反应通常会在1个月内消失。
最后大多数医生并没有接受过特定间歇性禁食干预的培训。为了达到每天禁食 16 至 18 个小时的目的,医生可以建议患者在几个月的时间内逐渐减少每天进食的时间范围,或者医生可以推荐 5:2 的间歇性禁食方案,然而整个过程需要咨询营养师以确保患者的营养需求,并提供持续的咨询和教育。与所有生活方式干预措施一样,医生需要提供足够的信息,持续的沟通和支持并且进行定期强化,这对间歇性禁食的干预实施非常重要。
间歇性禁食获益多,未来值得期待
总而言之,临床前和临床研究均表明,间歇性禁食对健康状况具有广泛的获益,例如肥胖,糖尿病,心血管疾病,癌症和神经系统疾病。临床研究主要干预时间相对较短,仅为期数月。人们是否坚持间歇性禁食多年,并像动物模型中那样获益值得探讨;此外,临床研究主要集中于超重的年轻人和中年人,我们无法将这些研究中观察到的间歇性禁食的获益和安全性推广到其他年龄组;了解间歇性禁食与广泛的健康获益的潜在机制将有助于模拟间歇性禁食疗效的靶向药物开发,从而帮助那些不愿进行间歇性禁食的患者在不改变饮食模式的基础上获得间歇性禁食的好处。
参考文献:
[1]Rafael de Cabo, Mark P. Mattson, Effects of Intermittent Fasting on Health, Aging, and Disease.N Engl J med 381;26
[2]Anton SD, Moehl K, Donahoo WT, et al. Flipping the metabolic switch: understanding and applying the health benefits of fasting. Obesity (Silver Spring) 2018;26:254-68.
[3]Fisher FM, Maratos-Flier E. Understanding the physiology of FGF21. Annu Rev Physiol 2016;78:223-41.
[4]Longo VD, Mattson MP. Fasting: molecular mechanisms and clinical applications. Cell Metab 2014;19:181-92.
[5]Gälman C, Lundåsen T, Kharitonenkov A, et al. The circulating metabolic regulator FGF21 is induced by prolonged fasting and PPARalpha activation in man. Cell Metab 2008;8:169-74.
[6] Imai SI, Guarente L. It takes two to tango: NAD+ and sirtuins in aging/longevity control. NPJ Aging Mech Dis 2016;2: 16017. 25.
[7]Lee HC. Physiological functions of cyclic ADP-ribose and NAADP as calcium messengers. Annu Rev Pharmacol Toxicol 2001;41:317-45.. Lee HC. Physiological functions of cyclic ADP-ribose and NAADP as calcium messengers. Annu Rev Pharmacol Toxicol 2001;41:317-45.
[8]Mattson MP, Moehl K, Ghena N, Schmaedick M, Cheng A. Intermittent metabolic switching, neuroplasticity and brain health. Nat Rev Neurosci 2018;19: 63-80.
[9] Wright C, Pegington M, et al. The effect of intermittent energy and carbohydrate restriction v. daily energy restriction on weight loss and metabolic disease risk markers in overweight women. Br J Nutr 2013;110:1534-47.
[10]Harvie M, Wright C, Pegington M, et al. The effect of intermittent energy and carbohydrate restriction v. daily energy restriction on weight loss and metabolic disease risk markers in overweight women. Br J Nutr 2013;110:1534-47.
[11]Anton SD, Moehl K, Donahoo WT, et al. Flipping the metabolic switch: understanding and applying the health benefits of fasting. Obesity (Silver Spring) 2018; 26:254-68.
[12]Mattson MP, Arumugam TV. Hallmarks of brain aging: adaptive and pathological modification by metabolic states. Cell Metab 2018;27:1176-99.
[13]Mattison JA, Colman RJ, Beasley TM, et al. Caloric restriction improves health and survival of rhesus monkeys. Nat Commun 2017;8:14063.
[14]Liao CY, Rikke BA, Johnson TE, Gelfond JA, Diaz V, Nelson JF. Fat maintenance is a predictor of the murine lifespan response to dietary restriction. Aging Cell 2011;10:629-39.
[15]Redman LM, Smith SR, Burton JH, Martin CK, Il’yasova D, Ravussin E. Metabolic slowing and reduced oxidative damage with sustained caloric restriction support the rate of living and oxidative damage theories of aging. Cell Metab 2018;27(4):805.e4-815.e4.
[16]Heilbronn LK, Smith SR, Martin CK, Anton SD, Ravussin E. Alternate-day fasting in nonobese subjects: effects on body weight, body composition, and energy metabolism. Am J Clin Nutr 2005;81:69- 73.
[17]Harvie MN, Pegington M, Mattson MP, et al. The effects of intermittent or continuous energy restriction on weight loss and metabolic disease risk markers: a randomized trial in young overweight women. Int J Obes (Lond) 2011;35:714-27.
[18]Chaix A, Zarrinpar A, Miu P, Panda S. Time-restricted feeding is a preventative and therapeutic intervention against diverse nutritional challenges. Cell Metab 2014;20:991-1005.
[19]Moro T, Tinsley G, Bianco A, et al. Effects of eight weeks of time-restricted feeding (16/8) on basal metabolism, maximal strength, body composition, inflammation, and cardiovascular risk factors in resistance-trained males. J Transl Med 2016;14:290.
[20]Wahl D, Coogan SC, Solon-Biet SM, et al. Cognitive and behavioral evaluation of nutritional interventions in rodent models of brain aging and dementia. Clin Interv Aging 2017;12:1419-28.
[21]Witte AV, Fobker M, Gellner R, Knecht S, Flöel A. Caloric restriction improves memory in elderly humans. Proc Natl Acad Sci U S A 2009;106:1255-60.
[22]Horie NC, Serrao VT, Simon SS, et al. Cognitive effects of intentional weight loss in elderly obese individuals with mild cognitive impairment. J Clin Endocrinol Metab 2016;101:1104-12
[23]Leclerc E, Trevizol AP, Grigolon RB, et al. The effect of caloric restriction on working memory in healthy non-obese adults. CNS Spectr 2019 April 10 (Epub ahead of print).
[24]Furmli S, Elmasry R, Ramos M, Fung J. Therapeutic use of intermittent fasting for people with type 2 diabetes as an alternative to insulin. BMJ Case Rep 2018; 2018:bcr-2017-221854.
[25]Sutton EF, Beyl R, Early KS, Cefalu WT, Ravussin E, Peterson CM. Early timerestricted feeding improves insulin sensitivity, blood pressure, and oxidative stress even without weight loss in men with prediabetes. Cell Metab 2018;27(6):1212- 1221.e3.
[26]Wan R, Camandola S, Mattson MP. Intermittent food deprivation improves cardiovascular and neuroendocrine responses to stress in rats. J Nutr 2003;133: 1921-9.
[27]Fontana L, Meyer TE, Klein S, Holloszy JO. Long-term calorie restriction is highly effective in reducing the risk for atherosclerosis in humans. Proc Natl Acad Sci U S A 2004;101:6659-63.
[28]Most J, Gilmore LA, Smith SR, Han H, Ravussin E, Redman LM. Significant improvement in cardiometabolic health in healthy nonobese individuals during caloric restriction-induced weight loss and weight loss maintenance. Am J Physiol Endocrinol Metab 2018;314:E396-E405.
[29]Lefevre M, Redman LM, Heilbronn LK, et al. Caloric restriction alone and with exercise improves CVD risk in healthy non-obese individuals. Atherosclerosis 2009;203:206-13.
[30]Hursting SD. When less may be more: calorie restriction and response to cancer therapy. BMC Med 2017;15:106.
[31]Demark-Wahnefried W, Nix JW, Hunter GR, et al. Feasibility outcomes of a presurgical randomized controlled trial exploring the impact of caloric restriction and increased physical activity versus a wait-list control on tumor characteristics and circulating biomarkers in men electing prostatectomy for prostate cancer. BMC Cancer 2016;16:61.
[32]Nencioni A, Caffa I, Cortellino S, Longo VD. Fasting and cancer: molecular mechanisms and clinical application. Nat Rev Cancer 2018;18:707-19.
[33]Choi IY, Piccio L, Childress P, et al. A diet mimicking fasting promotes regeneration and reduces autoimmunity and multiple sclerosis symptoms. Cell Rep 2016;15:2136-46.
[34]Cignarella F, Cantoni C, Ghezzi L, et al. Intermittent fasting confers protection in CNS autoimmunity by altering the gut microbiota. Cell Metab 2018;27(6):1222.e6- 1235.e6.
[35]Van Nieuwenhove Y, Dambrauskas Z, Campillo-Soto A, et al. Preoperative very low-calorie diet and operative outcome after laparoscopic gastric bypass: a randomized multicenter study. Arch Surg 2011;146:1300-5.