不想错过界哥的推送?
戳上方蓝字“医学界肿瘤频道”关注我们
并点击右上角“···”菜单,选择“设为星标”
免疫联合靶向治疗能否克服微卫星稳定结直肠癌(CRC)的免疫抵抗?姜黄素能否防治胃癌?炎症是如何导致胃癌的?请看第4期胃肠食管肿瘤资讯。
文丨Cindy
来源丨医学界肿瘤频 道
本期提要
-
IMblaze370试验:MEK/PD-L1*制剂抑**三线治疗结直肠癌失败
-
姜黄素或有助防治胃癌
-
“炎症如何导致胃癌”的谜团终于揭开
一
IMblaze370试验: MEK/PD-L1*制剂抑**三线治疗结直肠癌失败
通常情况下,微卫星稳定转移性CRC对免疫治疗无反应。那么免疫治疗联合靶向治疗会有怎样的结果呢?
III期临床试验IMblaze370给出了答案:免疫治疗联合靶向治疗与标准三线治疗相比,未能改善微卫星稳定转移性CRC患者的生存 [1,2]。
研究结果近日发表于《Lancet Oncology》。
IMblaze 370是一项随机、对照、多中心、开放标签、3期试验,在11个国家的73个学术医疗中心开展,招募对象为年龄至少18岁、无法切除的局部晚期或转移性CRC、基线东部肿瘤协作组体能状态评分0-1、接受至少2种全身化疗方案后疾病进展或不耐受的患者。
结果显示,入组363例患者,阿特珠单抗(PD-L1*制剂抑**)联合cobimetinib(MEK*制剂抑**)组为183例,阿特珠单抗组为90例,瑞戈非尼组为90例。
-
联合治疗组患者的中位总生存期并不优于瑞戈非尼组(8.9个月 vs 8.5个月,HR 1.00,P=0.99),而阿特珠单抗组总生存(7.1个月)劣于瑞戈非尼组(HR 1.19,P=0.34)。
-
联合治疗组和阿特珠单抗组的中位无进展生存期均为1.9个月,而瑞戈非尼组为2.0个月(图1)。联合治疗组有3%患者获得客观缓解,而两单药组各有2%患者获得客观缓解。
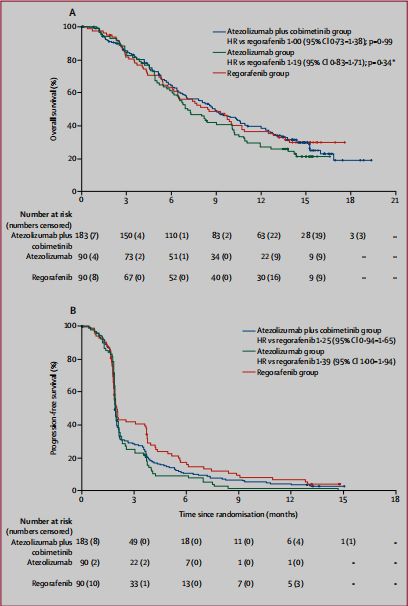
意向治疗人群的总生存(A)和无进展生存期(B)
“尽管临床前数据支持MEK / PD-L1*制剂抑**,但研究结果表明PD-L1免疫检查点和MAPK介导的免疫抑制的双重抑制,不足以对免疫豁免型(immune-excluded)肿瘤产生抗肿瘤免疫反应,如微卫星稳定转移性CRC。”研究者指出,该抗肿瘤反应失败可能是因为存在绕过MEK*制剂抑**抑制MAPK通路的替代机制。
在同期述评中,评论者指出,研究结果似乎终止了MEK抑制可克服微卫星稳定CRC患者免疫抵抗的观点。因为对潜在生物学理论和支持性初步临床结果抱有极大的科学兴趣和热情,所以IMblaze370试验的阴性结果非常令人失望。但是,关注这种意外失败的潜在原因势在必行。
他还指出,关于MEK抑制的免疫调节作用实际上并没有定论。一些数据报道了其抑制T淋巴细胞增殖反应、抗原特异性扩增以及损伤树突细胞对抗原的加工,这或可解释该试验的阴性结果。
他还质疑该试验缺乏生物标志物,并表示,对于微卫星稳定CRC的异质性肿瘤特征,可能需要“独特的免疫调节策略”来恢复免疫原性并产生抗肿瘤免疫应答。
二
姜黄素或有助防治胃癌
姜黄素广泛用于赋予食物颜色和味道,除此之外,还有什么作用?
巴西研究人员发现,姜黄素和其他生物活性化合物可能有助预防或抗击胃癌 [3]。
研究结果发表于《Epigenomics》。

研究的第一作者、巴西帕拉联邦大学(UFPA)的Danielle Queiroz Calcagno教授表示,姜黄素、胆钙化醇(一种维生素D)、白藜芦醇(多酚)和槲皮素等或可预防或抗击胃癌,它们是组蛋白活性的天然调节剂。
研究发现,来自胃癌患者的细胞表现出组蛋白乙酰转移酶(HAT)和组蛋白脱乙酰酶(HDAC)表达模式的改变。这些改变是表观遗传的,并且影响许多肿瘤(包括胃癌)基因组的结构和完整性。
此外,最近的研究表明,营养素和生物活性化合物可调节HAT和HDAC的活性,基于此,UNIFESP和UFPA的研究人员着手识别可能影响组蛋白乙酰化的因素,以便帮助预防胃癌,甚至治疗胃癌。
结果发现,除姜黄素外,其他化合物包括胆钙化醇、白藜芦醇(主要存在于葡萄籽和红葡萄酒)、槲皮素(苹果、西兰花和洋葱中含量丰富)、香叶醇(从木棉树、印度藤黄的树皮中分离提取)和丁酸钠(由肠道细菌通过膳食纤维发酵产生)均在调节组蛋白活性中发挥重要作用。
“这些化合物可通过促进或抑制组蛋白乙酰化,来激活或抑制参与胃癌发生的基因,”Calcagno说。例如,姜黄素主要通过抑制HAT和HDAC来影响组蛋白修饰,从而抑制癌细胞增殖并诱导细胞凋亡(程序性细胞死亡)。
三
“炎症如何导致胃癌”的谜团终于揭开
早在1982年,研究人员报告了慢性胃炎与胃幽门螺杆菌(Hp)之间的关联。随之一系列研究表明,Hp除参与胃炎外,也是消化性溃疡和胃癌发生的重要因素。虽然细菌和疾病之间的关联是明确的,但关于Hp引起胃癌的确切机制仍存争论。
将近40年后,目前日本金泽大学和日本医学研究与发展局的研究人员终于发现,Hp感染引起的炎症可增强NOXO1蛋白表达,从而诱导胃上皮干细胞增殖,并导致胃肿瘤 [4]。
研究最近发表于《Oncogene》。
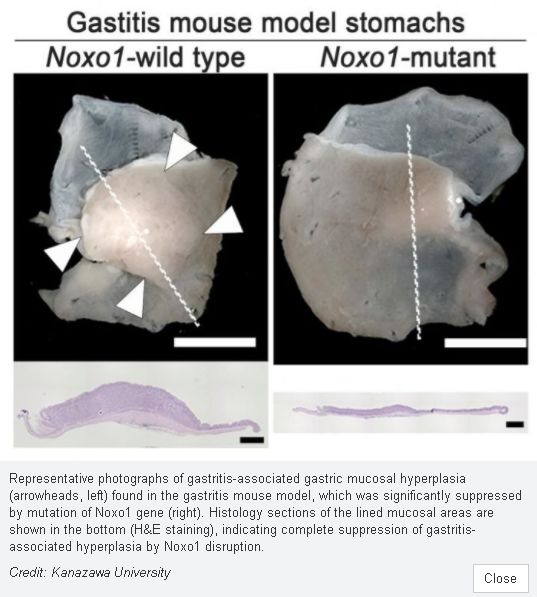
胃炎小鼠模型的胃炎相关胃黏膜增生及黏膜组织切片H&E染色
炎症如何导致胃癌?研究人员描述了其揭开谜团的过程。
研究人员表示,肿瘤坏死因子α(TNF-α)是一种引起炎症的细胞因子,他们之前发现,TNF-α通过激活一种叫做NOXO1的蛋白来促进胃肿瘤的形成,但不知道NOXO1如何在胃中诱导肿瘤形成。
NOXO1是NOX1复合物蛋白的一种成分,其可产生组织损伤分子即活性氧(ROS)。更准确地说,由ROS分子引起的氧化应激可导致胃细胞DNA的突变,从而导致肿瘤形成。然而,由Hp感染引起的炎症也产生ROS,增加胃的氧化应激。
在新发表的研究中,研究人员指出,炎症导致过多的NOX1复合物蛋白产生,以回应来自NF-κB的信号。NF-κB是一种启动对抗应激或细菌感染的基因的调节蛋白,也是炎症反应的主要参与者。然而,最重要的是,他们发现NOX1/ROS信号通路导致胃上皮干细胞不受控制地增殖,从而导致肿瘤形成。
了解到这一点,研究人员使用药物来抑制NOX1复合物的活性,这立即阻止了胃癌细胞的生长。更令人兴奋的是,在小鼠胃炎模型中,通过破坏NOXO1,竟然阻止了上皮干细胞的增殖。
“我们终于证明,炎症可增强NOXO1的表达,从而诱导胃上皮干细胞增殖,导致胃肿瘤,”研究人员解释道。“胃癌是全球第四大常见癌症,死亡率居第二位。若能够在原发部位破坏NOX1/ROS信号通路,则可能防止这种侵袭性疾病的发展。”
参考文献
[1]Eng C, Kim TW, Bendel J, et al. Atezolizumab with or without cobimetinib versus regorafenib in previously treated metastatic colorectal cancer (IMblaze370): a multicentre, open-label, phase 3, randomised, controlled trial[J]. Lancet Oncol. 2019 Apr 16.[Epub ahead of print]
[2]https://www.medpagetoday.com/hematologyoncology/coloncancer/79410
[3]https://medicalxpress.com/news/2019-04-highlights-anti-tumor-curcumin-stomach-cancer.html
[4]https://www.sciencedaily.com/releases/2019/04/190416094121.htm
有奖调研
为了了解中国肿瘤医生PD-1/PD-L1*制剂抑**的使用与认知情况,医学界肿瘤频道诚邀您参与下方调研,参与者有机会获得《临床肿瘤内科手册(第6版)》哦!快来扫描海报内二维码,速速参与吧!
征 稿
欢迎投稿到小编邮箱:zl@yxj.org.cn
请注明:【投稿】医院+科室+姓名
来稿以word文档形式,其他不予考虑
你在看我吗?
↓↓↓↓