编者按:本文中,美国堪萨斯大学癌症中心的Anwaar Saeed博士介绍了微卫星稳定型(MSS)胃食管癌的精准免疫治疗进展。
概要
CheckMate-649和KEYNOTE-590试验验证了将PD-1*制剂抑**纳武利尤单抗和帕博利珠单抗分别加到入基于5-FU的化疗方案中用于化疗初治的晚期胃食管癌(GE)患者的优势。这种优势可能局限于PD-L1联合阳性评分(CPS)较高的患者。
其他具有免疫治疗预测价值的实验标志物包括肿瘤突变负荷、DNA损伤反应基因突变、EB病毒和某些基因表达谱。
未来的试验设计必须考虑使用的IO药物组合和治疗人群;在这种疾病中,必须确定经典化疗之外的新型IO组合。
尽管多种免疫疗法(IO)药物研发人员正在推进免疫检查点*制剂抑**用于晚期食管胃癌患者,但为患者亚群量身定制合适的药物组合或IO联合方案仍是一个有意义的争议领域。
最大的障碍在于这类疾病具有分子异质性,直至最近,在许多关键的临床试验中,这些疾病都被归为一类。除了典型的解剖分类外,快速发展的肿瘤基因组下一代测序项目已经发现了多个具有不同基因组特征及预后和预测意义的分子亚群。在美国,癌症基因组图谱已被确定了多种分类,包括EB病毒(EBV)亚型、微卫星不稳定性(MSI)-高(错配修复缺陷)亚型、染色体不稳定性亚型和基因组稳定亚型,每一种都有不同的分子谱[1]。
CheckMate-649和KEYNOTE-590
在未接受化疗的晚期GE癌患者中,两项关键试验CheckMate-649(胃和GE交界部腺癌)和KEYNOTE-590(食管和GE交界部鳞状细胞癌和腺癌)验证了将PD-1*制剂抑**纳武利尤单抗和帕博利珠单抗分别联合基于5-FU化疗方案的优势[2,3]。虽然这两项试验都达到了OS终点,且纳武利尤单抗和帕博利珠单抗因此获FDA批准,但亚组分析结果表明,PD-L1联合阳性评分(CPS)较高的患者存在生存优势差异。
CheckMate-649试验中,PD-L1 CPS≥5患者和总人群(CPS≥0)OS的HR分别为0.7和0.8。2022年ASCO GI年会上公布了CheckMate-649试验更长随访时间的生存结果,揭示CPS<10患者中缺乏总生存益处,HR=0.92[4]。
关于KEYNOTE-590研究发表的结果也出现了类似的争论。尽管该研究在CPS≥10和总人群达到了主要生存终点,但关于PD-L1 CPS水平较低的患者的疗效引起了人们的关注。最近一项分析使用KMSubtraction来检索PD-L1亚组的数据,这些数据以前在关键试验的原始文献中没有报道过。结果显示,PD-L1低表达的胃癌、食管癌和GE癌(包括CPS1~9.5)患者中,纳武利尤单抗或帕博利珠单抗联合化疗中并无益处[5]。
尽管关于PD-L1表达作为免疫生物标志物的强度存在一些争议——特别是当其与诸如PD-L1表达的肿瘤内和肿瘤间异质性等已知因素相关时[6],但现有的数据表明,大多数专家都同意,使用CPS方法的PD-L1表达是最有效的可用标志物[2,3,7,8]
KEYNOTE-811研究和HER2阳性疾病的数据
与GE癌症试验中的“所有参与者”相比,聚焦于HER2阳性组的KEYNOTE-811研究显示,在曲妥珠单抗加化疗的ToGA试验方案中加入帕博利珠单抗取得了重大胜利[9]。该试验的第一个中期结果显示,客观缓解率(ORR)为74.4%,中位缓解持续时间为10.6个月;这些结果导致FDA最近加速批准该方案。PD-L1 CPS是否也可以将这一HER2阳性人群细分为高应答者和低应答者尚不清楚,我们热切等待KEYNOTE-811的详细结果。
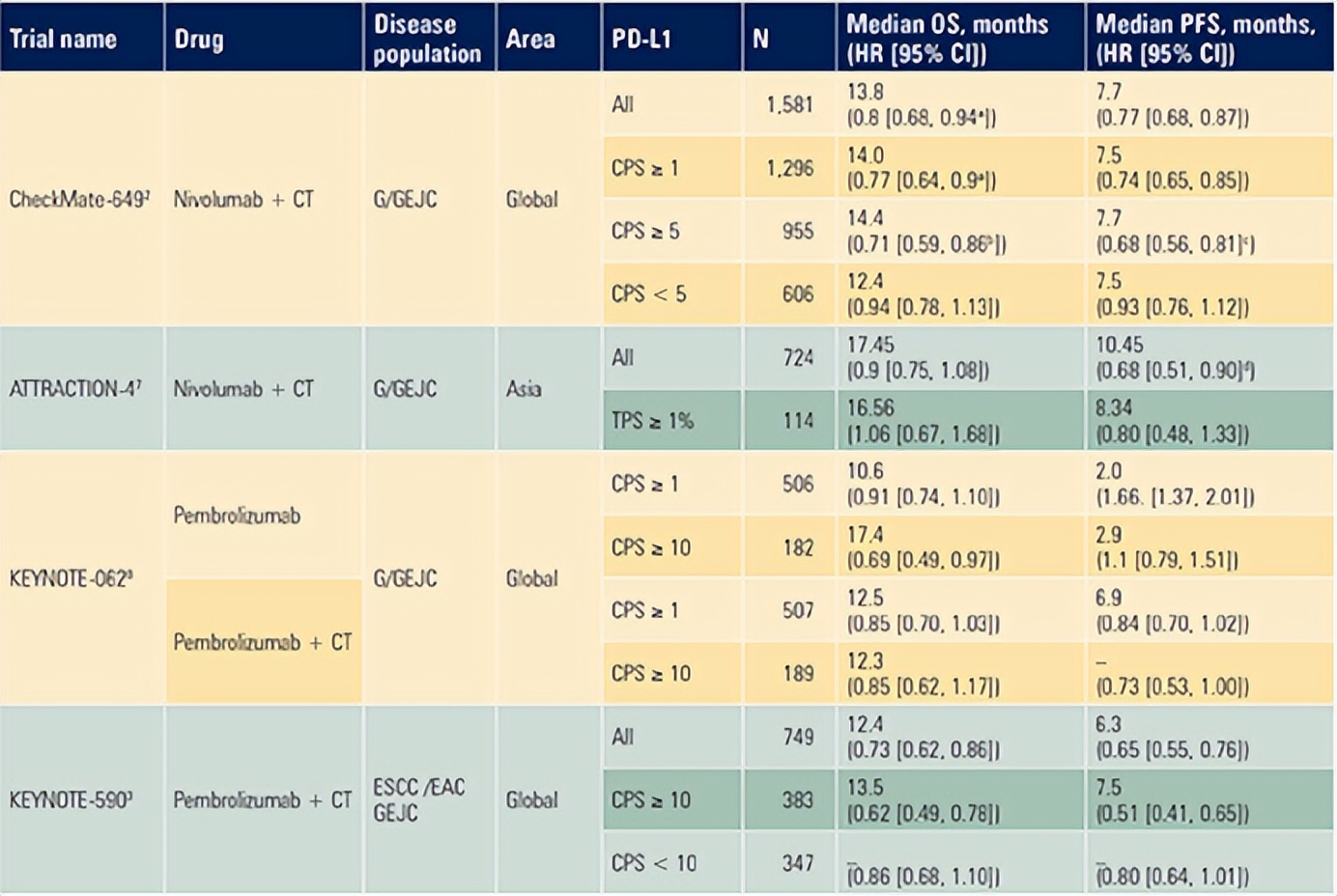
图1. 一线GE肿瘤中具有里程碑意义的IO试验(根据PD-L1表达分析生存结果)
PD-L1以外的其他IO分子标志物
肿瘤突变负荷(TMB)是FDA批准的组织不确定类的IO标志物。批准是基于FoundationOne CDx检测,该检测使用每兆酶10个突变的截断值来定义高TMB。由于KEYNOTE-158的数据主要来自非小细胞肺癌患者,而不包括上消化道恶性肿瘤,如GE癌,因此该截断值对GE癌和其他实体恶性肿瘤的适用性存在很大争议[10]。尽管如此,未来还需要在前瞻性试验来检验TMB在这一人群中的可预测性,并确定确切的临界值来看到有意义的益处。
DNA损伤反应(DDR)基因突变已被提出作为IO反应的其他可能标志物,并在一些正在进行的试验中进行评估[11,12]。尽管在其他肿瘤类型中存在更有力的证据支持这一观点,但GE癌的证据大多是回顾性的,需要验证。此外,与其他IO标记物(如MSI-H和高TMB)的重叠程度需要研究,因为这将使作为独立IO预测标记物的DDR改变能够更好地评估。
一项Ⅱ期试验显示,在胃癌中,EBV与显著的ORR为100%相关[13]。EBV是否为IO反应的独立预测因子,以及其与其他假定标志物如TMB、MSI和DNA损伤反应的相互作用,我们尚不清楚,需要进一步评估。
一些小规模的GE癌症试验正在检验用于识别炎症性肿瘤免疫微环境的一些预先确定的基因(基因表达谱),例如,KEYNOTE-012和KEYNOTE-059正在检验是否干扰素γ基因表达谱倾向于与更高的ORR相关[14,15]。其他研究开发了提高基因表达谱预测能力的新方法,例如通过使用人工智能。一个值得注意的例子是,在包括40%胃癌和26%食管癌的泛癌人群中,通过接受者操作曲线的约登指数评估,RNA特征在IO反应预测能力方面优于PD-L1表达、TMB和MSI状谱[16]。
未来展望
综上所述,多个已发表的试验结果要求优化未来的试验设计,以探讨使用的IO药物组合和治疗人群。例如,避免在1个试验中对2个肿瘤组织进行分组,并根据特定的分子亚群进行设计,将极大地减少分析结果的细微差别,并促进该领域有效的有意义的药物开发。这些考虑也将解决全面获批后带来的安全和财务危害问题。
此外,在这种疾病中,除了传统的化疗外,确定新的IO组合方案是一个巨大的未满足的需求。尽管与CTLA-4*制剂抑**组合未能在前线和后线显示临床协同作用[17],但目前研究人员正在测试其他新型药物,其中包括VEGF受体多酪氨酸激酶*制剂抑**、抗体药物偶联物和CAR-T细胞[18]。
参考文献
(上下滑动可查看)
1.Park R, Da Silva LL, Saeed A. Immunotherapy predictive molecular markers in advanced gastroesophageal cancer: MSI and beyond. Cancers (Basel). 2021;13:1715.
2.Janjigian YY, Shitara K, Moehler M, et al. First-line nivolumab plus chemotherapy versus chemotherapy alone for advanced gastric, gastro-oesophageal junction, and oesophageal adenocarcinoma (CheckMate 649): a randomised, open-label, phase 3 trial. Lancet. 2021;398:27-40.
3.Sun J-M, Shen L, Shah MA, et al; KEYNOTE-590 Investigators. Pembrolizumab plus chemotherapy versus chemotherapy alone for first-line treatment of advanced oesophageal cancer (KEYNOTE-590): a randomised, placebo-controlled, phase 3 study. Lancet. 2021;398:759-771.
4.Shitara K, Janjigian Y, Moehler M, et al. Nivolumab (NIVO) plus chemotherapy (chemo) versus chemo as first-line (1L) treatment of advanced gastric cancer/gastroesophageal junction cancer/esophageal adenocarcinoma (GC/GEJC/EAC): expanded efficacy, safety, and subgroup analyses from CheckMate 649. J Clin Oncol. 2022;40:4s (suppl; abstr 240).
5.Zhao JJ, Yap DWT, Chan YH, et al. Low programmed death-ligand 1–expressing subgroup outcomes of first-line immune checkpoint inhibitors in gastric or esophageal adenocarcinoma. J Clin Oncol. 2022;40:392-402.
6.Zhou KI, Peterson B, Serritella A, et al. Spatial and temporal heterogeneity of PD-L1 expression and tumor mutational burden in gastroesophageal adenocarcinoma at baseline diagnosis and after chemotherapy. Clin Cancer Res. 2020;26:6453-6463.
7.Kang YK, Chen LT, Ryu MH, et al. Nivolumab plus chemotherapy versus placebo plus chemotherapy in patients with HER2-negative, untreated, unresectable advanced or recurrent gastric or gastro-oesophageal junction cancer (ATTRACTION-4): a randomised, multicentre, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2022;23(2):234-247.
8.Shitara K, Van Cutsem E, Bang Y-J, et al. Efficacy and Safety of Pembrolizumab or Pembrolizumab Plus Chemotherapy vs Chemotherapy Alone for Patients With First-line, Advanced Gastric Cancer: The KEYNOTE-062 Phase 3 Randomized Clinical Trial. JAMA Oncol. 2020;6(10):1571-80.
9.Janjigian YY, Kawazoe A, Ya?ez P, et al. The KEYNOTE-811 trial of dual PD-1 and HER2 blockade in HER2-positive gastric cancer. Nature. 2021;600:727-730.
10.Marabelle A, Fakih M, Lopez J, et al. Association of tumour mutational burden with outcomes in patients with advanced solid tumours treated with pembrolizumab: prospective biomarker analysis of the multicohort, open-label, phase 2 KEYNOTE-158 study. Lancet Oncol. 2020;21:1353-1365.
11.Hsiehchen D, Hsieh A, Samstein RM, et al. DNA repair gene mutations as predictors of immune checkpoint inhibitor response beyond tumor mutation burden. Cell Rep Med. 2020;1(3):100034.
12.Saeed A, Park R, Al-Rajabi R, et al. CA209-8YD: a phase I/II trial of rucaparib in combination with ramucirumab with or without nivolumab in previously treated advanced gastroesophageal adenocarcinoma (GEA) (RiME). J Clin Oncol. 2022;40:4s (suppl; abstr TPS377).
13.Kim ST, Cristescu R, Bass AJ, et al. Comprehensive molecular characterization of clinical responses to PD-1 inhibition in metastatic gastric cancer. Nat Med. 2018;24(9):1449-58.
14.Muro K, Chung HC, Shankaran V, et al. Pembrolizumab for patients with PD-L1-positive advanced gastric cancer (KEYNOTE-012): a multicentre, open-label, phase 1b trial. Lancet Oncol. 2016;17(6):717-26.
15.Fuchs CS, Doi T, Jang RW, et al. Safety and Efficacy of Pembrolizumab Monotherapy in Patients With Previously Treated Advanced Gastric and Gastroesophageal Junction Cancer: Phase 2 Clinical KEYNOTE-059 Trial. JAMA Oncol. 2018;4(5):e180013.
16.Lu Z, Chen H, Jiao X, et al. Prediction of immune checkpoint inhibition with immune oncology-related gene expression in gastrointestinal cancer using a machine learning classifier. J Immunother Cancer. 2020;8:e000631.
17.Kelly RJ, Lee J, Bang Y-J, et al. Safety and efficacy of durvalumab and tremelimumab alone or in combination in patients with advanced gastric and gastroesophageal junction adenocarcinoma. Clin Cancer Res. 2020;26:846-854.
18.Saeed A, Park R, Dai J, et al. 345 Phase I/II trial of cabozantinib plus durvalumab in advanced gastroesophageal cancer and other gastrointestinal malignancies (CAMILLA): phase Ib safety and efficacy results. J Immunother Cancer. 2021;9(suppl 2):A372.