
结核病 (TB) 是全球至人死亡的主要原因之一,每年有约1000万新发病例和120万TB死亡病例。TB的诊断挑战重重,特别是对于儿科、HIV共感染和肺外结核病例,因难以获得可用痰液样本,被广泛应用的痰液微生物学诊断方法性能极差。亟需快速、灵敏特异和能评估治疗效果的非痰液TB诊断方法。
灵敏检测循环系统中的病原体游离DNA (cfDNA) 可诊断疾病并评估治疗。但受检测灵敏度限制,基于qPCR检测结核分枝杆菌cfDNA ( Mtb -cfDNA) 诊断TB的灵敏度却极差且高度变异。基于CRISPR/Cas12a的反式切割活性构建信号放大系统,可显著提升核酸检测的灵敏度,已被用于检测痰液样本中的高丰度 Mtb -DNA,但仍需进一步提升核酸检测灵敏度以追踪血液样本中痕量的 Mtb -cfDNA。
近日,由美国杜兰医学院的胡晔教授领导的跨国研究团队开发了一种超灵敏的CRISPR/Cas12a荧光检测系统 (CRISPR-TB) ,通过检测血液样本中的 Mtb -cfDNA灵敏诊断TB。通过分析来自非HIV感染的儿童和成人血液样品 (Eswatini队列) ,及处于严重免疫抑制状态状态下的HIV共感染儿童纵向样本 (PUSH队列) ,表明CRISPR-TB介导的超灵敏血液 Mtb -cfDNA检测有望提高儿童TB和HIV相关TB的诊断率,并具有早期诊断TB、评估TB进展和快速监测TB治疗的潜力。相关成果以 CRISPR detection of circulating cell-free M. tuberculosis DNA in adults and children, including children with HIV: a molecular diagnostics study 为题发表在 The Lancet Microbe 期刊上。

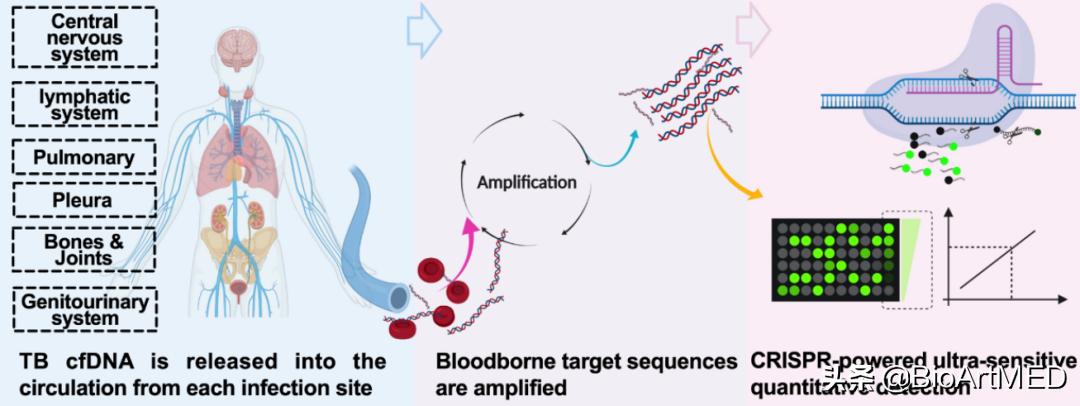
图1. CRISPR-TB通过分析血液 Mtb -cfDNA诊断结核病
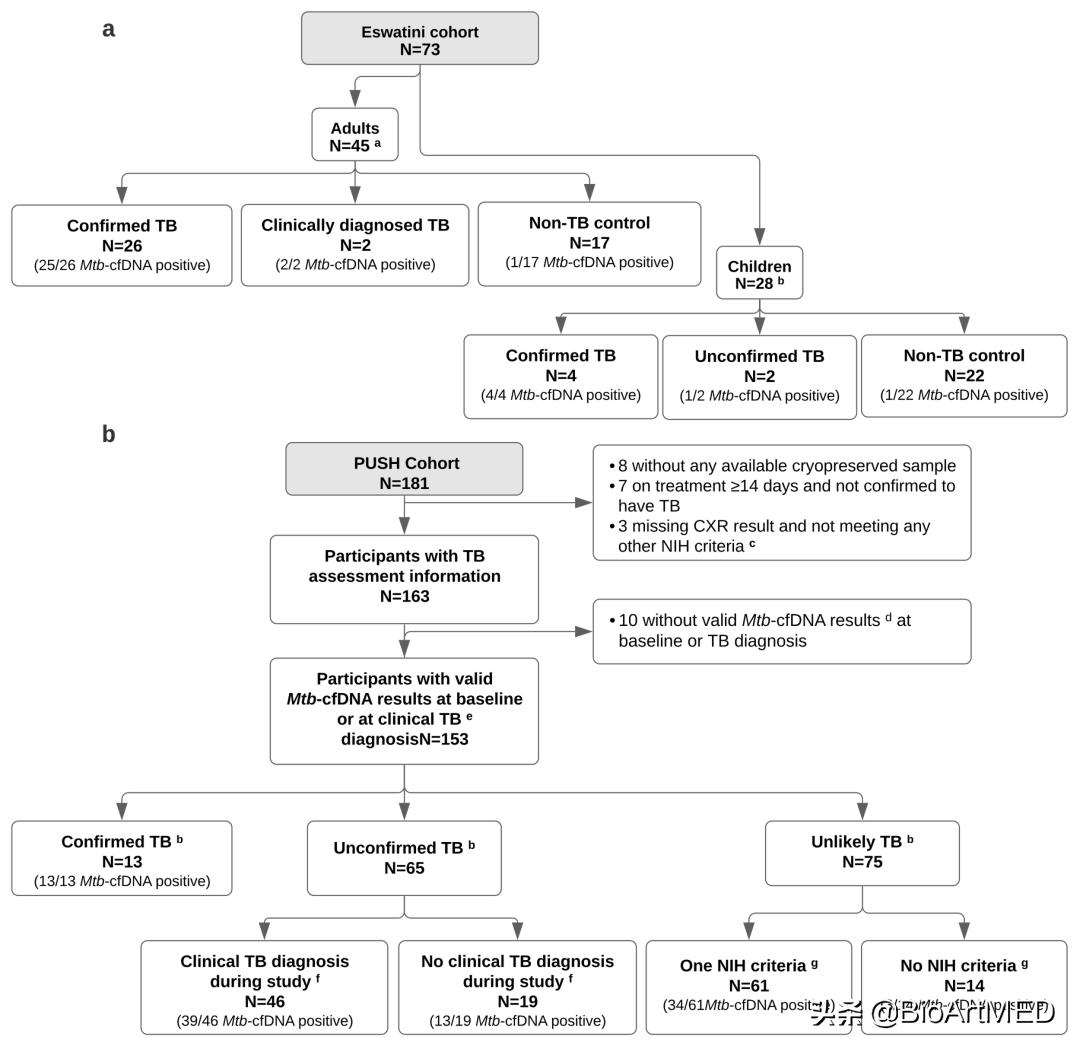
图2. 本研究涉及病例(图片来源Lancet Microbe)
定量CRISPR-TB灵敏特异诊断成人和儿童TB病例
通过系统优化cfDNA提取、cfDNA扩增和CRISPR放大等步骤,CRISPR-TB可准确识别 Mtb 和非结核分枝杆菌,灵敏检测血液样本中低至0.06 copy/μL的 Mtb -IS6110基因 (定量范围:0.125-250 copy/μL) ,为灵敏诊断TB和准确评估TB负担提供了技术基础。
首先在有症状的成人和儿童疑似病例 (Eswatini队列) 中验证该方法。CRISPR-TB对成人和儿童的诊断灵敏度分别为96.4% (27/28;95% CI:79.7%-99.9%) 和83.3% (5/6;95% CI:35.9%-99.6%) ,特异性分别为94.1% (16/17;95% CI:71.3%-99.9%) 和95.5% (21/22;95% CI:77.2%-99.9%) 。值得注意的是,CRISPR-TB确定了该队列中的全部6例肺外TB (淋巴结、骨骼、关节和胸膜结核) 。
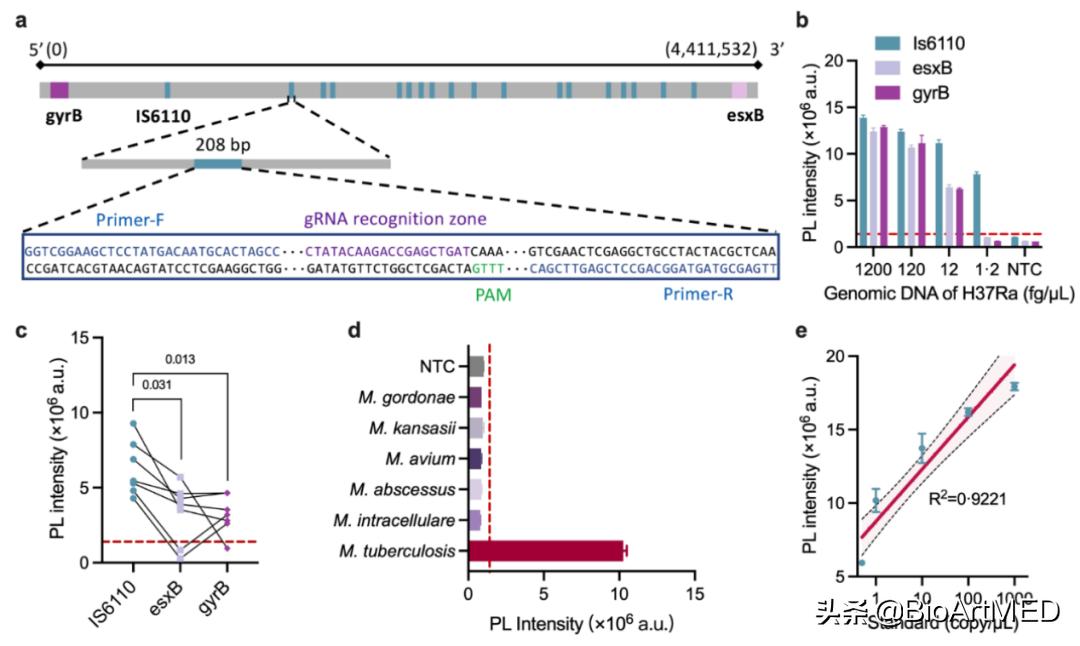
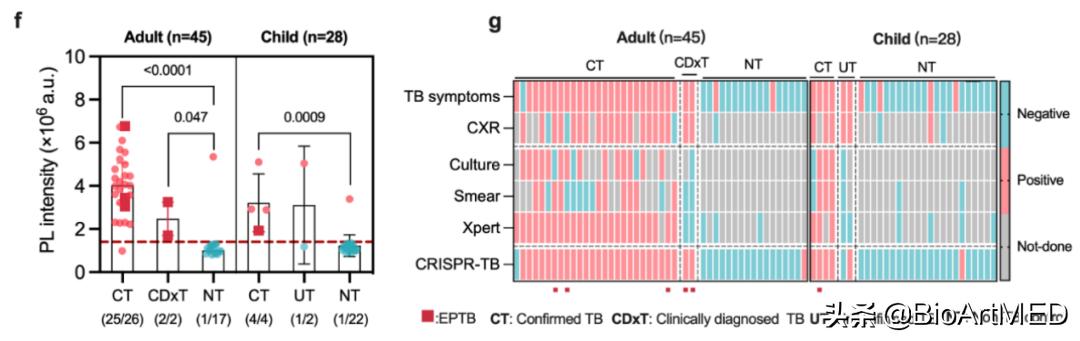
图3. 超灵敏特异CRISPR-TB(图片来源Lancet Microbe)
CRISPR-TB灵敏诊断严重免疫抑制HIV感染儿童
随后,通过对153名具有高结核病风险的住院HIV共感染儿童患者 (PUSH队列) 进行分析,评估了CIRPSR-TB对极具临床诊断挑战性人群的诊断能力。受试儿童的中位年龄为2.0岁 (IQR:0.8-5.1) ,女性占47.7%,大多数儿童处于严重的免疫抑制状态 (68.4%) 并出现至少一种提示结核病的症状 (90.2%) 。依据其临床表征和NIH分类标准,这些儿童被分类为确诊病例 (Confirmed TB) ,未确诊病例 (Unconfirmed TB) 和不太可能病例 (Unlikely TB) 。
CRISPR-TB检测到所有的Confirmed TB (13/13;95% CI:75.3%-100%) 和大多数Unconfirmed TB (52/65;80%) ,包括80% (4/5) 的肺外结核。针对不具有和具有至少1种NIH标准症状的Unlikely TB病例,CRISPR-TB的阴性率差异巨大 (78.6% Vs 44.3%) ,表明后者可能含有新发病例。基于不具有任何NIH标准症状的儿童,评估CRISPR-TB的特异性为78.6% (95% CI:49.2%-95.3%) ,明显低于Eswatini队列特异性估计值。
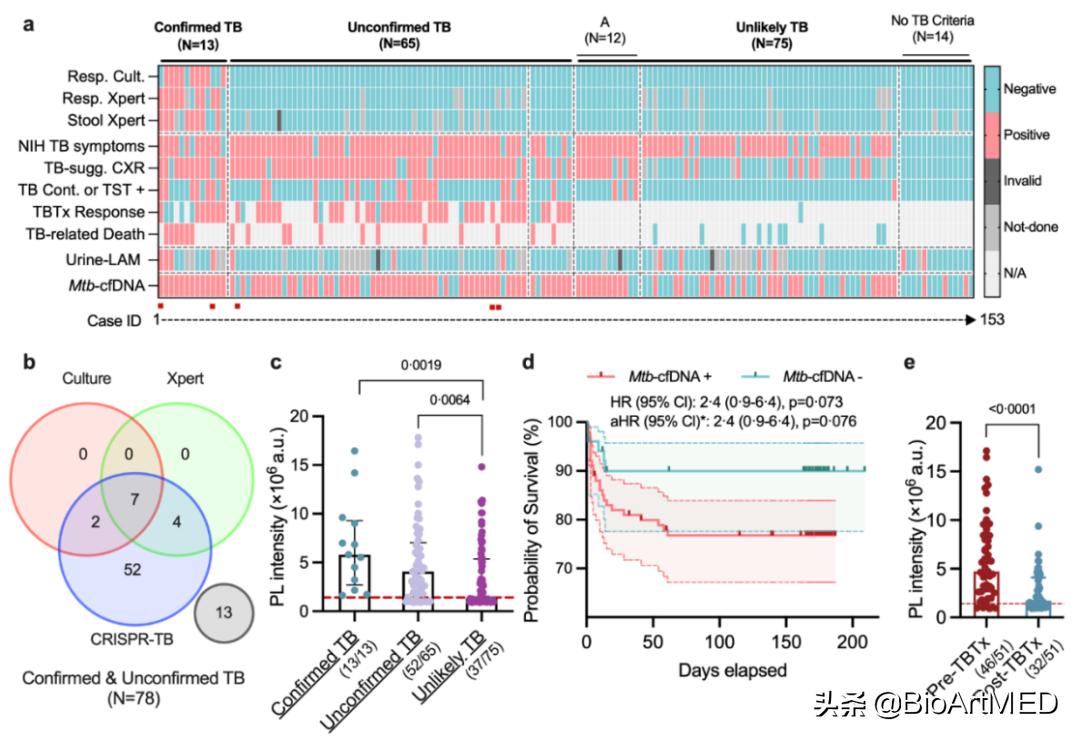
图4. CRISPR-TB评估HIV感染儿童病例(图片来源Lancet Microbe)
CRISPR-TB具有TB早期诊断的潜力
基于临床随访证据,12例PUSH病例被临床诊断为新发TB,其中的10位儿童在基线即显示了 Mtb -cfDNA阳性结果,较临床诊断时间提前43.5 (IQR:24.5-83) 天,表明CRISPR-TB的早期潜力诊断。
CRISPR-TB可能预测严重免疫抑制HIV感染儿童死亡
在为期6个月的随访研究中,28位儿童不幸死亡,他们的基线 Mtb -cfDNA水平高于存活的儿童 (p=0.08) 。Kaplan-Meier生存分析显示,基线 Mtb -cfDNA阳性儿童的死亡风险是阴性儿童的2.4倍 (95% CI:0.9-6.4;p=0.073) ,即使在调整了年龄和基线CD4+%后依然如此 (p=0.076) 。对于未接受TB治疗的95名儿童,基线 Mtb -cfDNA阳性儿童的死亡风险更高 (HR:3.9,95% CI:1.3-11.7;p=0.015) ;但对接受结核病治疗的58名儿童,基线 Mtb -cfDNA阳性与死亡率增加无关 (HR:0.9,95% CI:0.1-7.5];p=0.9) 。
CRISPR-TB可能监控严重免疫HIV感染儿童TB治疗
进一步利用CRISPR-TB追踪了51位接受TB治疗的儿童血液中 Mtb -cfDNA水平变化。结果表明,在经过5.6 (IQR:3.2-5.8) 个月治疗后, Mtb -cfDNA水平下降了73.7%,其中Confirmed TB,Unconfirmed TB和Unlikely TB病例的 Mtb -cfDNA水平分别降低71.4%,74.3%和70.6%。其中约89.4% (42/47) 接受治疗的基线 Mtb -cfDNA阳性儿童表现出症状改善或体重增加,其中83.3% (35/42) 的儿童 Mtb -cfDNA水平降低,33.3% (14/42) 的儿童 Mtb -cfDNA清除。
系统分析了27名具有≥4个随访样本儿童的 Mtb- cfDNA水平变化,约92.6% (25/27) 的儿童 Mtb -cfDNA水平随治疗介入直接降低 (n=11) 或升高后降低 (n=14) ,约51.9% (14/27) 的儿童在接受TB治疗后的一个月内 (中位15.5天,IQR:13-23) Mtb -cfDNA水平开始降低,约70.4% (19/27) 的儿童在研究结束时 (中位172天,IQR:167-175) Mtb -cfDNA清除或几乎清除。
结论
研究表明,灵敏检测疑似病例血液中的 Mtb -cfDNA可以诊断TB,包括HIV共感染儿童病例等微生物学方法无法诊断的少杆菌TB病例;在接受TB治疗后,血液中的 Mtb -cfDNA迅速下降,表明其具有监测TB治疗的潜力;基于 Mtb -cfDNA的测试还能预测TB的进展,诊断出通常被传统TB诊断所遗漏的具有高死亡风险的HIV感染儿童。此外, Mtb -cfDNA测试还具有早期诊断的潜力。总之,这些发现为血液 Mtb -cfDNA分析的实用性提供了强有力的初步证据,可用于非痰液的TB诊断和潜在的TB治疗监控应用。
原文链接:
https://doi.org/10.1016/S2666-5247(22)00087-8
制版人:十一
转载须知
【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经作者的允许禁止转载,作者拥有所有法定权利,违者必究。