710032西安空军军医大学西京医院甲乳外科李信,易军,贠军,徐昕,李一可,魏洪亮
乳腺癌是全世界癌症相关死亡的主要原因,也是女性最常见的癌症,占全球癌症死亡的23%。尽管在诊治方面取得了一些进展,但由于癌细胞的高增殖能力和对临床治疗的内在抵抗,干预效果往往不理想。近年来,长链非编码RNAs(lncRNAs)在各种生物过程中具有重要功能,尤其是癌症中。对癌基因和lncRNAs的研究有助于阐明乳腺癌的发病机制及开发新型分子靶向治疗。LncRNAs可作为多种肿瘤的竞争性内源性RNA来参与乳腺癌的发生发展。例如,Tang等发现lncCCAT1通过激活Wnt/β-catenin信号来促进乳腺癌干细胞功能。Qin等发现TSLNC8为竞争性内源性RNA吸收miR-214-3p来抑制乳腺癌细胞的增殖。Qiao等发现LINC00673可通过miR-515-5p来促进乳腺癌细胞的增殖。在众多lncRNAs中,LINC01296已经被报道在一些肿瘤中发挥肿瘤促进作用,其不仅是结直肠癌的潜在预后生物标记物,而且可作为膀胱癌的候选癌基因。然而,LINC01296在乳腺癌中的表达模式和功能尚不清楚。因此,本研究采用实时定量PCR(QPCR)检测乳腺癌组织的LINC01296表达并分析其与临床病理特征和预后的关系,现将结果报告如下。
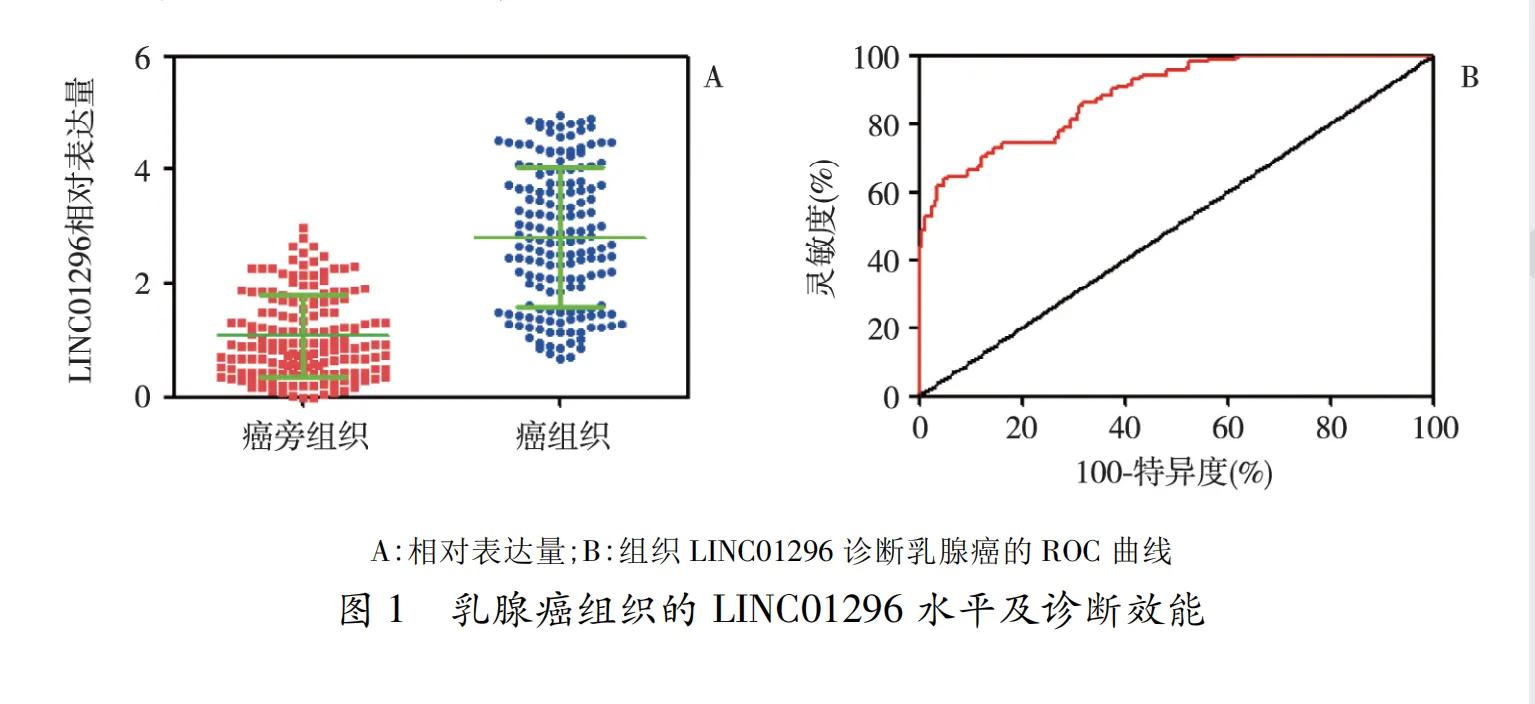
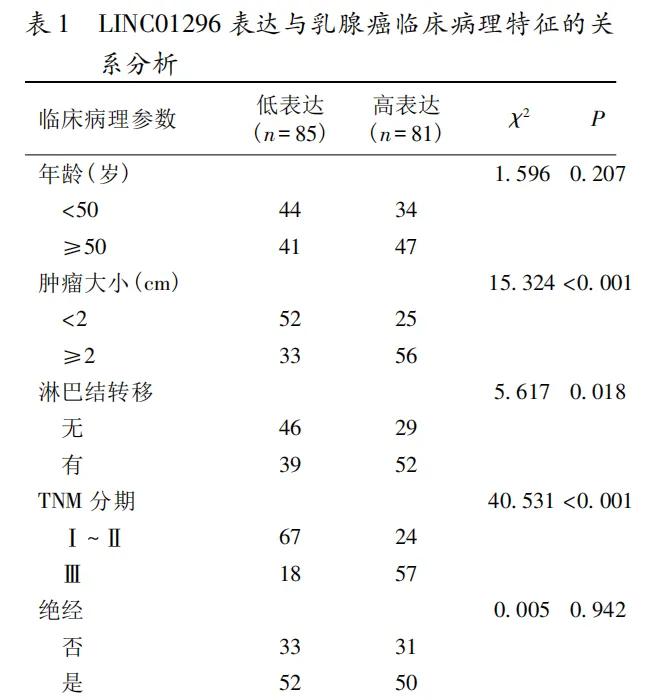
1资料与方法1.1一般资料收集本院2015年1月至2018年12月女性乳腺癌患者手术切除的166对癌组织和癌旁组织,均经病理组织学证实,年龄范围27~74岁,中位年龄54.0岁,<50岁78例,≥50岁88例;肿瘤大小<2cm77例,≥2cm89例;组织学分级:Ⅰ级44例,Ⅱ级47例,Ⅲ级75例;TNM分期:Ⅰ期38例,Ⅱ期53例,Ⅲ期75例;淋巴结转移阳性91例,阴性75例;雌激素受体(ER)阳性102例、孕激素受体(PR)阳性93例、HER-2阳性79例;Nottingham预后指数(NPI)<3.4者53例,3.4~5.4者62例,>5.4者51例。术前均未行抗肿瘤治疗,手术切除的组织立即冷冻于-80℃以用于提取RNA。1.2主要试剂RNeasyMiniKit、逆转录试剂盒QuantiTectReverseTranscriptionKit和QPCR试剂盒QuantiTectSYBRGreenPCRKit购自德国Qiagen公司,LINC01296和内参GAPDH引物由南京金斯瑞公司合成。1.3RNA提取和QPCR采用RNeasyMiniKit从组织中提取总RNA,根据试剂盒说明书采用QuantiTectReverseTranscriptionKit逆转录合成cDNA,随后于ABIPrism7500系统上使用Quanti-TectSYBRGreenPCRKit进行QPCR。以GAPDH为内参,采用2-ΔΔCt表示LINC01296的相对表达量。LINC01296上游引物:5’-TAAGGCT-GGAGCTGCTCAAC-3’;下游引物:5’-AGGATCT-GGGCTGCAGTCTA-3’;GAPDH上游引物:5’-GATTTGGTCGTATTGGGCGC-3’,下游引物:5’-GCCTTCTCCATGGTGGTGAA-3’。1.4Kaplan-Meierplotter在线分析采用Kaplan-Meierplotter在线数据库分析LINC01296表达与乳腺癌预后的关系,进入mRNAgenechip页面,选择breastcancer,预后指标纳入总生存期(OS)、无病生存期(RFS)、无远处转移生存期(DMFS)和进展后生存期(PPS),随访数据分别纳入患者626、1764、664和173例。1.5统计学分析采用SPSS23.0版统计软件进行数据分析。LINC01296水平以均数±标准差表示,组间比较采用t检验,LINC01296水平与临床病理特征的关系分析采用χ2检验,受试者工作特征(ROC)曲线评价组织LINC01296水平诊断乳腺癌的效能。以P<0.05为差异有统计学意义。2结果2.1乳腺癌组织的LINC01296表达166例乳腺癌组织中的LINC01296水平为2.810±1.219,高于对应癌旁组织的1.070±0.721(t=15.831,P<0.001);组织LINC01296诊断乳腺癌的曲线下面积为0.886(95%CI:0.853~0.919,P<0.001),最佳截断点为2.340时约登指数最大(0.5904),灵敏度和特异度分别为63.86%和95.18%。见图1。
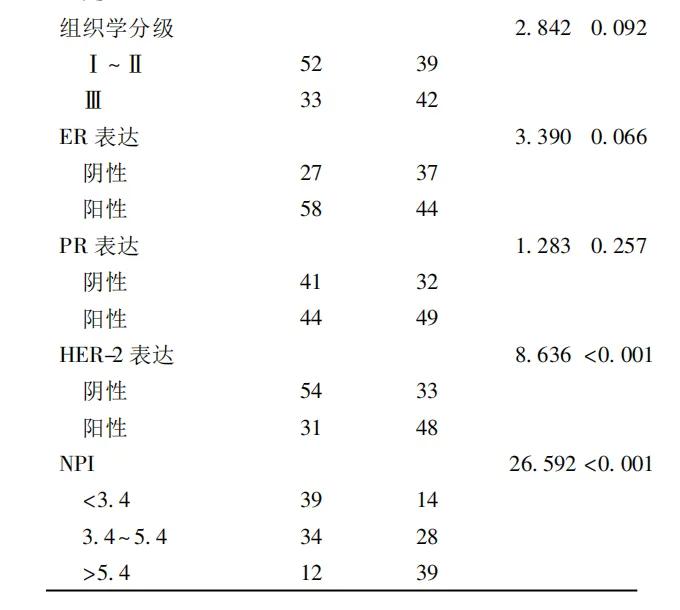
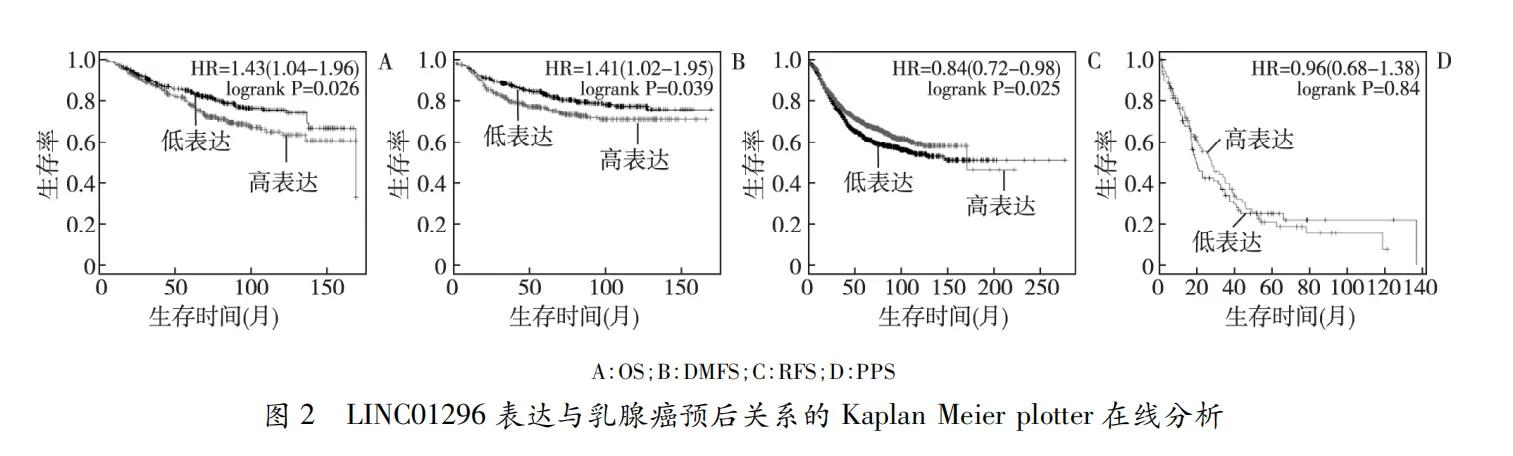
2.2LINC01296表达与乳腺癌临床病理特征的关系以乳腺癌组织的均数2.810将166例癌组织分为低表达组(≤2.810)85例和高表达组(>2.810)81例,进一步分析发现LINC01296表达与肿瘤大小、淋巴结转移、TNM分期、HER-2表达和NPI有关(P<0.05),而与年龄、绝经、组织学分级、ER和PR表达均无关(P>0.05)。2.3LINC01296表达与乳腺癌预后关系的在线分析Kaplan-Meierplotter在线分析显示乳腺癌组织LINC01296表达与OS、DMFS和RFS均有关,而与PPS无关,其中低表达的中位OS为123.6个月,高于高表达的66.72个月(HR=1.43,95%CI:1.04~1.96),但低表达的中位RFS为33.0个月,低于高表达的39.0个月(HR=0.84,95%CI:0.72~0.98),尽管不同表达的中位DMFS均未达,但低表达仍优于高表达(HR=1.41,95%CI:1.02~1.95)。见图2。
3讨论LncRNAs是一个大的非编码转录子群,已成为包括乳腺癌在内的重要调节因子和预后标志物。目前,lncRNAs被认为是癌症发展的关键因素,因为lncRNAs失调常导致肿瘤的发生和恶性进展,而靶向lncRNAs可更直接地诱导抗癌作用。LINC01296定位于染色体14q11.2,在不同肿瘤中的作用和分子机制已被广泛研究。如Liu等报道,LINC01296差异表达与结直肠癌细胞的恶性程度和不良临床预后密切相关,此外,功能和机制分析显示LINC01296在体外可影响结直肠癌细胞的增殖、转移和对5-氟尿嘧啶的耐药。Wang等发现LINC01296促进膀胱癌的进展并可作为膀胱癌的生物标志物和治疗靶点。Xu等指出LINC01296/miR-598/Twist1是促进非小细胞肺癌发生的正反馈环,为该恶性肿瘤的治疗提供了新思路和策略。Zhang等的研究表明LINC01296通过对人胆管癌miR-5095的应答来促进肿瘤生长和进展。上述结果提示LINC01296在肿瘤发展中是一个促进因子。然而,LINC01296在乳腺癌中的表达模式及与乳腺癌预后的关系鲜有报道。本研究检测了乳腺癌组织中LINC01296的表达水平,以进一步证实LINC01296在乳腺癌中的表达是否上调。与其他类型肿瘤中的报道一致,乳腺癌组织的LINC01296水平较正常组织升高。ROC曲线结果也证实该lncRNA在诊断乳腺癌上效能较好,该结果有力地提示了LINC01296作为检测乳腺癌潜在生物标记物的可能性。此外,LINC01296高表达赋予乳腺癌患者的恶性临床病理特征,包括肿瘤大小、淋巴结转移、TNM分期、HER-2表达和NPI。更重要的是,Kaplan-Meierplotter在线分析显示LINC01296的高表达水平与较短的OS和DMFS密切相关。以上结果支持LINC01296参与了乳腺癌的发生发展,可能是乳腺癌的潜在治疗靶点。LINC01296在多种肿瘤中的临床意义和生物学功能已有报道,但其在肿瘤中的调控机制尚不清楚。目前围绕LINC01296的作用机制可分为两种:(1)LINC01296作为竞争内源性RNA或天然miRNA海绵,如可为内源性“海绵”来吸附miR-26a、miR-598和miR-5095;(2)与参与表观遗传学的因子的相互作用,导致靶基因表观遗传沉默,如EZH2、KLF2等。LINC01296通过何种途径或信号通路来调控乳腺癌的发生发展目前尚不清楚,本研究推测上述或部分通路可能介导了LINC01296对乳腺癌的调控作用,这将为今后的工作重点,后续将借助体外细胞实验来验证。综上所述,LINC01296在乳腺癌中高表达且参与了该肿瘤发生发展,高水平LINC01296与不良预后关系密切,可作为乳腺癌预后预测和治疗的潜在靶点。本研究样本量较少且未完全评估该指标的不良预后风险,后续将扩大样本量进行完善。