诱导产生乙型肝炎病毒(HBV)特异性CD8+T细胞反应可能是实现慢性乙型肝炎(CHB)功能性治愈的必要机制。迄今为止,人类通过接种疫苗获得的最高数量CD8+T细胞应答是先使用复制能力不强的腺病毒载体、随后使用减毒痘痘病毒加强诱导的。
VTP-300 是 临床阶段生物制药公司 Vaccitech Ltd 开发用于慢性乙型肝炎治疗的一款治疗性乙肝疫苗,由黑猩猩腺病毒载体(ChAdOx1 HBV)和异源改良疫苗安卡拉加强(MVA-HBV),编码来自基因C乙肝型病毒序列的聚合酶、核心和S抗原。
目前正在延长服用抗病毒药物(HBV DNA 检测不到,HBsAg<4000 IU/ml)的慢乙肝患者群体中进行一项完整的Phase 1b/2a期试验(n=55)。
试验分四组:
第1组(n=10),Day 0: MVA-HBV 1 x 10^8 pfu IM(肌注) 注射、 Day 28: MVA-HBV 1 x 10^8 pfu IM 注射
第2组(n=18),Day 0: ChAdOx1-HBV 1 x 2.5 10^10 vp IM 注射、 Day 28: MVA-HBV 1 x 10^8 pfu IM 注射
第3组(n=18)ChAdOx1-HBV 1 x 2.5 10^10 vp IM 注射、Day 28: MVA-HBV 1 x 10^8 pfu IM 注射 + nivolumab 0.3 mg/kg IV 注射
第4组(n=9)Day 0: ChAdOx1-HBV 1 x 2.5 10^10 vp IM 注射 + nivolumab 0.3 mg/kg IV 注射、Day 28: MVA-HBV 1 x 10^8 pfu IM 注射 + nivolumab 0.3 mg/kg IV 注射
使用基因型C和D HBV肽在IFNg ELISpot试验中评估 HBV特异性T细胞应答。
研究结果,纳入了55例患者作为受试者,所有受试者均无安全信号或疫苗相关SAE报告。
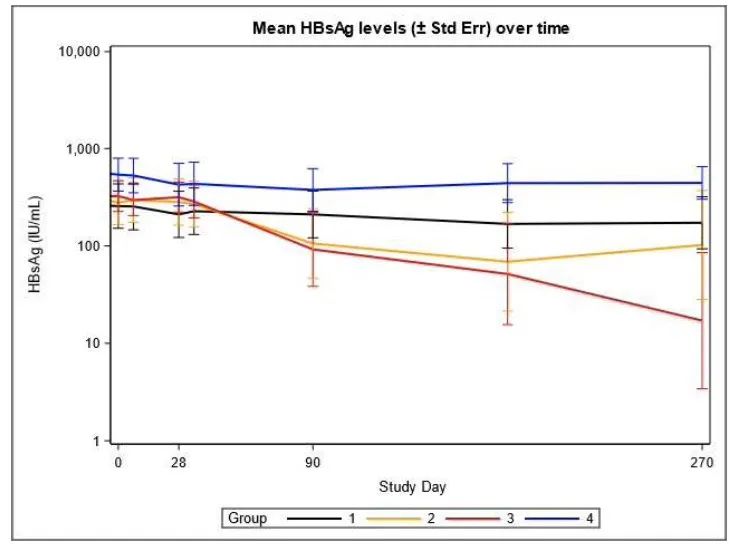
2名患者出现与HBsAg下降相关的轻度转氨酶骤发升高。第1组和第4组的HBsAg无明显变化。在第2组中,3名HBsAg起始值小于50 IU/ml的患者的log10下降幅度分别为-0.70、-0.73 和-1.39 log10。在第3组中,在3、6和9个月时,HBsAg log10 的平均下降幅度分别是-0.64(N=12)、-0.72(N=10)和-0.99(N=7)。所有出现大于 0.5 log10 降低的应答都持续8个月,直到研究结束。
对20例患者的HBV T细胞应答进行了HBV核心(8/20)、HBsAg(17/20)和聚合酶(8/20)评估。
在第1-4组中经过初免接种后,HBV特异性T细胞的总反应峰值平均值分别为437、244、688、332 SFU/106。加强接种高峰(第35天)后,第1-4组的总HBV特异性T细胞应答分别为 344、689、689 和277 SFU/106。
13名患者在初次接种后和16名患者在增强接种后的反应均较基线有所增强。大多数患者的反应持续3-6个月。HBV基因型间交叉反应性T细胞反应与基因型D肽高度交叉反应。
研究结论认,VTP-300 免疫疗法作为单一疗法和在加强时间点与低剂量 Nivolumab 联合使用,具有免疫原性,在控制良好的慢乙肝患者中HBsAg降低,同时表现出良好的安全性 。
来源:肝脏时间(HeparSpace)