昆虫肠道是食物消化和营养物质吸收的主要部位,其中产生的消化酶,主要负责营养物质的消化吸收,有些也参与对病原微生物的免疫反应。食物中的蛋白质,在昆虫体内必须首先在肠道中经蛋白酶水解为游离氨基酸,才能被昆虫吸收并用于其生长发育。
柞蚕作为我国有经济价值的可食性昆虫,其蛋白质和不饱和脂肪酸含量高,有报道称其粗蛋白含量与鸡蛋相当。柞蚕蛋白质应该来自柞树叶蛋白质的转化。
金属羧肽酶M14家族成员在很多昆虫中被证实参与外源蛋白向内源蛋白的转化,然而柞蚕金属羧肽酶M14基因家族成员,还没有任何报道。
前期研究,在柞蚕肠道转录组数据中发现1个高表达的金属羧肽酶基因,本研究首先想克隆该基因的全长ORF序列,明确该基因的序列特征,为后续基因家族成员的鉴定提供参考。

柞蚕解剖和肠道总RNA的提取
柞蚕的解剖:选取野外饲养的生长正常的5龄柞蚕幼虫,带回实验室准备解剖。提前将剪刀、镊子、0.9%的生理盐水、玻璃平皿和吸水纸,在121℃的高压灭菌锅内灭菌。
将灭菌后的0.9%的生理盐水倒在玻璃平皿内并置于冰上,将柞蚕固定于泡沫板上,解剖并收集肠道组织,去掉内容物,将组织移至冰浴的0.9%的生理盐水中清洗,确保肠道内容物清洗干净后,放在灭菌后的吸水纸中吸干多余水分,分别装入提前标注好组织名称和日期的1.5mL无RNA酶离心管上,迅速放入液氮中速冻,随后放入-80℃冰箱中备用。
肠道总RNA的提取:提前将研钵、研磨杵和药匙洗干净并晾干,用铝箔包好后,在210℃的干热灭菌箱中灭菌4~6h。灭菌结束后,关闭仪器,待温度降至室温,取出待用。
在研钵中反复加入适量液氮提前预冷,并取出-80℃超低温冰箱里的柞蚕肠道组织样品置于液氮中,研钵预冷好后立即将组织样品置于研钵内迅速研磨,研磨过程中,随时补充液氮以保证液氮不完全挥发,直至样品充分研磨成粉末。

RNA的提取按照TotalRNAKitⅡ试剂盒进行抽提。本实验方法中提到的β-巯基乙醇、氯仿、无水乙醇、DEPC水等需自行准备。
RNA提取的方法如下:(1)提前在每1mL的裂解缓冲液(RNASolv®Reagent)中加入20μL的β-巯基乙醇,β-巯基乙醇有毒性,注意在通风橱中进行。用DEPC水提前配制好70%的乙醇备用。同时启动离心机,将离心机温度提前预冷至4℃。
(2)取30~80mg研磨好的粉末于1.5mL的提前预冷好的无RNA酶的离心管中,并加入1mL裂解缓冲液,充分涡旋混匀后室温静置5min。
(3)加入100~200μL的氯仿(在通风橱中进行),在涡旋振荡仪上高速震荡20s后室温静置3~5min,放入离心机中4℃,12,000×g离心15min。
(4)离心结束后,将上清液转移至新的1.5mL的无RNA酶的离心管中,注意不要吸到沉淀。上清液中加入等体积的70%的乙醇,涡旋混匀。
(5)将RNA结合柱套入收集管中,并将上一步所得的混合液转移至结合柱中(结合柱最大容量为700μL),将其放入离心机,10,000×g,1min,弃废液,并将结合柱放回收集管中。重复此步骤直至所有混合液被转移完。
(6)结合柱中加入500μLRNAWashBufferⅠ,10,000×g,30~60s,弃废液,将结合柱放回收集管中。
(7)结合柱中加入500μLRNAWashBufferⅡ,10,000×g,30~60s,弃废液,将结合柱放回收集管中。
(8)重复上一步骤,在弃掉收集管中滤液并装回结合柱后,放入离心机中10,000×g离心2min,尽量去除吸附柱中残留的无水乙醇。
(9)将结合柱放入一个新的无RNA酶的离心管中,在结合柱中央滴加45~75μL的DEPCWater洗脱RNA,静置2min后,将其放入离心机10,000×g离心2min,洗脱RNA。若想得到浓度更高的RNA,可将离心管中的RNA重新加入结合柱中,再次离心。离心完成后在离心管上标注好RNA名称和日期,-80℃保存备用。
RNA浓度和纯度的测定
RNA抽提完成后,用超微量紫外分光光度计检测RNA样品的浓度和纯度。首先用超纯水清洗探头,然后用DEPC水调零,直至NucleicAcidConc显示为0.0±0.1ng/μL。
用无RNA酶的枪头吸取1μL的RNA用于浓度测定,其A260/A280≥2.00为佳,说明RNA纯度较高。
若A260/A280比值低于2.0,说明存在蛋白质或酚类物质的影响。
琼脂糖凝胶电泳

溴化乙锭(Ethidiumbromide,EB)溶液:在专门配制EB溶液的瓶中,加入0.5g的溴化乙锭固体粉末,随后加入50mL的蒸馏水稀释并充分混匀,常温避光保存以备用。由于溴化乙锭具有剧毒,在配制过程中,注意佩戴好口罩和手套,做好防护。
琼脂糖凝胶的制备
实验常用的琼脂糖凝胶浓度为1%,具体制备方法如下:用天平称取1g的琼脂糖(Agarose)粉末,加入实验室制备琼脂糖凝胶专用的瓶中,同时量取100mL的提前稀释好的1×TAE缓冲液加入瓶中,适当摇匀后,放入微波炉中加热直至琼脂糖粉末完全溶解(注意加热的瓶子的瓶盖不能盖紧),加热时间一般需要1~2min。
加热完成后,拿出瓶子查看琼脂糖粉末的溶解情况,若没有完全溶解,轻晃摇匀后将瓶子重新放入微波炉中加热30~60s,直至琼脂糖完全溶解,完全溶解的液体呈透明状且没有固体颗粒残留。
加热完成后,会产生大量气泡,需轻晃至无气泡产生,室温放置使溶液温度降至50~60℃后,在溶液中加入1~2μL的提前配制好的EB溶液,轻晃混匀。
在溶液降温的同时,提前准备好所需的梳子、制胶板和制胶槽,并将其表面残留的凝胶冲洗干净,将制胶板放入制胶槽内,同时将梳子插入到制胶槽的固定位置,随后将混匀并降温的凝胶溶液倒入放置好的制胶器内,将制胶器水平放置在凝胶制备区域的实验台上,静置30min左右使凝胶自然凝固。
凝胶凝固后,轻轻垂直向上拔出梳子,取出制胶板,轻轻放入电泳槽内,电泳槽提前倒入电泳液(1×TAE缓冲液)。
整个制胶过程需佩戴一次性PE手套,加热和混匀时还需佩戴隔热线手套,防止污染和烫伤。
准备好后开始点样,将电泳样品缓缓加入样孔中,过程中防止戳破凝胶。
样品全部加完后,开始电泳,选择合适的电压和电流,可以选择恒压电泳(常用电压为100~200V),也可以选择恒流电泳(常用电流为120~200mA)。
抗生素溶液的配制

氨苄青霉素(Amp+):称取5g的氨苄青霉素粉末于50mL的灭菌后的容量瓶中,缓慢加入ddH2O使粉末充分溶解,定容至50mL。
在超净台中,用孔径为0.22μm的滤器过滤除菌,将过滤后的氨苄青霉素溶液分装到经高压灭菌后的1.5mL的离心管中,管盖上标注好名称和日期,-20℃保存备用。
卡那霉素(Kan+):称取0.5g的粉末状的硫酸卡那霉素于50mL的灭菌后的容量瓶中,缓慢加入ddH2O使粉末充分溶解,定容至50mL。
在超净台中,用孔径为0.22μm的滤器过滤除菌,将过滤后的卡那霉素溶液分装到经高压灭菌后的1.5mL的离心管中,管盖上标注好名称和日期,-20℃保存备用。
细菌培养用LB培养基的配制方法
液体LB培养基:根据实验需要,可配制不同体积的LB培养基。

如需配制300mL的LB液体培养,则称取1.5g酵母提取物(Yeastextract),3g胰蛋白胨(Tryptone),3g氯化钠,倒入三角锥形瓶或蓝盖瓶中,加入300mL的蒸馏水后,用铝箔纸和牛皮纸封口(蓝盖瓶的旋盖需松开两圈),121℃高压蒸汽灭菌3h,灭菌结束后取出,蓝盖瓶旋盖及时旋紧,室温放置或4℃保存备用。
在液体培养基中加入实验所需的抗生素后,可制备对应抗性的液体培养基,同样4℃保存。
固体LB培养基:如需配制300mL的LB固体培养基,则称取1.5g酵母提取物(Yeastextract),3g胰蛋白胨(Tryptone),3g氯化钠,倒入三角锥形瓶中,加入300mL的蒸馏水后,用铝箔纸和牛皮纸封口,121℃高压蒸汽灭菌3h取出。
室温放置至50℃左右后,在提前经紫外照射的超净台中,将培养基倒入灭菌后的玻璃平皿中(注意倒入的培养基的厚度),待培养基凝固后,用封口膜封口,标注为无抗性的LB固体培养基,标注好日期后,4℃保存。
若是制备有抗性的固体LB平板培养基,则在培养基降温至50℃左右时,加入1:1000体积的相应抗生素,摇匀后迅速倒入玻璃平皿中,防止倒入的过程中培养基凝固。

细菌转化实验
(1)超净台提前经紫外线照射30min左右。从-80℃冰箱中取出感受态细胞(100μL)迅速置于冰上,在超净工作台中加入连接产物(5μL)后迅速置于冰上静置30min。
(2)在42℃水浴锅中热激60~90s,迅速置于冰上2min。
(3)加入500μL的无抗性的LB液体培养基,于37℃摇床220rpm震荡培养45~60min。
(4)3,000rpm离心5min,吸除250μL的上清液,用枪头吹打使沉淀与剩余上清液充分混匀,吸取80~100μL菌液涂布到含有氨苄青霉素(Amp+)的固体LB平板上,封口膜封口后,倒置于37℃培养箱培养12h(过夜培养)。
菌液的保存(保菌):提前将甘油和1.5mL的离心管放入高压蒸汽灭菌锅灭菌,在超净工作台中将600μL的过夜培养的菌液和300μL的甘油加入到离心管中,并涡旋混匀,标注好菌液名称和日期,置于-80℃冰箱中保存。
ApMCP1基因的克隆
首先扩增ApMCP1基因的中间片段。根据该基因现有的序列,使用PrimerPremier5软件设计引物(表2-1),并送生物公司合成。以稀释后的(一般稀释10倍)柞蚕肠道cDNA为模板,进行RT-PCR。
PCR的扩增体系为:酶2×EasyTaq®PCRSuperMix6μL,上游引物ApMCP1-F0.5μL,下游引物ApMCP1-R0.5μL,模板1μL,ddH2O4μL,反应体系的总体积为12μL。
其中,5′末端RACE反应步骤:(1)首先对提取的柞蚕肠道总RNA样品进行特殊处理。
(2)使用LigatedRNA和本小组设计的RACE克隆专用的特异引物Oligo(dT)60进行反转录反应,cDNA的合成方法根据2.1.3中的方法进行。
(3)5′末端RACE反应需进行两轮PCR,第一轮PCR以5′RACE第一链cDNA为模板,扩增体系为:2×TaqPlusMasterMixII6μL,5′RACEOuterPrimer0.5μL,5raceApMCP1-R10.5μL,模板2μL,ddH2O3μL,反应体系的总体积为12μL。
PCR反应程序为:预变性:95℃5min变性:95℃30s退火:50℃40s30个循环延伸:72℃90s终延伸:72℃5min
第一轮PCR反应程序结束后,将PCR产物稀释100倍后,作为模板进行第二轮PCR反应,反应体系的扩增体系为2×TaqPlusMasterMixII12.5μL,5′race-25nest0.5μL,5raceApMCP1-R20.5μL,模板2μL,ddH2O9.5μL,反应体系的总体积为25μL,PCR反应程序同第一轮PCR反应一样(退火温度改为57℃)。
反应程序结束后,取5μL点样,琼脂糖凝胶电泳后使用凝胶成像系统进行拍照检测,若有条带且正确,则将对应的剩余PCR产物纯化回收,连接到pEASY®-T1Simple克隆载体上(反应体系和反应条件同上)。
将连接产物转化到配制好的感受态细胞中,涂布到有氨苄青霉素(Amp+)抗性的固体LB平板上,倒置于37℃培养箱中培养12h(过夜培养)。

第二天挑菌后,吸取2μL菌液作为模板于PCR反应体系中,进行PCR筛选验证,PCR验证为阳性的菌液,吸取5μL于5mL的LB(Amp+抗性)液体培养基中扩大培养(过夜摇菌),第二天吸取1mL菌液寄送生物公司测序,剩余菌液置于4℃保存。
测序结果即为该基因克隆的5′末端片段序列。
ApMCP1基因的序列分析
通过BLASTN2.11.0+[68]将ApMCP1基因的核苷酸序列与柞蚕基因组[69]进行本地比对,分析该基因的基因结构。

结果与分析
羧肽酶中研究较多的就是金属羧肽酶,且家族种类多。金属羧肽酶M14基因家族成员在柞蚕中还未被鉴定,因此将该基因命名为ApMCP1,方便进一步研究。消化酶相关基因。
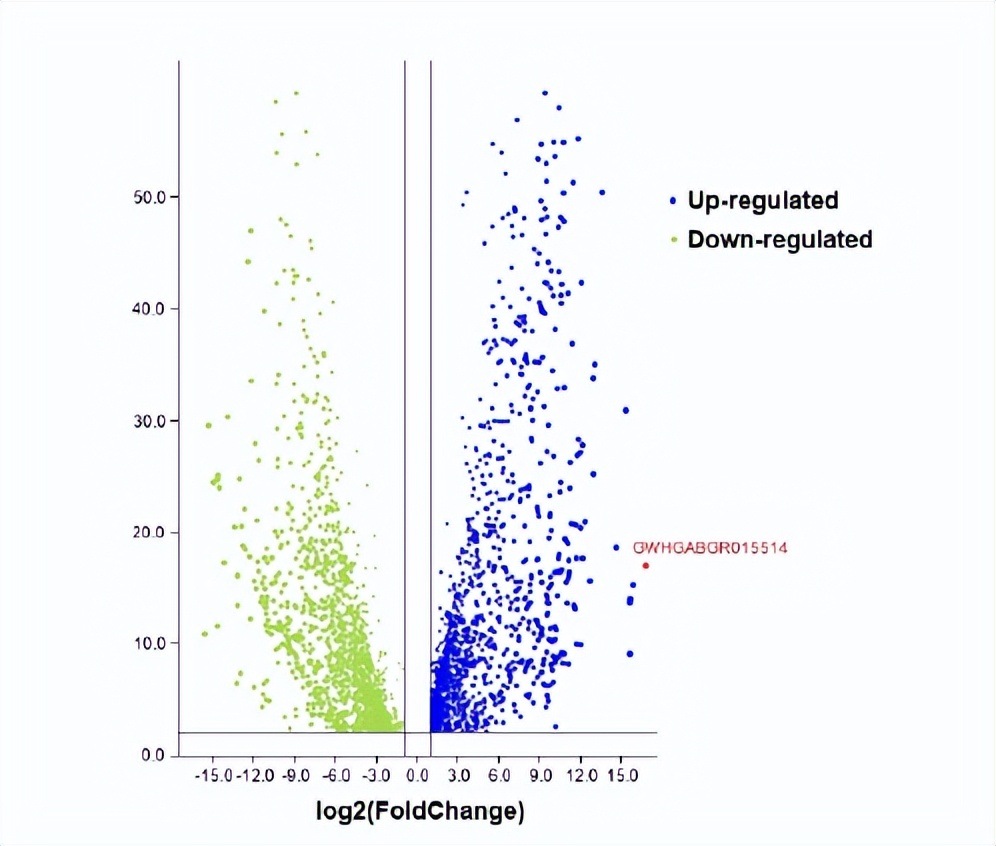
在蓝色圆点所示的肠道高表达基因中,其中一个基因(红色圆点)在柞蚕基因组中被注释为金属羧肽酶M14基因,对应在柞蚕基因组中的登录号为GWHGABGR015514。
羧肽酶中研究较多的就是金属羧肽酶,且家族种类多。金属羧肽酶M14基因家族成员在柞蚕中还未被鉴定,因此将该基因命名为ApMCP1,方便进一步研究。
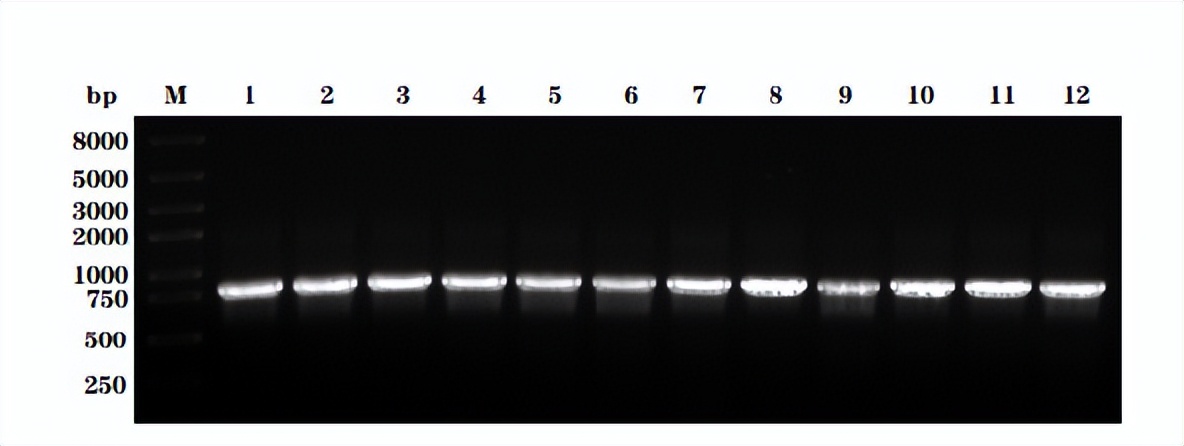
因的中间片段,大约850bp左右,同时可以确定ApMCP1确实在肠道中表达。将纯化后的产物与T载连接转化后,通过菌落PCR筛选阳性克隆,测序后得到833bp的中间片段。
将测序得到的中间片段、5′末端序列及转录组组装转录本进行比对拼接,发现测序的序列和转录组组装序列完全吻合。

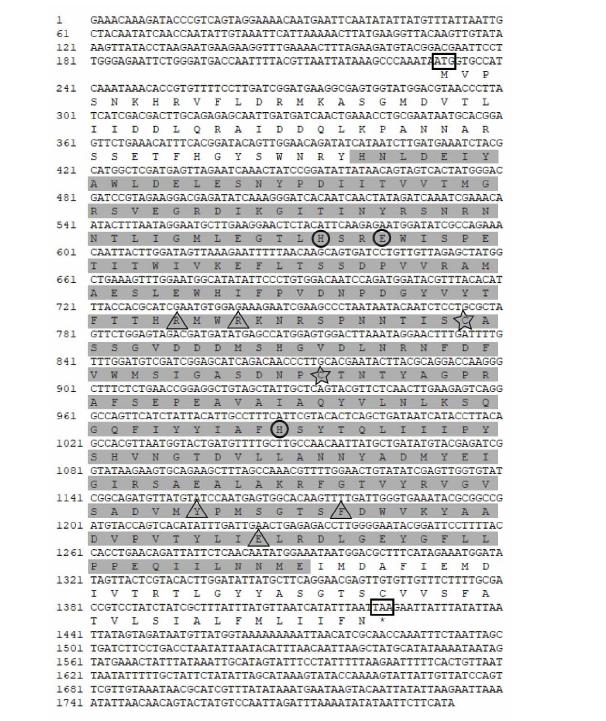
因此将扩增的中间片段序列、克隆得到的5′末端序列整理拼接到组装好的ApMCP1转录本序列中,得到ApMCP1的全长ORF序列。转录组组装序列和RT-PCR、5′RACE的测序序列的比较。
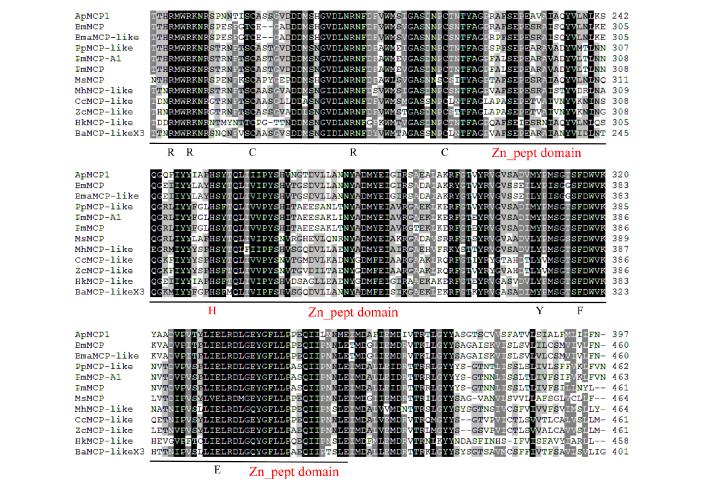
根据ApMCP1的锌结合位点(H69SRE72…H196),可以得知ApMCP1基因属于M14A亚家族成员。
