最近这段时间,北京是真的结结实实地降温了,早上出门,小风一吹,感觉自己头皮发凉,不禁心生疑惑,我头发呢?我头发怎么都没了?
还不是因为压(bu)力(shui)大(jiao)!
是了,当代年轻人,谁没点压力呢,压力之下,我们都难免会出现一些焦虑情绪。虽然说这是正常的情绪反应,但是与长期的慢性压力有关的,频繁的急性情绪反应其实并不利于我们的健康,会增加抑郁症和焦虑症的风险。
而就在今天,《细胞》杂志上的一项研究[1]告诉我们,压力竟然可以通过免疫系统来导致焦虑的产生!
这项研究是由浙江大学靳津教授和东南大学柴人杰教授的团队联合完成的,他们在小鼠中发现,压力可以诱导CD4+ T细胞的线粒体裂解,合成了过多的黄嘌呤,通过血液循环进入大脑,直接刺激了大脑杏仁核,从而导致了小鼠的焦虑行为。
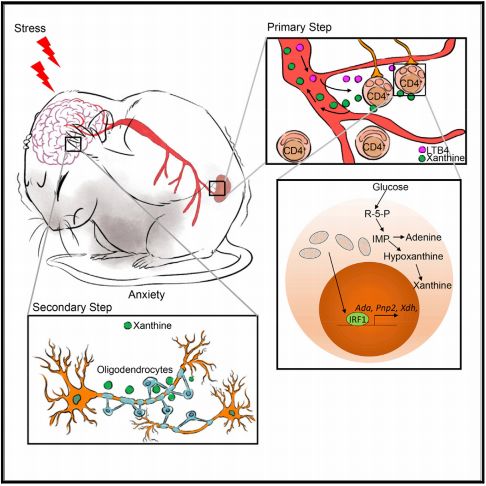
这个小鼠,它看起来就很焦虑[1]
目前,针对焦虑症和抑郁症的药物多是直接靶向中枢神经系统,在治疗的同时也有很多副作用,包括性功能障碍、代谢紊乱和高血压。
所以,只有更全面地了解它们产生的机制,才可能诞生新的靶点和药物。
其实,这也不是科学家们第一次发现慢性压力与免疫系统存在相互作用了,之前的研究就显示,慢性压力会减弱免疫反应,减少白细胞和外周淋巴细胞,损伤中性粒细胞的吞噬功能[2,3]。一些由免疫细胞产生的细胞因子,比如说白介素-6和白介素-1b,还会影响中枢神经系统的很多功能[4,5]。
在这次的实验中,研究人员首先对小鼠进行了基因编辑,让它们成为了适应性免疫有缺陷的小鼠,然后对它们和普通小鼠一起进行连续8天的足部电击,这是在很多研究中验证过的“压力引发焦虑”的小鼠模型。
他们发现,普通小鼠受到电击的影响,出现了一些焦虑行为,就算是开阔的场地,它们也不再有兴趣对中心地带进行探索,而是只在场地周围打转,但免疫缺陷小鼠却“毫无自觉”,它们依然跟没接受过电击似的满场跑。
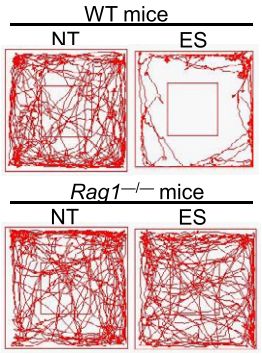
普通小鼠(上)和基因敲除小鼠(下)在正常情况(NT)和电击后(ES)的行动轨迹
看来,适应性免疫果然在压力引发焦虑中发挥着重要作用。
那到底是哪种免疫细胞呢?
研究人员分别对CD4+ T细胞和CD8+ T细胞进行了抑制,发现,缺少CD4+ T细胞时,小鼠再次丧失了焦虑感。
同时,他们发现,在压力的压迫下,包括幼稚T细胞和效应CD4+ T细胞在内的非炎性CD4+T细胞的线粒体发生了裂解!
之前就有研究指出,线粒体的形态对一些细胞和组织的代谢调节有密切的关联[6,7]。研究人员这次也确认了,敲除了与线粒体融合有关的基因的小鼠,和与它一起出生的普通小鼠相比,代谢产物的组成有不小的差别,比如说氨基酸里与神经兴奋和神经抑制传递有关的色氨酸和谷氨酸。

线粒体(图片来源:pixabay.com)
另外,大多数嘌呤和它们的衍生物都有了10-100倍的增加。有意思的是,其中黄嘌呤是只在大脑中疯狂增加,但在外周免疫器官里明显减少了,而一旦缺少了CD4+ T细胞之后,血液中的黄嘌呤就会明显下降。
鉴于已经在一些抑郁症患者和焦虑症患者血液中发现了水平明显高于常人的黄嘌呤,所以研究人员怀疑,CD4+ T细胞的线粒体裂解说不定就是通过黄嘌呤来诱导焦虑的产生的。
实验证明,他们的猜想是正确的。代谢组和转录组分析表明,C D4+ T细胞的线粒体裂解会导致转录因子IRF-1(干扰素调节因子1)的积累,主要是在Ada、Xdh和Pnp2三个基因的启动子区域。
IRF-1和它们的启动子区结合后,改变了细胞的代谢,促使葡萄糖不去选择正常的糖酵解途径,产生*酮丙**酸,而是选择了戊糖五磷酸途径,合成了高于正常水平的黄嘌呤。
作为一种代谢产物,它能够随血液循环,轻松地穿过血脑屏障,进入大脑。通过追踪,研究人员观察到,黄嘌呤会和大脑左侧杏仁核的少突胶质细胞上的腺苷受体A1结合 。杏仁核是大脑中调控恐惧和焦虑的关键区域,左侧杏仁核更是和普通的焦虑、社交焦虑、强迫症还有创伤应激有关。

(图片来源:pixabay.com)
在实验中,黄嘌呤和腺苷受体A1结合促进了少突胶质细胞的增殖和异常活化,导致与焦虑有关的神经元过度活跃。 直接用黄嘌呤处理的小鼠出现了和电击小鼠同样的焦虑行为。
至此,这个研究算是彻底阐明了压力是如何导致焦虑的,它会让CD4+ T细胞的线粒体发生裂解,通过转录因子IRF-1的增加,让细胞中的葡萄糖选择了“错误的”代谢途径,产生了过多的黄嘌呤,随血液循环进入大脑,与左侧杏仁核中的少突胶质细胞结合,过度激活焦虑相关神经元,从而导致了一系列焦虑行为。
看来,我们在各种压力下出现的焦虑说不定都是CD4+ T细胞捣的鬼?
不过CD4+ T细胞毕竟是很重要的免疫细胞,不能为了不焦虑,说干掉它们就干掉它们,所以研究人也指出,如果之后的研究能够在CD4+ T细胞群中进一步找到更加特异性的T细胞,通过药物对特异性靶点进行抑制,或许就能够为抑郁症和焦虑症患者们带来新的药物[8]。
编辑神叨叨
全体奇点糕呕心沥血呕心沥血呕心沥血打造的重磅音频课程《医学趋势50讲》终于上线了。 我们一口气帮你同步了全球医学前沿领域最重磅的进展。 只需500分钟,让你彻底搞懂最重磅的医学前沿进展。
课程亮点如下:
1、全面: 一网打尽最重磅的医学前沿进展。
在这套《医学趋势50讲》中,我们囊括了免疫治疗、干细胞、微生物、人工智能、二代测序,抗癌新药研发等15个重要的前沿领域,帮你将全球最顶尖的科研成果一举收入囊中。
2、紧跟趋势: 帮你无缝同步全球认知。
奇点跨学科专业知识团队,依靠强大的自有数据库系统,每天跟踪全球3000多本医学与生命科学领域的重要期刊,实时把握医学前沿科技最强劲的脉搏。和全球认知同步,你不需要费心费力,我们把全球脉动送到你的耳边。
3、有趣易懂: 不用绞尽脑汁,就能理解全球医学顶尖难题。
医学和生命科学领域的论文往往晦涩难懂,再加上语言的隔阂,导致很多人对此望而却步。这一次,我们帮你把艰深晦涩的前沿学术调制成清新爽口的科学小品,让你在享受科学之美的同时,轻轻松松理解医学顶尖难题。和全球最聪明的大脑思考同样的问题,你也可以。
参考资料:
[1] https://www.cell.com/cell/fulltext/S0092-8674(19)31117-1
[2] Glaser, R., and Kiecolt-Glaser, J.K. (2005). Stress-induced immune dysfunction: implications for health. Nat. Rev. Immunol. 5, 243–251.
[3] Padgett, D.A., and Glaser, R. (2003). How stress influences the immune response. Trends Immunol. 24, 444–448.
[4] Chourbaji, S., Urani, A., Inta, I., Sanchis-Segura, C., Brandwein, C., Zink, M., Schwaninger, M., and Gass, P. (2006). IL-6 knockout mice exhibit resistance to stress-induced development of depression-like behaviors. Neurobiol. Dis. 23, 587–594.
[5] Engler, H., Brendt, P., Wischermann, J., Wegner, A., Ro¨ hling, R., Schoemberg, T., Meyer, U., Gold, R., Peters, J., Benson, S., and Schedlowski, M. (2017). Selective increase of cerebrospinal fluid IL-6 during experimental systemic inflammation in humans: association with depressive symptoms. Mol. Psychiatry 22, 1448–1454.
[6] Mishra, P., and Chan, D.C. (2016). Metabolic regulation of mitochondrial dynamics. J. Cell Biol. 212, 379–387.
[7] Wai, T., and Langer, T. (2016). Mitochondrial Dynamics and Metabolic Regulation. Trends Endocrinol. Metab. 27, 105–117.
[8] http://www.news.zju.edu.cn/2019/1101/c23245a1736210/page.htm

本文作者 | 应雨妍