
念珠菌是定植于人体口腔、胃肠道的共生菌,在某些情况下(营养变化、菌群失调、宿主机体免疫力降低)可变为致病菌,引发浅表感染甚至严重的全身系统性感染。虽然是机会性致病菌,念珠菌引起的真菌感染近年来急剧增加,尤其是免疫功能低下的患者[1-2]。因较高的致死率,侵袭性念珠菌感染已成为备受关注的公共卫生问题[3]。
治疗念珠菌感染的药物有限,且抗真菌药物日益加剧的耐药性和不可忽略的不良反应更是导致治疗失败的主要原因[3]。联合用药是一种实用有效的新药开发策略,提高药物疗效的同时可以潜在减少单一药物的使用剂量,降低药物不良反应[4]。越来越多的研究表明,从天然植物(尤其是药用植物)中提取的化合物及其衍生物联合传统的抗真菌剂对杀灭念珠菌具有显著的协同作用[5-7]。因此本文归纳了念珠菌对传统抗真菌药物的耐药情况,并总结了中药协同传统抗真菌药物的抑菌活性和抑菌机制,以期为抗念珠菌新型治疗策略的研究提供参考依据。
1 念珠菌对传统抗真菌药物耐药现状
目前临床使用的抗真菌剂主要有唑类、多烯类、烯丙胺类、棘白菌素类和核苷类。这些药物都聚焦于抑制细胞生长,主要作用靶点有所不同,如抑制麦角甾醇、DNA、葡聚糖、几丁质等的合成[8-16],具体的抗真菌机制和耐药机制见表1。
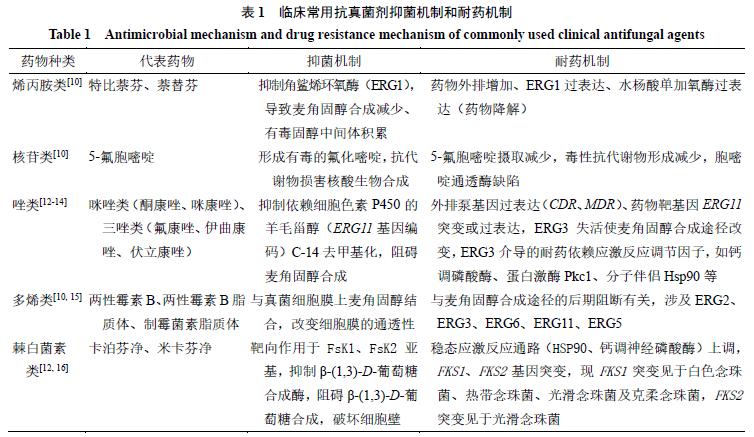
耐药性、宿主毒性是限制抗真菌药物使用的主要障碍。氟康唑是临床治疗全身或局部感染最常用的抗真菌药物,靶向作用于去甲基化酶Erg11,抑制细胞膜主要成分麦角固醇的合成以达到杀菌效果[4]。氟康唑的不良反应相对较小,但耐药或交叉耐药现象突出。Xiao等[11]历时3年从国内77家医院收集到念珠菌血症患者分离的4 010株念珠菌,分析其对临床常用抗真菌剂的耐药性,发现白色念珠菌、*平近**滑念珠菌对各种唑类药物相对敏感,耐药率小于5%;而热带念珠菌对氟康唑的耐药率为36.5%,伏立康唑的耐药率为50.8%,对两种药物的交叉耐药率也高达26.5%;光滑念珠菌对氟康唑的耐药率也达到了10.2%。
两性霉素B对真菌细胞的杀灭作用是由于其对真菌细胞膜上的麦角固醇具有较高的亲和性,使细胞膜上形成微孔,改变了细胞膜的通透性,导致胞内物质外泄。然而,两性霉素B对宿主细胞膜中的胆固醇也表现出较高的的亲和力,从而影响肾小管的通透性[10]。5-氟胞嘧啶可阻碍DNA的合成,可能对骨髓有一定的毒性。棘白菌素通过抑制葡聚糖的合成靶向作用于真菌细胞壁。因此类靶标不存在于哺乳动物细胞中,这些药物对宿主细胞的毒性较小[10]。近年来也出现了对两性霉素B、棘白菌素类药物卡泊芬净耐药的念珠菌[4, 10]。
2 中药协同传统抗真菌药物的抑菌活性
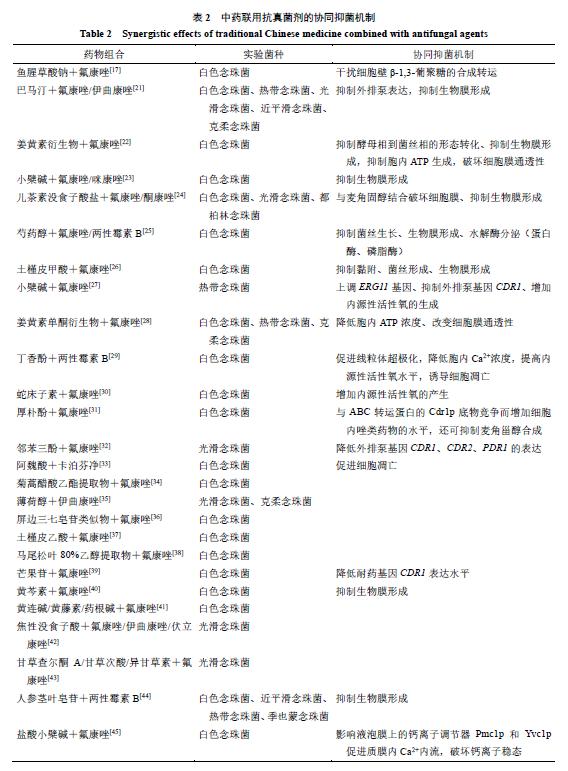
常规抗真菌剂耐药性的出现对临床治疗念珠菌感染带来了挑战,这一现状也使得联合用药策略受到更广泛的关注。越来越多的研究表明,传统抗真菌药物与中药联合使用可以协同抑制念珠菌(包括浮游细胞、生物膜),克服念珠菌耐药性或增强抗真菌剂的活性,以实现协同抑菌作用。
2.1 协同抑制浮游细胞
有研究表明联合用药对耐药念珠菌浮游细胞有良好的协同抑菌效果。Shao等[17]发现鱼腥草酸钠联合氟康唑对白色念珠菌表现出良好的协同抑菌效果,能明显降低药物的使用浓度。单独使用鱼腥草酸钠时,对白色念珠菌的最低抑菌浓度(MIC)范围为32~256 μg/mL,而与氟康唑联合使用时,鱼腥草酸钠的MIC范围下降至8~64 μg/mL;两药合用时氟康唑的MIC下降更显著,较单独使用降低了2~256倍。
同时应用部分抑菌浓度指数(FICI)评估两种药物的作用方式,发现与氟康唑敏感的菌株相比,鱼腥草酸钠联合氟康唑对耐氟康唑的白色念珠菌表现出更好的协同作用。Liu等[7]研究绞股蓝皂苷联用氟康唑对白色念珠菌的抑菌效果也有类似的现象,两种药物联合对耐氟康唑的白色念珠菌具有良好的协同抗菌活性(FICI 0.253 9~0.257 8),而两种药物对敏感的白色念珠菌表现为无关作用。出现这种现象的原因可能是敏感的菌株本身对氟康唑的MIC就相对较低,联合用药时MIC的下降幅度不如耐药菌株下降明显。
2.2 协同抑制生物膜
中药联用抗真菌剂对抗生物膜也有较好疗效。生物膜是不同于浮游细胞的另外一种生物存在形式,是由菌株自身产生的细胞外基质包裹菌细胞(酵母细胞、菌丝体和假菌丝)形成的微生物群落。念珠菌通过黏附可以在医疗器械(静脉留置导管、人工心脏瓣膜、置换关节等)、宿主组织中形成生物膜,其内的酵母细胞可播散至其他部位,引发局部或全身的感染[18]。在美国,每年使用静脉插管500多万个,其中50%以上的静脉插管会引发生物膜感染[8]。生物膜特有的致密三维网状结构不仅有助于病原体逃避宿主免疫攻击,还能抵御药物的抗菌作用[19]。念珠菌生物膜对抗真菌药物的耐药性是其浮游细胞的1 000倍[20]。生物膜形成是持续性念珠菌血症发展、治疗失败的主要因素。因此,研发能够对抗生物膜的有效药物和治疗策略有重要意义。
Wang等[21]研究表明,单独用药时,氟康唑、巴马汀对抗生物膜的生物被膜生长80%被抑制时的药物浓度(SMIC80)都大于1 024 μg/mL,而巴马亭联用氟康唑时,氟康唑的药物浓度下降了4~32倍,巴马汀下降了4~128倍。Dong等[22]发现32 μg/mL姜黄素衍生物联用4 μg/mL氟康唑对白色念珠菌生物膜的抑制率可达到90%,同时在激光共聚焦扫描显微镜下观察到,未经药物处理的生物膜可见丰富的菌丝,而联用组生物膜的结构被严重破坏,其内细胞以酵母相细胞为主,且细胞有凋亡的趋势。
此外,小檗碱+氟康唑/咪康唑、儿茶素没食子酸盐+氟康唑/酮康唑、芍药醇+氟康唑/两性霉素B、土槿皮甲酸+氟康唑也可抑制念珠菌生物膜的形成[23-26],见表2。由此可见,中药联合传统抗真菌药物对耐药念珠菌、生物膜都能发挥协同抑菌的活性,发挥药效的同时还能降低药物的使用浓度,表现出了新型治疗策略的潜在价值。只是目前的研究多集中在白色念珠菌,中药联合抗真菌剂杀灭非白念珠菌的研究相对较少。
3 中药协同传统抗真菌药物的抑菌机制
3.1 外排泵
外排泵基因过表达促进药物外排是念珠菌对唑类药物耐药的主要机制。而一些中药活性成分联合唑类药物恰恰可以降低外排泵基因( CDR 、 MDR )的表达,从而达到协同抑菌的效果。Shao等[27]研究表明,与未用药的对照组相比,小檗碱(2 μg/mL)联用氟康唑(8 μg/mL)下调 CDR1 基因3倍、下调 CDR2 基因10倍( P <0.05), MDR1 变化并不显著。巴马汀联用氟康唑作用于白色念珠菌也能显著降低外排泵相关基因 CDR1 、 CDR2 、 MDR1 、 FLU1 的表达。巴马汀联用氟康唑扩展到非白色念珠菌,也有抑制外排泵基因表达的作用,可显著下调*平近**滑念珠菌 CDR1 、 MDR1 基因表达,下调光滑念珠菌 CDR2 表达[21]。
3.2 毒力因子
念珠菌的毒力因子也是联合用药抑菌机制的一类靶点。毒力是指病原体致病能力的强弱,以及对各种不利环境的抵抗能力。毒力因子可以促进病原菌在宿主组织中黏附、浸润和扩散,也有助于病原体耐受宿主的适应性免疫[2]。念珠菌的毒力因子包括利于病原菌黏附宿主的黏附素、破坏宿主组织的水解酶(磷脂酶、脂肪酶、蛋白酶)和菌丝形成、生物膜形成等。与单药相比,芍药醇联用唑类药物氟康唑或两性霉素B对抑制念珠菌的毒力因子具有较强的协同作用,可抑制菌丝生长、生物膜形成(512 μg/mL芍药醇联合512 μg/mL氟康唑或4 μg/mL两性霉素B)和水解酶分泌(蛋白酶、磷脂酶)[25]。
绞股蓝皂苷联合氟康唑抗白色念珠菌不仅可以抑制毒力因子菌丝(32 μg/mL绞股蓝皂苷+8 μg/mL氟康唑)和早期生物膜的生长(32 μg/mL绞股蓝皂苷+0.5 μg/mL氟康唑),在32 μg/mL浓度下绞股蓝皂苷还可以抑制药物外排[7]。此外小檗碱、姜黄素衍生物、儿茶素没食子酸盐、巴马汀、土槿皮甲酸联用唑类药物也可抑制念珠菌毒力因子的产生,见表2。
3.3 其他
中药协同传统抗真菌剂抗念珠菌的机制还有以下几点:姜黄素衍生物联用氟康唑可协同抑制念珠菌胞内ATP生成,破坏细胞膜通透性[22, 28];丁香酚(100 μg/mL)联用两性霉素B(0.05 μg/mL)则可促进白色念珠菌线粒体超极化,降低胞内Ca2+浓度,提高内源性活性氧水平,诱导细胞凋亡[29];鱼腥草酸钠(16 μg/mL)联合氟康唑(8 μg/mL)发挥协同抑菌作用的机制与干扰细胞壁β-1,3-葡聚糖合成转运有关,二者联用可抑制相关基因 IFD6 、 PHR1 的表达,促进基因 ZAP1 、 ADH5 、 XOG 1和 FKS1 的表达[17]。
4 结语
一些中药成分不仅自身具有抗念珠菌活性,而且与抗真菌剂联合使用时也显示出良好的协同作用。这在一定程度上归因于中药与抗真菌剂有不同的药物靶点。二者联用时可同时靶向两个甚至多个药物靶点发挥更强的抑菌效果,这种特性是联合用药的优势之一,也是其发挥协同抑菌效果的关键所在。现有的联合用药研究为探索新型抗真菌治疗策略提供了重要参考途径,但仅体外研究不足以证明药物的安全性和有效性,因此今后还需要更多的体内实验进一步评估联合用药的不良反应和疗效。
利益冲突 所有作者均声明不存在利益冲突
参考文献(略)
来 源:李贞,陈伟琴,刘维薇.中药协同抗真菌药物抗念珠菌的研究进展 [J]. 现代药物与临床, 2022, 37(12): 2891-2896 .