肺癌的免疫治疗
在临床工作中,常常有肺癌患者及家属咨询免疫治疗的相关情况。今天就来讲讲肺癌目前免疫治疗的情况。
作为中国乃至全球第一大癌种,每年全球约有170万人死于肺癌,而在国内这一数字是62.6万,每年肺癌新发病例达78.1万例,相当于平均每10分钟就有15人罹患疾病。预测到2020年,每年新发病例和死亡病例将分别超过80万和70万。
肺癌的种类极其复杂、种类繁多,其中非小细胞肺癌(NSCLC)是肺癌中最常见的类型,约占所有肺癌患者的85%。众多的患者也意味着巨大的市场,对于肺癌的研究与药物开发也一直是国内外在肿瘤领域的关注重点。
在经历了多年的放化疗时代后,2005年中国的肺癌治疗正式进入精准靶向治疗元年,随后的十数年里多款肺癌靶向药物相继上市给患者提供了多种选择,2018年又上市了首个肺癌免疫疗法药物。目前在晚期NSCLC治疗中的应用研究也进行得如火如荼,从二线到一线,从姑息到新辅助,可谓席卷NSCLC治疗的各个领域。
接下来详细介绍一下当前批准应用于肺癌领域的免疫药物。
Pembrolizumab帕博利珠单抗
一线治疗
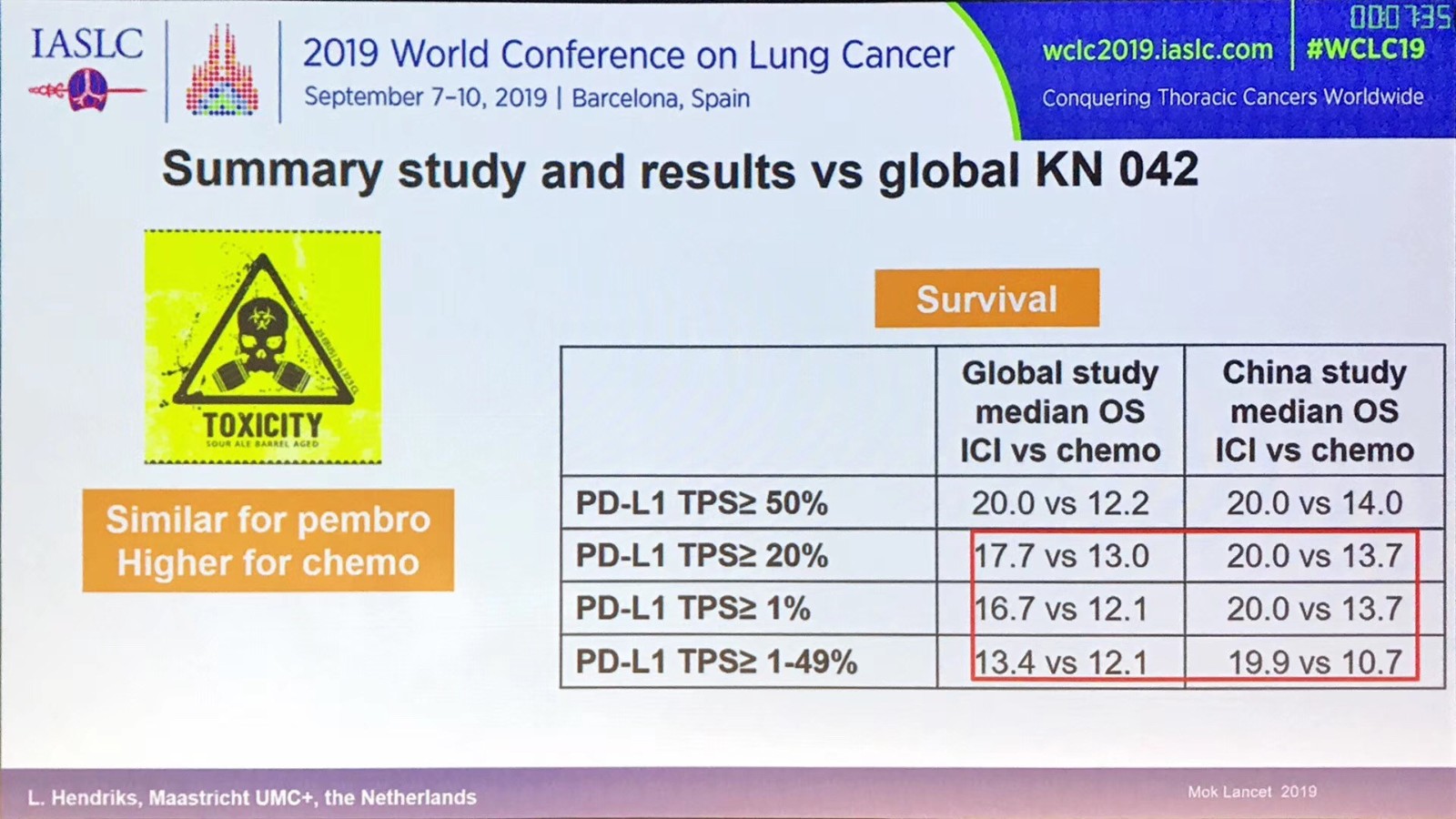
2019年9月30日,中国国家药品监督管理局(NMPA)正式批准默沙东PD-1*制剂抑**药物帕博利珠单抗(pembrolizumab)联合培美曲塞和铂类化疗适用于表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性、PD-L1表达≥1%的局部晚期或转移性非小细胞肺癌(NSCLC)的一线治疗。此次新适应症的获批是基于3期临床试验KEYNOTE-042研究的总生存期(OS)数据,其中包括了中国亚组及中国扩展队列数据。在2019年世界肺癌大会上,广东省人民医院吴一龙教授汇报了KEYNOTE-042中国研究结果,数据显示,一线帕博利珠单抗单药在中国患者中有更好的疗效和安全性。数据截至2018年9月4日,中位随访时间11.3个月,主要终点OS分析,对于PD-L1 TPS≥50%、≥20%和≥1%的患者,帕博利珠单抗单药均显著优于化疗。在PD-L1 TPS≥50%人群中,两组中位OS分别为20.0个月和14.0个月(HR=0.62,95%CI 0.38~1.00);TPS≥20%人群,两组中位OS分别为20.0个月和13.7个月(HR=0.62,95%CI 0.41~0.95);TPS≥1%人群,两组中位OS分别为20.0个月和13.7个月(HR=0.65,95%CI 0.45~0.94)。更令人值得关注的是,在PD-L1 TPS=1~49%人群中,帕博利珠单抗组同样显著优于化疗组,两组中位OS分别为19.9个月和10.7个月(HR=0.69,95%CI 0.40~1.20)。相比全球数据,帕博利珠单抗一线治疗PD-L1 TPS≥1%中国患者在疗效上保持着一致性,同时对于PD-L1 TPS 1~49%患者,中国人群数据疗效更好,并且显著优于化疗。
安全性分析显示,帕博利珠单抗安全性更优,两组3~5级的药物相关不良事件发生率分别为17%和68%。一线帕博利珠单抗单药有望为更多的中国患者带来chemo-free和长期生存。(见下图)
2019年11月25日,国家药品监督管理局(NMPA)官网显示,帕博利珠单抗联合卡铂和紫杉醇一线治疗EGFR基因突变阴性和ALK阴性的转移性鳞状NSCLC的适应证在中国获批。本次帕博利珠单抗新适应证的获批是基于国际多中心、随机、安慰剂对照的Ⅲ期KEYNOTE-407研究结果,11月23日,在2019年欧洲肿瘤内科学会亚洲会议(ESMO Asia)上,吉林省肿瘤医院程颖教授公布了KEYNOTE-407研究中国亚组(包括中国扩展队列)中期分析数据。
KEYNOTE-407研究共纳入125例既往未接受治疗的经病理学确认为鳞状细胞癌的中国大陆Ⅳ期非小细胞肺癌患者,包括无症状脑转移患者,按1∶1随机分配接受帕博利珠单抗(200mg,Q3W)+卡铂(AUC 6,Q3W)+紫杉醇(200mg/m2,Q3W)/白蛋白紫杉醇(100mg/m2,Q1W)或安慰剂+卡铂+紫杉醇/白蛋白紫杉醇治疗4周期,后续分别给予帕博利珠单抗或安慰剂维持治疗,安慰剂组中发生进展的患者可以交叉到帕博利珠单抗单药治疗进行。
研究主要终点为无进展生存期(PFS;盲态独立评审委员会[BIRC]评估)和总生存期(OS)。次要终点包括客观缓解率(ORR),并对PD-L1表达情况不同(TPS>=50%、TPS=1~49%、TPS<1%)的患者群体的OS、PFS和ORR进行预先设定的亚组分析,以评价在中国人群中帕博利珠单抗联合化疗带来的获益情况以及与全球研究结果的一致性。
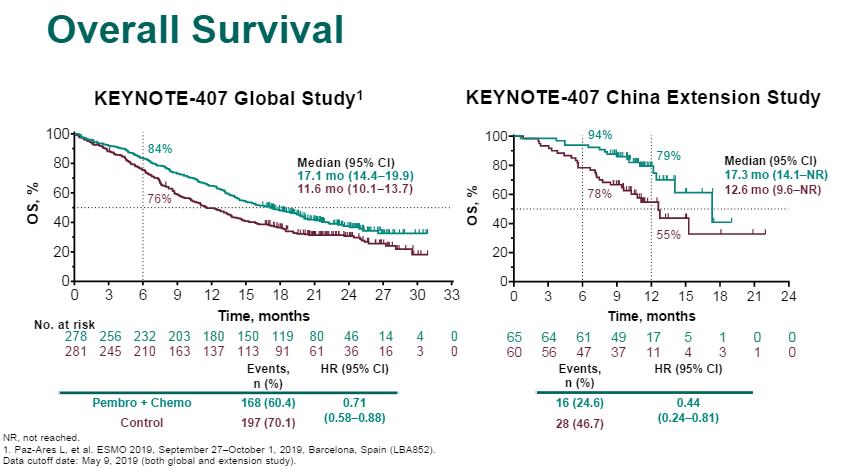
中位随访10.4个月后,结果显示,帕博利珠单抗联合化疗组和化疗组中位OS分别为17.3 个月 vs 12.6个月,联合组较化疗组降低了56%的死亡风险;联合组和化疗组中位PFS分别为8.3个月vs 4.2个月,联合组较化疗组降低了68%的疾病进展或死亡风险;除此之外,相比化疗组,联合治疗组的ORR提升了36.8%(ORR:78.5% vs 41.7%)。(见下图)
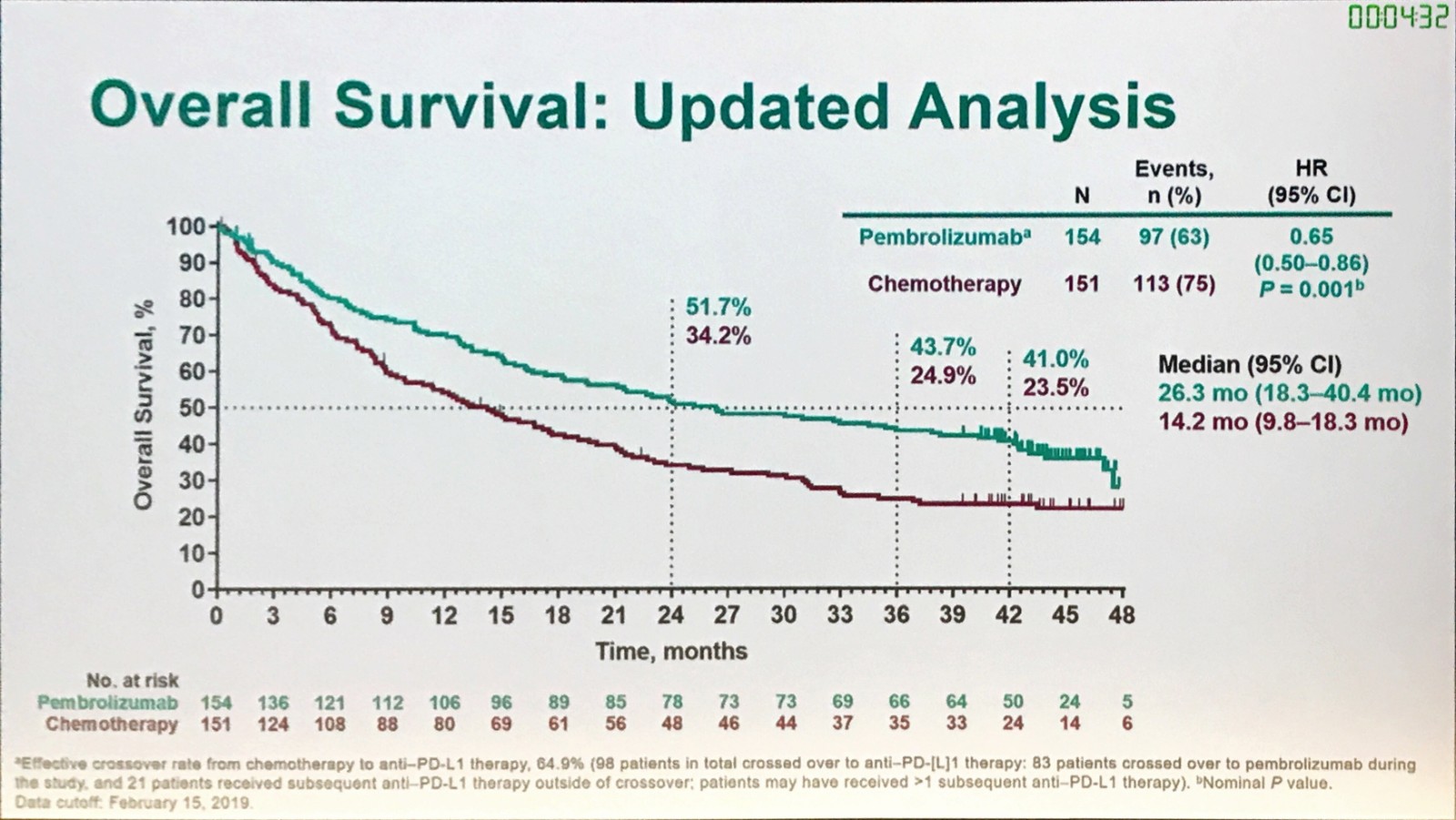
一项国际、随机、开放标签的III期临床研究(Keynote-024):≥50%PD-L1表达的EGFR野生型及ALK无易位的初治晚期非小细胞肺癌患者随机分为Pebroblizumab组和含铂方案的化疗组,免疫治疗组取得了优于化疗组的PFS(10.3个月vs 6.0个月),而3-5度的不良反应却远低于化疗组,分别为免疫组的26.6%与化疗组的53.3%。因此,试验提前终止,化疗组患者进展后使用Pebroblizumab进行治疗。基于该项研究,2016年10月25日,美国FDA批准帕博利珠单抗单药一线治疗EGFR/ALK阴性、PD-L1表达≥50%的转移性NSCLC患者,确立了Pebroblizumab在非小细胞肺癌的一线治疗地位。2019年世界肺癌大会(WCLC)上,Ⅲ期KEYNOTE-024研究的3年随访数据同样证实了一线帕博利珠单抗单药所带来的长期获益。在化疗组有64.9%的患者交叉接受了帕博利珠单抗治疗的情况下,帕博利珠单抗单药对比化疗仍可以为患者带来持久的长期OS获益。两组的中位OS分别为26.3和14.2个月(HR=0.65,95%CI 0.50~0.86,P=0.001),3年的OS率,两组分别为43.7%和24.9%。(见下图)
美国FDA于2019年4月11*批日**准用于一线治疗EGFR/ALK阴性、PD-L1表达≥1%的局部晚期或转移性鳞状或非鳞状NSCLC患者。除此之外,基于KEYNOTE-189和KEYNOTE-407研究结果,帕博利珠单抗联合化疗也先后被美国FDA批准用于EGFR/ALK阴性的晚期非鳞状和鳞状NSCLC一线治疗。
III期KEYNOTE-189研究既往结果显示,中位随访10.5个月时,与安慰剂联合培美曲塞/铂类相比,帕博利珠单抗联合培美曲塞/铂类显著提高了无EGFR/ALK敏感突变的晚期NSCLC患者的OS(HR 0.49;95%CI 0.38~0.64;P<0.001)、PFS(HR, 0.52; 95% CI 0.43~ 0.64; P <0.001)和ORR(47.6% vs 18.9%; P <0.001),且毒性可控。
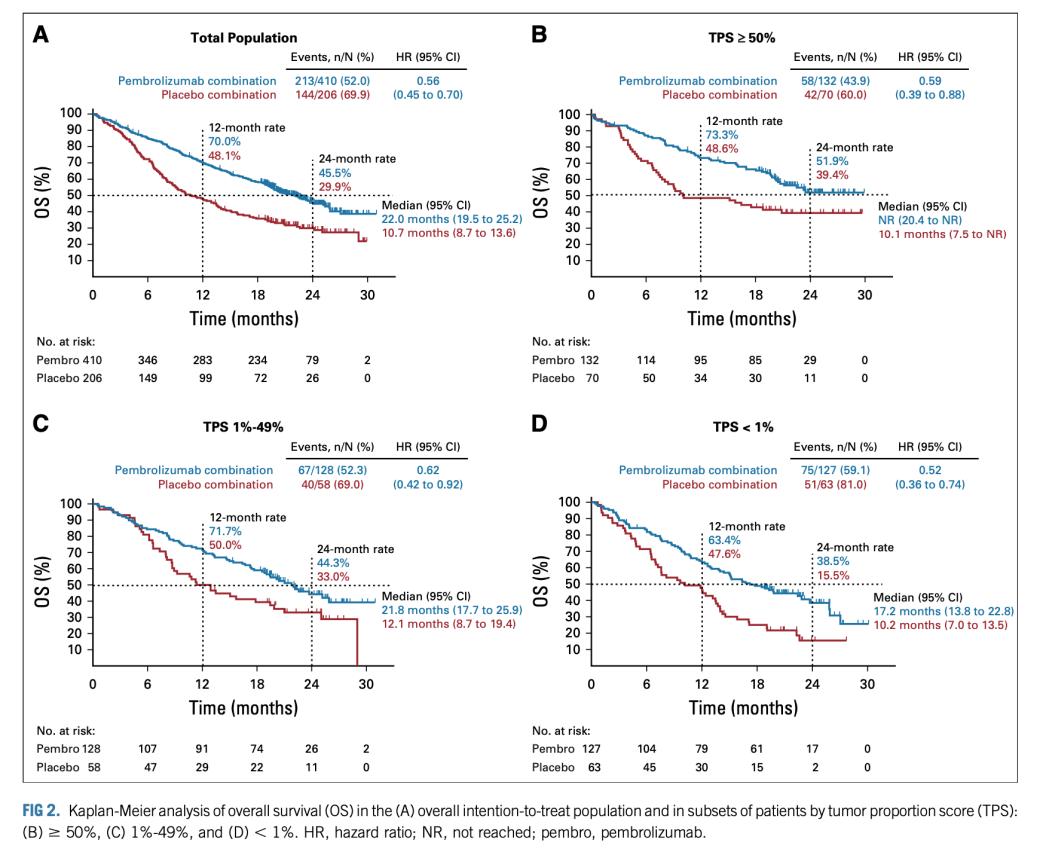
KEYNOTE-189最新分析评估了自首次中期分析数据截止日期起额外再随访约10个月时,帕博利珠单抗联合治疗的有效性和安全性。转移性NSCLC患者经常发生肝、脑转移,且预后差,这种转移是否改变免疫治疗的获益程度还不确定。因此研究还评估了肝/脑转移患者的预后。此外,为确定帕博利珠单抗在二线治疗中的疗效,也对PFS2进行了探索性分析。患者和研究设计:患者为未治的经病理证实转移非鳞状NSCLC,无敏感EGFR/ALK突变,ECOG PS 0~1分,至少一个可测量病灶,有足够肿瘤组织用于PD-L1评估。排除标准包括有症状的中枢神经系统转移、需糖皮质激素治疗的非感染性肺炎病史、活动期自身免疫性疾病或全身性免疫抑制治疗。患者被随机(2:1)分为两组,每3周给予培美曲塞/铂类+帕博利珠单抗(n=410)或安慰剂(n=206)共4个周期,然后给予培美曲塞+帕博利珠单抗或安慰剂维持治疗共35个周期。其中,安慰剂联合组疾病进展患者可以转到帕博利珠单抗单药治疗。通过中央评审按RECIST1.1标准对肿瘤反应进行评估。研究终点:双主要终点为OS和PFS,次要终点为ORR、DOR和安全性。探索性终点为基线肝或脑转移患者的疗效。另外一个探索性终点为PFS2,定义为从随机化开始到后续治疗(包括随后的抗PD-1/L1治疗)中客观肿瘤进展或任何原因死亡的时间。OS(见下图):截止到2018年9月21日,中位随访时间为23.1个月,帕博利珠单抗联合组有213例(52.0%)患者死亡,安慰剂联合组有144例(69.9%)患者死亡。两组的更新中位OS分别为22.0个月(19.5~25.2个月)和10.7个月(8.7~13.6个月)(HR 0.56;95% CI,0.45~0.70)。预计24个月OS率分别为45.5%和29.9%。无论PD-L1表达水平如何,帕博利珠单抗联合治疗都明显提高生存获益。
二线治疗
I期随机临床研究(Keynote-001):这项试验证明了Pembrolizumab的安全性以及PD-L1表达与疗效的正相关。
2019年ASCO会议,KEYNOTE-001 5年随访OS结果更新。KEYNOTE-001研究是迄今为止帕博利珠单抗治疗晚期NSCLC患者的最长期随访研究。该研究于2011年开始招募患者,彼时免疫疗法尚未被广泛应用,因此大多数参与者既往曾接受过全身药物治疗或靶向治疗。
该研究共入组550例晚期NSCLC患者,其中未经治患者101例,经治患者449例。所有患者接受帕博利珠单抗2 mg/kg q21或10 mg/kg q14/21方案治疗,近年来该方案改为单剂量200 mg q21。
结果显示,中位随访60.6个月时,18%的患者(100例)仍生存。未经治患者的5年生存率为23%,经治者为15.5%。PD-L1表达水平较高提示生存时间更长。在未经治患者中,PD-L1表达≥50%时,5年生存率为29.6%;而PD-L1表达<50%者中则为15.7%。经治患者中,PD-L1表达≥50%时,5年生存率为25%,PD-L1表达1%~49%患者为12.6%,PD-L1表达<1%者中仅为3.5%。
经治患者接受帕博利珠单抗治疗后,42%的患者获得了中位16.8个月的缓解持续时间。在帕博利珠单抗一线治疗的患者中,23%的患者获得了中位38.9个月的缓解持续时间。免疫相关不良事件发生率为17%,最常见的为甲状腺功能减退,最严重的为肺炎。
作为帕博利珠单抗在领域随访时间最长的研究数据,这些结果在会上进行了讨论。有与会者表示,过去晚期NSCLC患者的5年生存率约为5%,KEYNOTE-001研究证实帕博利珠单抗用于初治患者5年总生存率达23.2%,经治患者达15.5%,作为医生还是深受鼓舞的。5年生存对晚期NSCLC患者而言具有里程碑式的意义,在KEYNOTE系列首个研究中看到长期总生存数据非常令人鼓舞。
Nivolumab纳武利尤单抗
二线治疗
两项III期临床研究(CheckMate017、CheckMate057):是观察铂类化疗进展后的非小细胞肺癌临床试验,比较了在鳞癌和非鳞癌患者Nivolumab与多西他赛随机分组治疗,结果均表现出免疫治疗组比多西他赛化疗组OS的增加,其中鳞癌患者(9.6个月vs6.0个月),非鳞癌患者(12.2个月vs9.4个月),以及3-4度AEs的降低。通过这两项III期临床研究确立了Nivolumab在非小细胞肺癌中的二线地位。尽管这两项研究结果并未将PD-L1在肿瘤细胞中的表达纳入治疗前检测规范,但结果显示PD-L1的高表达患者确实对Nivolumab表现出更高的有效率。其报道最常见的免疫治疗相关副作用为甲状腺功能减退、结肠炎、肺炎、肾炎和皮疹。
在2019WCLC大会上,CheckMate 017/057两项研究的长期汇总分析数据(5年OS)以口头报告的形式公布,这是目前肿瘤免疫治疗随机III期临床试验中报道过的随访时间最长的数据。CheckMate 017/057研究分别针对二线鳞状和非鳞NSCLC患者,这2项研究的患者均在接受一线含铂化疗期间或之后出现疾病进展,随后以1:1的比例进行随机分组,以评估接受纳武利尤单抗治疗(3mg/kg,每2周给药一次)与标准治疗多西他赛(75 mg/m2,每3周给药一次)的疗效,直到疾病进展或出现不可耐受毒副反应。完成初步分析后,多西他赛组中未见生存获益的患者可交叉进入纳武利尤单抗组进行治疗。主要终点均为总生存(OS),其他终点包括无疾病进展生存(PFS)、客观缓解率(ORR)、根据肿瘤PD-L1表达状态的疗效、安全性和患者报告结局(PROs)等。(5年OS见下图)
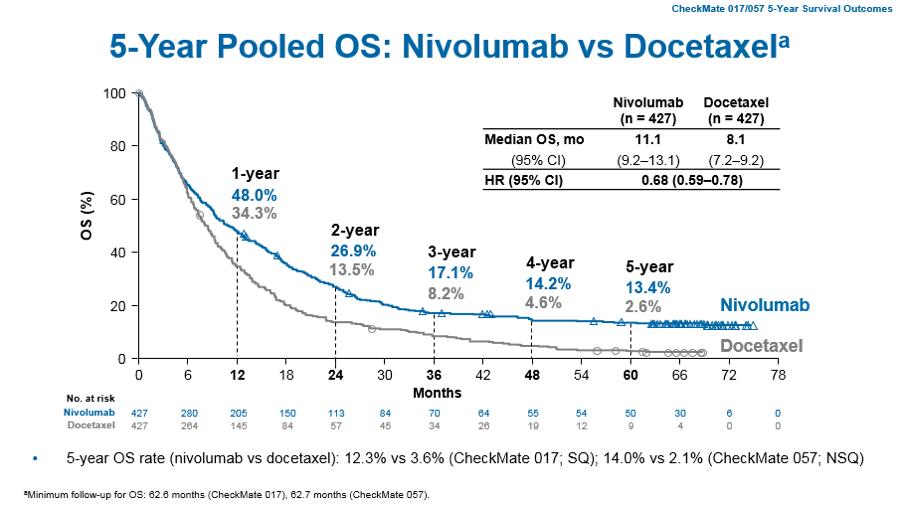
一项多中心、随机III期临床研究(CheckMate 078):比较了纳武利尤单抗与多西他赛在含铂双药化疗治疗后出现疾病进展的IIIb/IV期EGFR和ALK阴性的NSCLC患者中的疗效与安全性。纳武利尤单抗对比多西他赛,显示出显著的生存获益,最短随访8.8个月时,两组的中位OS分别为12.0和9.6个月,中位PFS均为2.8个月,纳武利尤单抗使疾病进展风险降低23%。另外两项次要终点,ORR和中位缓解持续时间(mDOR),纳武利尤单抗也显示出更好的效果。并且,在鳞癌和非鳞癌患者、不同PD-L1表达水平的患者均能获益。治疗相关的3-4级副反应事件在Nivolumab组及多西他赛组分别为11%及52%。
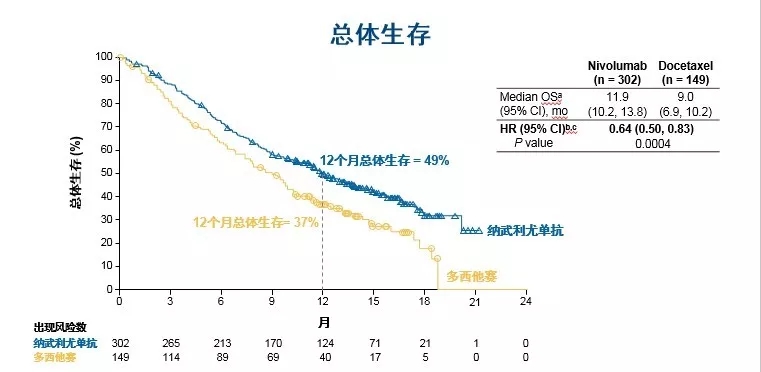
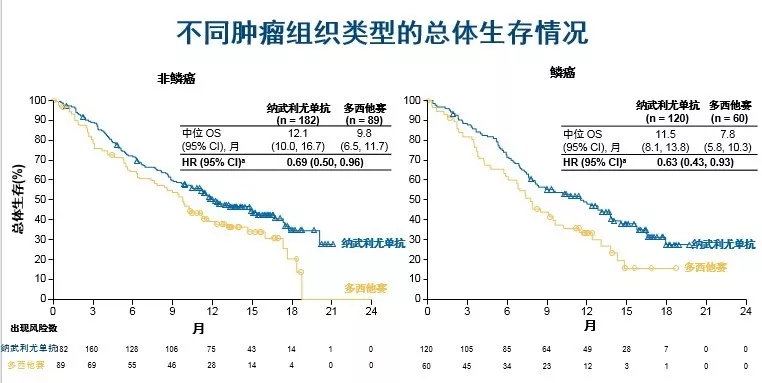
CheckMate 078是第一个以中国人群为主的免疫检查点*制剂抑**的临床研究,验证了其在东亚人群中的卓越疗效和安全性。此前公布的研究数据表明,CheckMate 078研究的总生存、客观缓解率和起效时间,均与CheckMate 017/057数据一致,纳武利尤单抗在亚洲人群同样具有较好疗效,并无人种差异性,可见在二线治疗中,免疫治疗已全面超越化疗。韩宝惠教授表示,"既往的研究中,无论是化疗还是靶向治疗,中国人群的数据均略优于国外数据,这可能与人种特性有关"。对于近几年才进入中国的免疫治疗,中国数据是否能重复甚至优于全球数据?对于CheckMate 078研究,韩教授提到该研究的入组速度非常快,大约1年的时间便入组完毕,表明纳武利尤单抗的患者依从性较好,而且初步疗效显著,患者入组研究的意愿强烈,促成了整个临床研究的顺利开展。基于这项研究,中国药监局于2018年6月批准该药用于晚期NSCLC的二线治疗。(见下图)
INCLUDEPICTURE \d "https://mmbiz.qpic.cn/mmbiz_png/ibGx5uB9xrIsVCm22cXl4HriaibpUersQibhTOzUWcSehCZOFhrS7nHiarC9Aau3HvwnDjx3CtibqyPvfUVqBfbWHwoA/640?wx_fmt=png&tp=webp&wxfrom=5&wx_lazy=1&wx_co=1" \* MERGEFORMATINET
durvalumab度伐利尤单抗注射液
美国FDA于2018年2月批准了Durvalumab(PD-L1*制剂抑**,全人源IgG1单克隆抗体)用于经含铂方案为基础的放化疗后,疾病未进展的Ⅲ期不可切除NSCLC患者的巩固治疗。2019年12月10日午间消息,国家药监局已批准阿斯利康旗下PD-L1药物Imfinzi(durvalumab度伐利尤单抗注射液)、商品名英飞凡上市,用于治疗同步放化疗后未进展的不可切除、III期非小细胞肺癌。此次适应症的获批是基于PACIFIC试验。
2019年美国临床肿瘤学会(ASCO)年会上,Imfinzi(在III期不可切除非小细胞肺癌(NSCLC)的PACIFIC试验的三年总生存率(OS)结果表明,对于接受既往的标准治疗,即同步放化疗后疾病未进展的III期不可切除非小细胞肺癌患者,接受Imfinzi治疗的患者3年的OS率为57%,而安慰剂组为43.5%。Imfinzi组的中位OS尚未达到,而安慰剂组为29.1个月。Imfinzi显示出了持久和持续的OS获益。
Atezolizumab阿替利珠单抗
2月13日,国内抗癌领域传出好消息,又一个PD-L1免疫治疗药获批上市,那就是阿替利珠单抗(T药)!阿替利珠单抗获批联合化疗(卡铂和依托泊苷),一线治疗成人广泛期小细胞肺癌。此次中国获批主要依据全球多中心三期临床试验IMpower133试验结果。
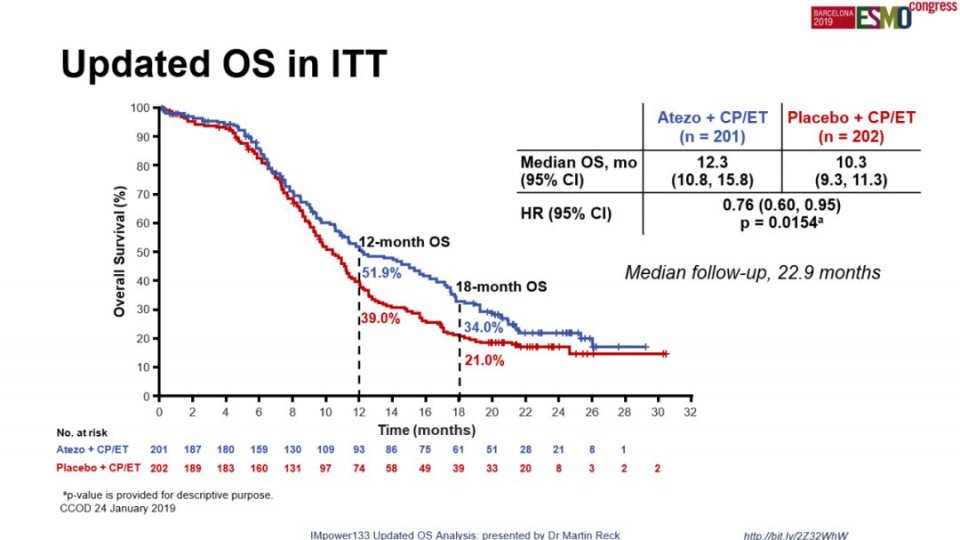
IMpower133试验的结果显示,与单纯化疗方案(卡铂和依托泊)相比,广泛期小细胞肺癌患者使用PD-L1*制剂抑**-阿替利珠单抗联合标准治疗方案-卡铂和依托泊苷可提高生存率。中位随访13.9个月后,联合治疗组的中位总生存期(OS)为12.3个月,而单独化疗为10.3个月,降低该研究受试患者死亡风险30%。(见下图)
2019年第一版NCCN指南将该方案作为广泛期小细胞肺癌一线治疗的优选推荐。之前,广泛期小细胞肺癌常用的标准治疗方案是铂类+依托泊苷,而现在PD-L1 的加入,将改写小细胞肺癌30多年的一线方案。
INCLUDEPICTURE \d "https://mmbiz.qpic.cn/mmbiz_png/ibGx5uB9xrIsVCm22cXl4HriaibpUersQibhFstUrmuBWBsnHdxx4k5toQkyCFdQvRAt9ibQYSNLnTSh0eK4gvCbp3A/640?wx_fmt=png&tp=webp&wxfrom=5&wx_lazy=1&wx_co=1" \* MERGEFORMATINET
信迪利单抗
2020年5月7日,信达生物制药和礼来制药共同宣布:双方共同开发的创新PD-1*制剂抑**达伯舒®(信迪利单抗注射液)的一项随机、双盲、III期对照临床研究(ORIENT-12)——达伯舒®(信迪利单抗注射液,以下简称信迪利单抗)联合健择®(注射用吉西他滨,以下简称吉西他滨)和铂类化疗用于晚期或转移性鳞状非小细胞肺癌(NSCLC)一线治疗达到主要研究终点。这是全球首个评价PD-1抗体联合健择®(吉西他滨)和铂类用于鳞状NSCLC一线治疗的随机、双盲、III期临床研究。达伯舒®联合健择®(注射用吉西他滨)和铂类化疗一线治疗鳞状非小细胞肺癌III期研究ORIENT-12达到主要研究终点。
本研究共入组357例受试者,按照1:1随机入组,分别接受达伯舒®(信迪利单抗注射液)200mg或安慰剂联合健择®(注射用吉西他滨)和铂类治疗,每3周给药1次,完成4或6个周期联合治疗后,进入达伯舒®(信迪利单抗注射液)或安慰剂维持治疗,直至疾病进展、毒性不可耐受或其他需要终止治疗的情况。对照组疾病进展后可有条件交叉至达伯舒®(信迪利单抗注射液)单药治疗。
研究显示信迪利单抗联合吉西他滨和铂类对比安慰剂联合吉西他滨和铂类,显著延长了无进展生存期(PFS),达到预设的研究终点,PFS显著获益,安全性特征与既往报道的信迪利单抗研究结果一致,无新的安全性信号。