

撰文 | 王聪
CAR-T ,即 嵌合抗原受体T细胞免疫疗法 。简单一点说,CAR-T就是把病人的免疫T细胞在体外通过生物技术改造,令其识别肿瘤细胞表面的抗原,然后把这些细胞输回病人体内,达到识别、杀死癌细胞的治疗效果。
2017年, FDA 首次批准了CAR-T疗法上市,用于治疗白血病和淋巴瘤等血液类癌症,CAR-T疗法的成功应用,让许多在等待骨髓配型中绝望的人重新燃起了希望,也标志着细胞治疗时代的到来。
如今,CAR-T已成为针对癌症的免疫疗法中最重要的新进展之一,并在血液肿瘤中取得了许多突破,然而,到目前为止, CAR-T在实体肿瘤中一直未能取得实质性突破 。
在许多癌症类型中,癌细胞表面都有着大量特定蛋白质,但是由于该蛋白质往往在正常组织中也少量存在,这就导致CAR-T细胞无法很好地区分癌细胞和正常细胞,从而导致治疗时正常的细胞和器官遭到攻击,进而导致与治疗相关的致命不良反应。
2021年3月11日, 加州大学旧金山分校 的研究人员在国际顶尖学术期刊 Science 杂志发表了题为:T cell circuits that sense antigen density with an ultrasensitive threshold 的研究论文。
该研究设计了一个 两步正反馈电路 ,可让*伤杀**性T细胞根据S型抗原密度阈值来区分靶标,从而解决了CAR-T细胞疗法对低表达肿瘤抗原的正常细胞的误杀。在表达HER2的癌细胞和小鼠肿瘤模型中, 该方法能够准确、有效的杀死高表达HER2的癌细胞,而不*伤杀**低表达HER2的正常细胞 。
这项研究 找到了将CAR-T细胞疗法应用于实体瘤的解决方案,是CAR-T细胞疗法攻克实体瘤的一个质的飞跃。

HER2 (人表皮生长因子受体-2)是 乳腺癌 、 卵巢癌 ,以及 胃癌 等腹部肿瘤的蛋白标志物。由于基因扩增,HER2的表达在肿瘤中倍增,因此该蛋白质大量存在于肿瘤细胞表面。
理想的治疗性T细胞能够区分表达高抗原密度的肿瘤细胞和表达低抗原量的正常细胞。要想实现这一点,T细胞就需要具有S型超敏剂量反应曲线。
研究团队设计了一个 两步识别 电路,synNotch受体以低亲和力检测抗原(HER2),当完全激活时,该synNotch受体诱导高亲和力CAR的表达。低亲和力的synNotch充当高抗原密度过滤器,高亲和力的CAR激活T细胞的*伤杀**和增殖,充当放大器的作用。
通过这种具有超灵敏抗原密度感应的T细胞设计,低亲和力的synNotch受体作为一个过滤器,只有遇到高表达HER2的肿瘤细胞时,CAR-T细胞才会启动并杀死肿瘤细胞,而遇到低表达HER2的正常细胞,CAR-T细胞则不会启动。
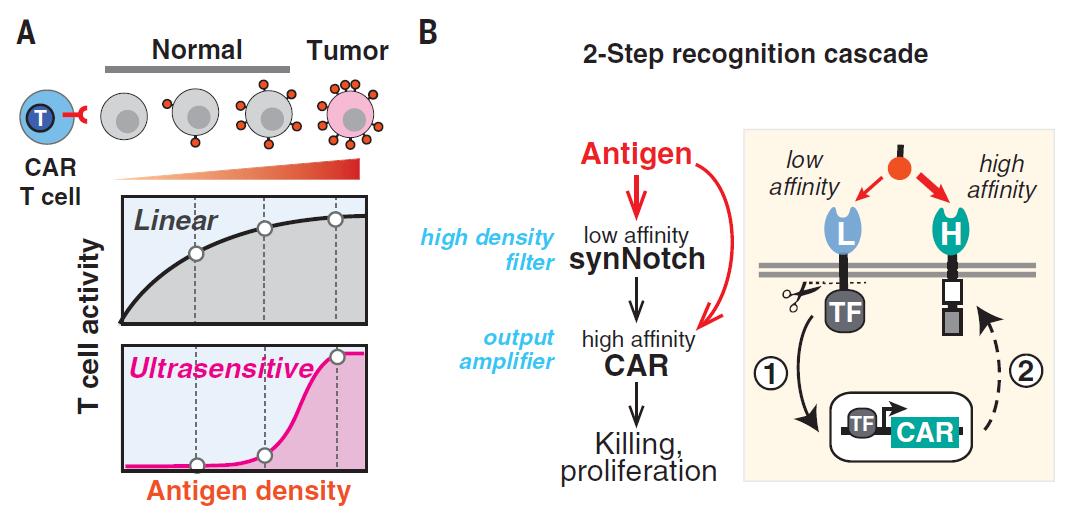
通过这种两步识别电路,对细胞表面的靶蛋白进行机器精确的区分,从而控制CAR-T细胞的功能,通过这一技术, 能够让CAR-T细胞只杀死肿瘤组织中的癌细胞,而不会*伤杀**低表达HER2的正常细胞。
接下来,研究团队在体外细胞水平和小鼠实体瘤模型中进行了验证,实验结果表明,该方法能够准确、有效的杀死癌细胞,而不*伤杀**正常细胞。

虽然,CAR-T实现真正攻克实体瘤,还需要克服其他几个挑战,包括肿瘤异质性、抑制性肿瘤微环境,以及改善T细胞向肿瘤的转运等,但是这项研究实现超灵敏肿瘤抗原密度区分的能力,为扩大CAR-T对实体瘤的治疗范围,提供了关键性工具。
对于这些实验结果,研究团队表示非常兴奋,目前研究团队正在进一步开发该技术,以将其应用于治疗卵巢癌等实体肿瘤。随着研究的进展,研究团队的目标是开发靶向更多抗原的CAR结构,再结合该技术,从而应用于更多的实体肿瘤。这就像“多弹头导弹”一样,癌细胞将难以抵抗。
论文链接:
https://science.sciencemag.org/content/371/6534/1166.full